Clear Sky Science · ru
Статистическая кристаллография выявляет аллостатическую сеть в Mpro SARS-CoV-2
Как смена формы белка помогает ферменту коронавируса работать
Вирус, вызывающий COVID-19, зависит от молекулярного аппарата под названием главная протеаза, который разрезает длинные вирусные полипептиды на рабочие фрагменты. На этот фермент нацелены уже существующие препараты, но исследователи по‑прежнему затрудняются проследить, как его тонкие внутренние движения контролируют переходы между включённым и выключенным состояниями. В этой работе использованы более тысячи снимков протеазы, зафиксированных в кристаллах, чтобы показать, как удалённые области молекулы «переговариваются» с рабочим центром, где идёт химия, и как эта скрытая коммуникация может быть нарушена.
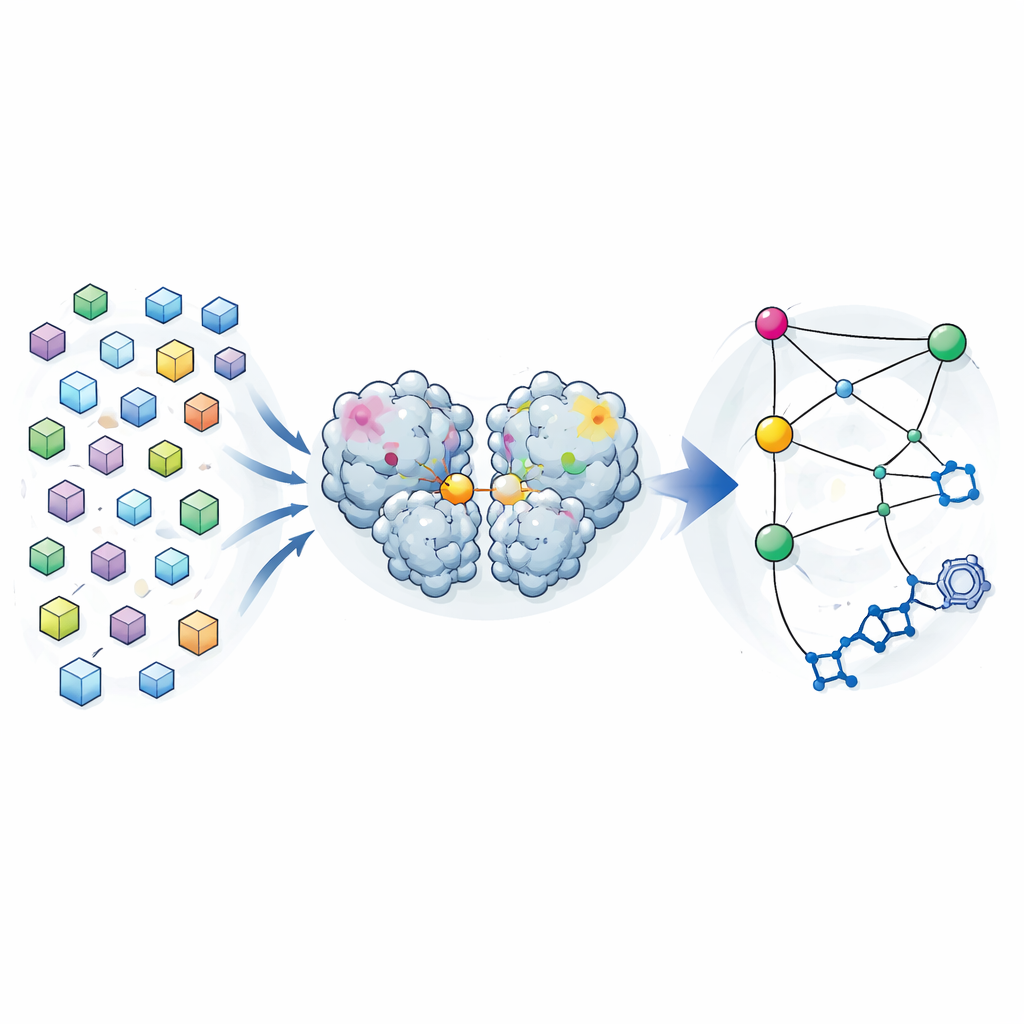
Множество снимков вместо одного
Традиционная кристаллография стремится дать одну «лучшею» структуру белка, усреднённую по множеству молекул в кристалле. Авторы перевернули эту логику. В ходе более ранней кампании по поиску лекарств они собрали дифракционные данные почти с 7000 кристаллов главной протеазы SARS-CoV-2. После тщательной фильтрации образцов с связанными соединениями и применения строгих критериев качества в их распоряжении осталось 1146 высокоразрешающих структур фермента в свободной форме. Вместо того чтобы считать мелкие различия между этими структурами шумом, они проанализировали их как распределение форм, которые протеаза может принимать, оставаясь близкой к рабочему состоянию.
Поиск дальнодействующих связей внутри фермента
Сравнивая, как положение каждого атома меняется от структуры к структуре, команда построила карту ковариаций — некую статистическую «отпечаток», показывающую, какие регионы склонны двигаться синхронно. Они обнаружили, что корреляции, выявленные в кристаллах, во многом совпадали с теми, которые предсказывали длительные молекулярно‑динамические симуляции протеазы в растворе. Это указывало на то, что вариативность, «замороженная» в кристаллах, отражает реальные флексии, которые фермент исследует в воде. Сфокусировавшись на том, как разные области коррелируют с активным сайтом — карманом, где происходит разрезание — исследователи обнаружили три «горячих точки» в домене димеризации протеазы, той части, что помогает двум копиям фермента сдваиваться. Изменения в этих точках, удалённых от активного центра, оказались тесно связаны с перестройками в каталитическом кармане.
Проверка «горячих точек» таргетными изменениями
Чтобы понять, действительно ли статистически выделенные сайты управляют функцией, исследователи изменили каждую «горячую точку», заменив одну аминокислоту на аланин — стандартный приём для небольшого локального сдвига структуры. Затем они измерили, насколько хорошо каждый мутантный фермент образует димеры, связывает фрагмент, имитирующий субстрат, и расщепляет флуоресцентный тестовый пептид. Одна позиция, N214, показала себя подтверждённой «аллостатической горячей точкой»: мутация ослабляла образование димеров более чем в десять раз и даже при наличии достаточного числа димеров скоростной показатель катализа падал примерно на порядок. Высокорасполагающие структуры мутанта раскрыли причину: локальная сеть водородных связей, обычно стабилизирующая ключевую петлю, формирующую «оксанионное гнездо» в активном сайте, была нарушена, и эта петля частично потеряла порядок и выровненность, нужную для химии.
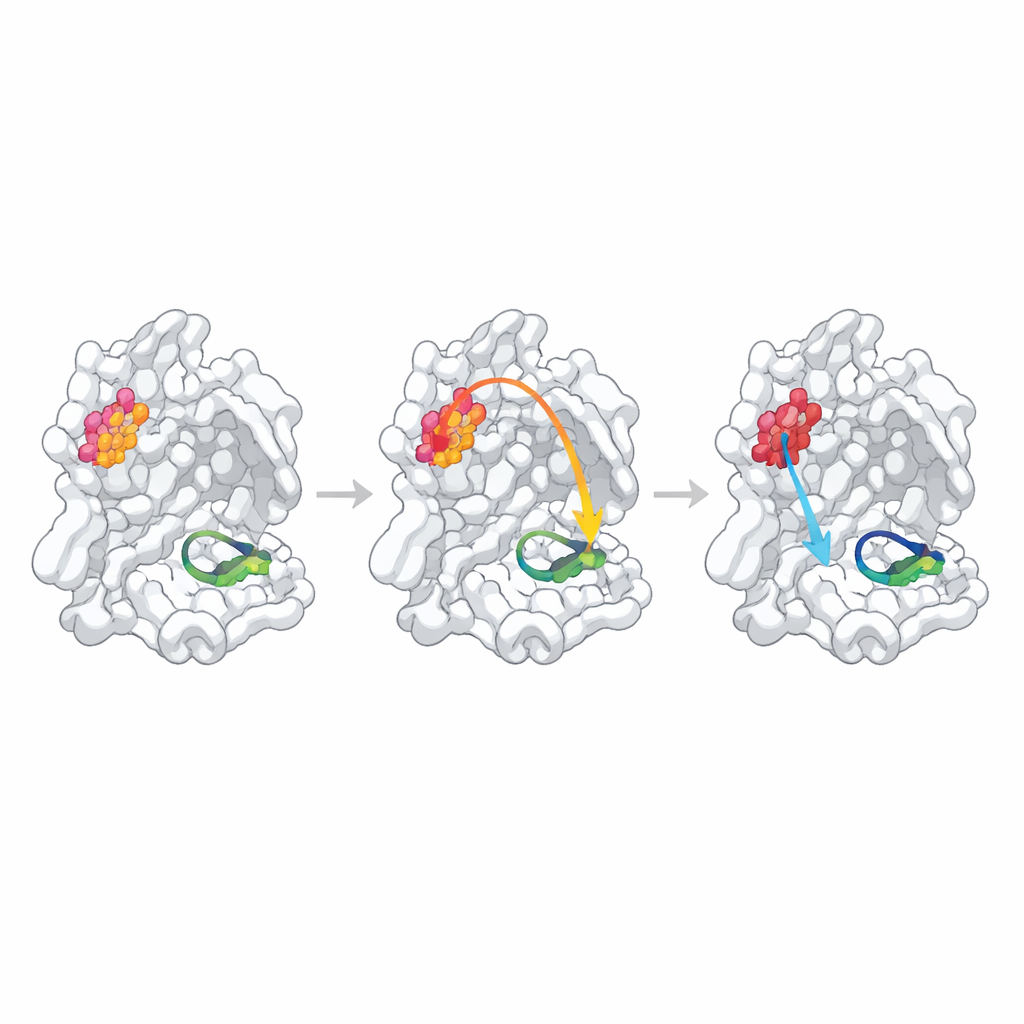
Когда предсказанные связи слабы или скрыты
Две другие предсказанные «горячие точки» вели себя иначе. Замена Q256, остатка, обращённого к раствору и явно не вовлечённого в контакты димеризации, привела лишь к умеренному снижению активности, которое в значительной степени объяснялось слегка ослабленным образованием димеров и несколько худшим связыванием тестового ингибитора. Его кристаллическая структура показала совершенно новую упаковку, где соседние молекулы заполнили пустоту, образованную мутацией, что усложнило отделение истинной внутренней коммуникации от кристалло‑специфических эффектов. Третий сайт, S284, расположен в небольшом «молнии‑застёжке», соединяющей две копии фермента. Как и следовало ожидать по сравнению с последовательностями родственных коронавирусов, замена этого остатка практически не повлияла ни на структуру, ни на функцию, что указывает на то, что данная аланиновая замена была слишком мягким возмущением, чтобы протестировать предсказанный путь.
Кристаллы как мини‑силовые эксперименты
Любопытный побочный вывод работы заключается в том, что многие различия между структурами кристаллов можно было проследить до крошечных изменений в кристаллической решётке — повторяющемся расположении белков и растворителя. По мере того как кристаллы слегка высыхали при обращении с ними, их элементарные ячейки сжимались или растягивались, и эти сдвиги тянули за собой точки контакта между соседними молекулами протеазы. Эти силы распространялись через белок, порождая структурное разнообразие, на котором базировался анализ ковариаций. Иными словами, каждый кристалл выступал как небольшое механическое испытание, деликатно растягивая протеазу в разных направлениях и показывая, как она изгибается, не разрушаясь.
Почему это важно для биологии и разработки лекарств
Рассматривая тысячи кристаллических структур как статистическую популяцию, а не как единственный ответ, авторы смогли вывести аллостатическую сеть, которая связывает остаток интерфейса димера N214 с каталитическим центром главной протеазы SARS-CoV-2. Нарушение этого сайта не просто уменьшает число образующихся димеров; оно конкретно искажает геометрию активной петли, необходимую для эффективного катализа. Это подтверждает, что активность фермента управляется дальнодействующей коммуникацией по всему белку. В более широком смысле исследование демонстрирует подход «статистической кристаллографии», в котором неконтролируемые, повседневные возмущения кристаллов — например, небольшие различия в степени высыхания — становятся ресурсом для картирования функциональных движений. По мере накопления подобных наборов данных для других белков эта стратегия может помочь обнаруживать новые регуляторные сайты и направлять дизайн лекарств, действующих не только путём блокировки активных центров, но и путём перенастройки внутренних «разговоров», которые задают работу белков.
Цитирование: Creon, A., Scheer, T.E.S., Reinke, P. et al. Statistical crystallography reveals an allosteric network in SARS-CoV-2 Mpro. Commun Biol 9, 602 (2026). https://doi.org/10.1038/s42003-026-10127-w
Ключевые слова: главная протеаза SARS-CoV-2, аллостерия, динамика белков, кристаллография, поиск лекарств