Clear Sky Science · zh
粘杆菌素与细菌素的组合能阻止粘单胞菌中粘杆菌素耐药性的产生
这对医院感染意味着什么
在医院获得的耐药感染越来越难以治疗。其中最令人担忧的病原体之一是鲍曼不动杆菌(Acinetobacter baumannii),它能抵御几乎所有可用抗生素。医生常常不得不依赖粘杆菌素这种强效的“最后手段”药物。但随着细菌进化出耐药性,即便是粘杆菌素也开始失效。本研究探讨了将粘杆菌素与天然细菌肽——细菌素结合,是否既能更有效地杀死这些顽固微生物,又能减缓耐药性的出现。
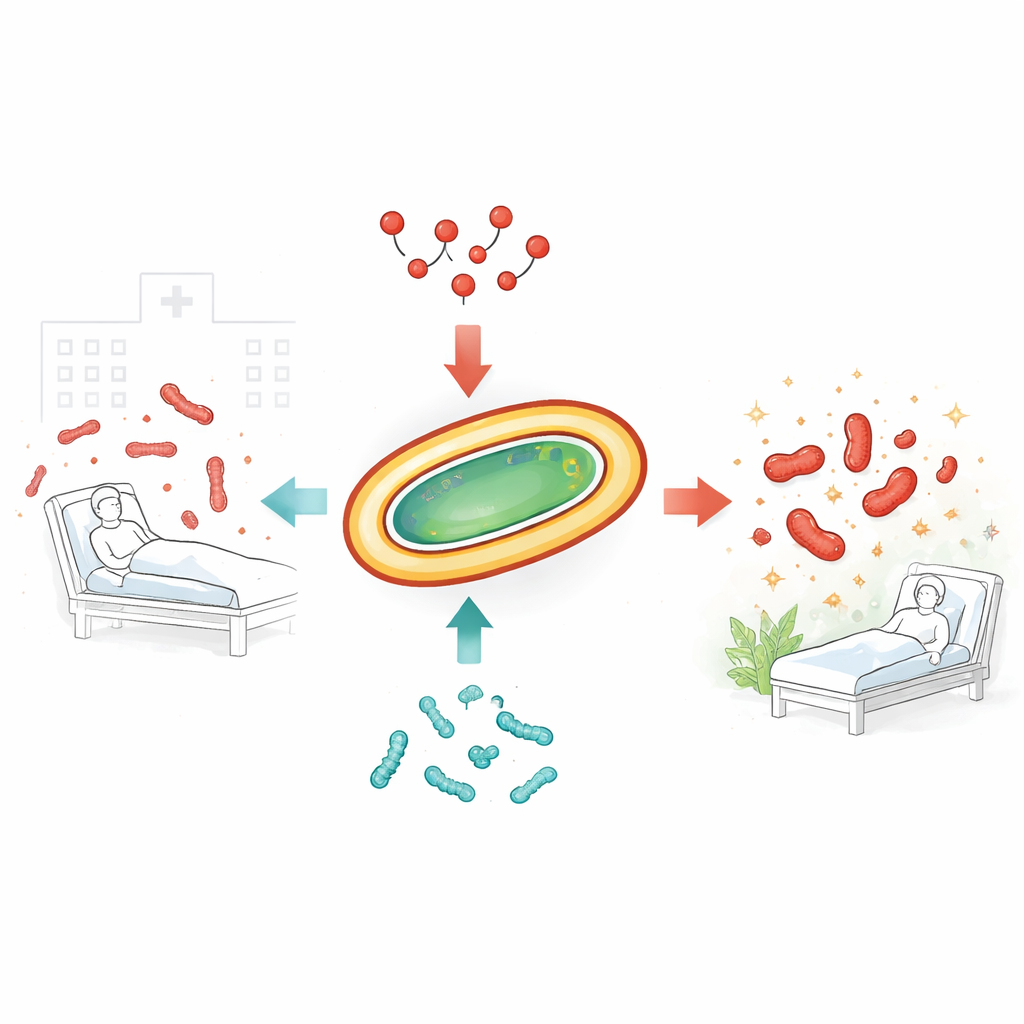
比抗生素更难对付的强悍细菌
研究人员重点研究了几株近期临床分离的鲍曼不动杆菌,这些菌株来自真实患者并已对多种常用药物产生耐药性。基因分析显示,这些菌株在DNA序列和携带的耐药基因类型上都存在差异。标准测试证实大多数菌株仍对粘杆菌素敏感,但有一株高度耐药。研究者将粘杆菌素与医院常用的其他常规抗生素(如替加环素或亚胺培南)联合使用时,最多只出现相加效应,而非能显著增强杀菌并抑制耐药性的真正协同效应。
天然细菌武器加入战斗
许多细菌产生微小的蛋白质武器,称为细菌素,用以抵御竞争对手。研究团队筛选了一组此类分子,发现几种由无害的革兰氏阳性细菌产生的细菌素能够抑制鲍曼不动杆菌,尽管只在较高剂量下有效。他们选择了两种小型螺旋肽——乳酸菌素Z(Lacticin Z)和肠球菌素L50(Enterocin L50)进行深入研究。在试管中的膜模型实验中,这两种肽都能强烈结合模拟鲍曼不动杆菌内膜的脂质混合物,并能在这些人工囊泡上打孔。然而,对完整细菌的影响要小得多,这表明细菌的外表层充当了屏障,阻止肽到达其首选靶点。
粘杆菌素打开缺口,细菌素完成杀伤
粘杆菌素通过与革兰氏阴性菌外层的一种脂质成分结合并扰乱膜的结构来发挥作用。在鲍曼不动杆菌中,作者展示了粘杆菌素不仅使外膜变得渗漏,还扰乱了内膜的电位并耗竭了细胞的ATP(主要能量货币)。单独使用粘杆菌素常常无法完全清除培养物中的所有细胞:一些细菌幸存,随着时间推移带有特定膜相关基因改变的突变体出现并变得高度耐药。当研究者在粘杆菌素中加入低剂量、单独无效的乳酸菌素Z或肠球菌素L50时,细菌存活率显著下降。该组合还阻止或大幅减少了通常预示耐药突变体兴起的再生现象,即便在模拟已部分丢失典型外层分子的菌株中亦如此。
从两个方向攻击细胞包膜
为了理解这种协作机制,团队探查了多种削弱细菌表面的方式。阻断外层脂质(脂质A)合成的化学物质或破坏外膜稳定性的化合物使鲍曼不动杆菌对细菌素更为敏感,支持了外层屏障一旦受损,肽便能到达并破坏内膜的观点。细菌素还增强了以细胞壁外层为靶的抗生素亚胺培南的活性,尤其是在该药物已经开始扰乱包膜时。重要的是,将粘杆菌素与乳酸菌素Z或肠球菌素L50联合使用不仅能杀死更多细胞,还大幅降低了稳定遗传耐药突变体的出现率。幸存的细胞更倾向于是短暂耐受而非永久耐药。
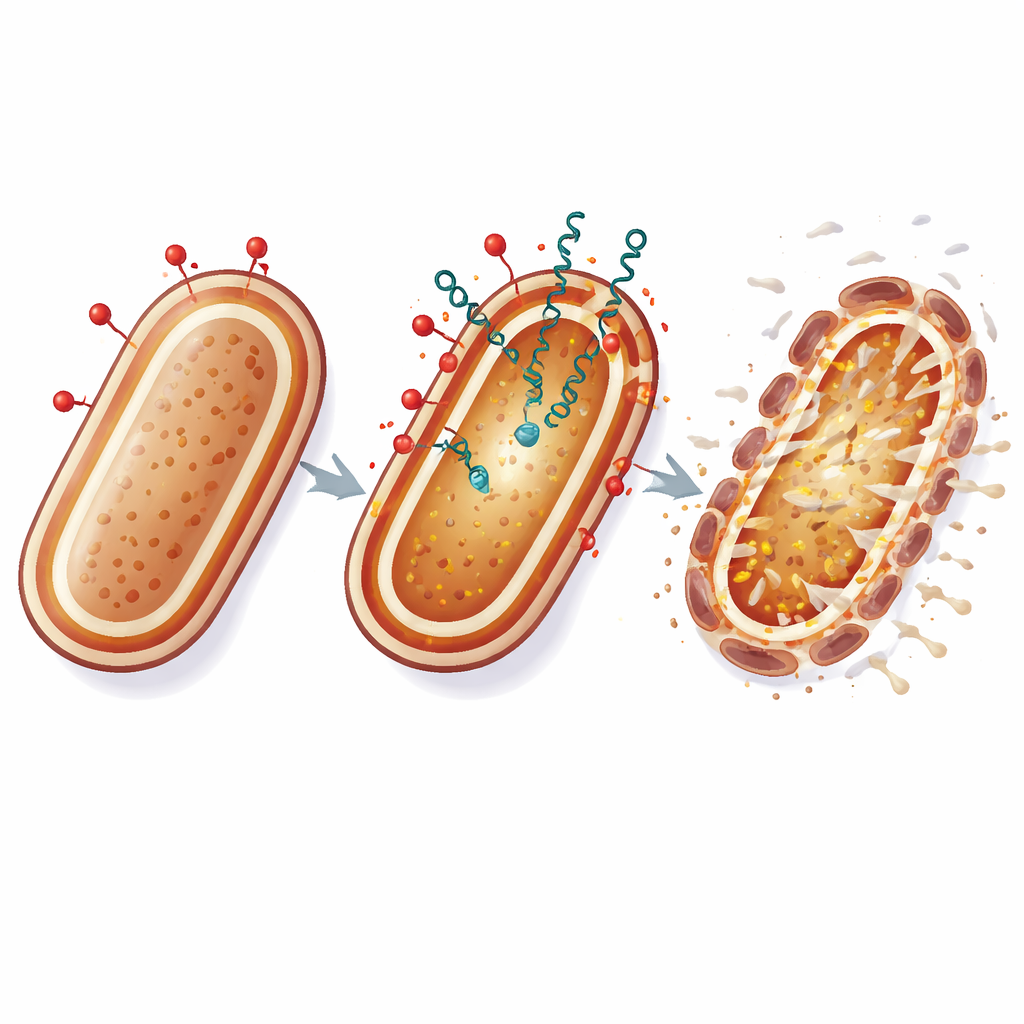
这对未来治疗可能意味着什么
通俗地说,粘杆菌素像一把撬棍撬开细菌的外层盔甲,而细菌素则从缝隙中溜入攻击维持生命的内膜。通过同时攻击细胞包膜的两个脆弱点,这一策略使鲍曼不动杆菌通过简单的遗传调整来适应变得更加困难。尽管这些实验在实验室中完成,但结果表明,精心挑选的传统抗生素与天然细菌肽的组合可能延长最后手段药物的有效期,并为 otherwise 无法治疗的医院感染提供新的治疗选择。
引用: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
关键词: 抗生素耐药性, 鲍曼不动杆菌, 粘杆菌素, 细菌素, 联合用药