Clear Sky Science · it
Combinazioni di colistina e batteriocine prevengono la selezione di resistenza alla colistina in Acinetobacter baumannii
Perché questo conta per le infezioni ospedaliere
Le infezioni resistenti ai farmaci contratte negli ospedali stanno diventando sempre più difficili da curare. Uno dei colpevoli più preoccupanti è il batterio Acinetobacter baumannii, che può resistere a quasi tutti gli antibiotici disponibili. I medici spesso devono ricorrere alla colistina, un potente farmaco “di ultima istanza”. Ma anche la colistina comincia a fallire mentre i batteri evolvono resistenza. Questo studio esplora se affiancare la colistina a peptidi naturali prodotti da batteri, detti batteriocine, possa sia uccidere questi microrganismi ostinati in modo più efficace sia rallentare l’emergere della resistenza.
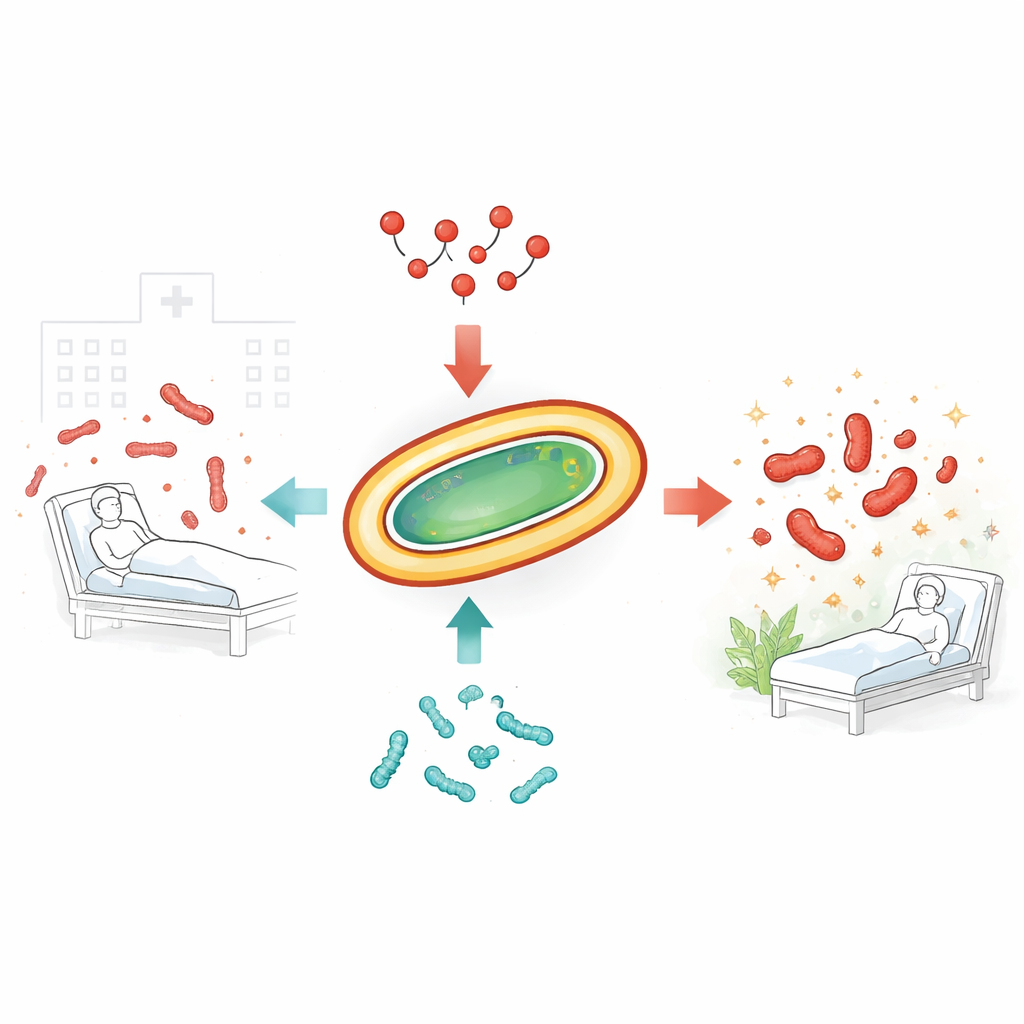
I germi ostinati che mettono in difficoltà gli antibiotici
I ricercatori si sono concentrati su diversi isolati clinici recenti di A. baumannii, raccolti da pazienti reali e già resistenti a molti farmaci comunemente usati. L’analisi genetica ha mostrato che questi ceppi erano diversi tra loro, sia nel DNA sia nei tipi di geni di resistenza che portavano. I test standard hanno confermato che la maggior parte era ancora sensibile alla colistina, mentre uno ceppo risultava altamente resistente. Quando gli scienziati hanno provato a combinare la colistina con altri antibiotici convenzionali spesso impiegati in ospedale, come tigeciclina o imipenem, le associazioni hanno prodotto al massimo un effetto additivo, non la vera sinergia che potrebbe aumentare significativamente l’uccisione e frenare la resistenza.
Armi naturali dei batteri entrano in campo
Molti batteri producono piccole armi proteiche, chiamate batteriocine, per difendersi dai concorrenti. Il gruppo ha esaminato una serie di queste molecole e ha scoperto che diverse, prodotte da batteri Gram-positivi innocui, potevano inibire A. baumannii, sebbene solo a dosi elevate. Hanno selezionato due piccoli peptidi elicoidali — Lacticin Z ed Enterocin L50 — per uno studio più approfondito. In modelli di membrana in provetta, entrambi si legavano fortemente a miscele di lipidi che imitano la membrana interna di A. baumannii e potevano perforare queste vescicole artificiali. Tuttavia, i batteri intatti erano molto meno colpiti, suggerendo che lo strato esterno della cellula funge da scudo, impedendo ai peptidi di raggiungere il loro bersaglio preferito.
La colistina apre la porta, le batteriocine finiscono il lavoro
La colistina agisce legandosi a un componente lipidico del rivestimento esterno dei batteri Gram-negativi e disturbando la struttura delle loro membrane. In A. baumannii, gli autori hanno mostrato che la colistina non solo rende la membrana esterna permeabile, ma altera anche il potenziale elettrico della membrana interna e prosciuga la cellula dell’ATP, la sua principale valuta energetica. Da sola, la colistina spesso non riusciva ad eliminare tutte le cellule in una coltura: alcune sopravvivevano e, nel tempo, comparivano mutanti con modifiche in specifici geni legati alle membrane che diventavano altamente resistenti. Quando i ricercatori hanno aggiunto basse dosi di Lacticin Z o Enterocin L50, altrimenti inattive, insieme alla colistina, la sopravvivenza batterica è calata drasticamente. La combinazione ha anche impedito o ridotto fortemente il ricrescimento che di solito segnalava l’emergere di mutanti resistenti, anche quando i microrganismi imitavano ceppi che avevano parzialmente perso le molecole tipiche dello strato esterno.
Colpire l’involucro cellulare da due lati
Per capire come funziona questa collaborazione, il gruppo ha analizzato diversi modi per indebolire la superficie batterica. Sostanze chimiche che bloccano la sintesi del lipide dello strato esterno (lipid A) o che destabilizzano la membrana esterna rendevano A. baumannii più vulnerabile alle batteriocine, sostenendo l’idea che una volta compromesso lo scudo esterno i peptidi possano raggiungere e danneggiare la membrana interna. Le batteriocine hanno anche aumentato l’attività di un antibiotico che prende di mira la parete cellulare esterna, l’imipenem, quando quel farmaco aveva già iniziato a disturbare l’involucro. È importante notare che la combinazione di colistina con Lacticin Z o Enterocin L50 non solo uccideva più cellule, ma riduceva nettamente anche la comparsa di mutanti geneticamente e stabilmente resistenti. Le cellule sopravvissute tendevano a essere temporaneamente tolleranti piuttosto che permanentemente resistenti.
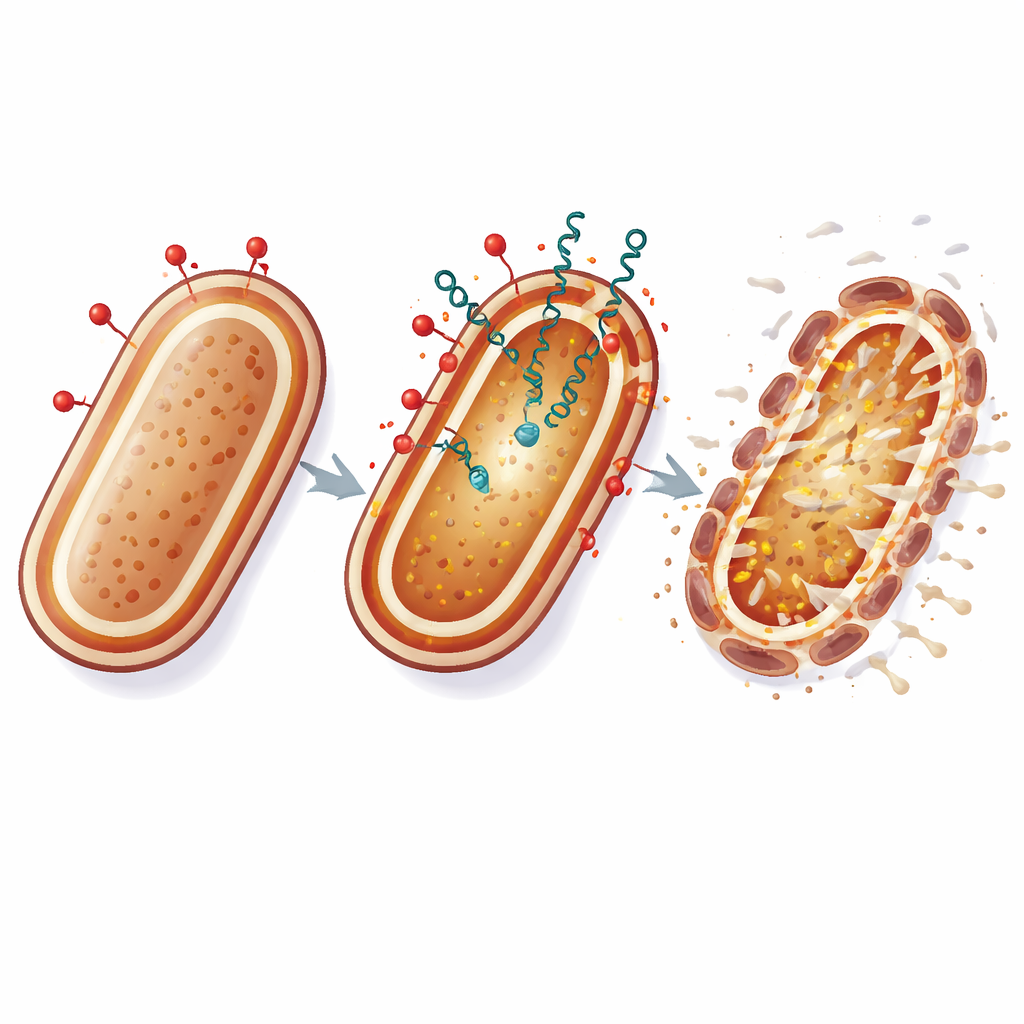
Cosa potrebbe significare per i trattamenti futuri
In termini pratici, la colistina agisce come un piede di porco che apre l’armatura esterna del batterio, mentre le batteriocine si insinuano attraverso le fessure e attaccano la membrana interna che sostiene la vita. Colpendo l’involucro cellulare in due punti vulnerabili contemporaneamente, questa strategia rende molto più difficile per A. baumannii adattarsi tramite semplici modifiche genetiche. Sebbene questi esperimenti siano stati condotti in laboratorio, i risultati suggeriscono che combinazioni scelte con cura di antibiotici tradizionali con peptidi batterici naturali potrebbero estendere la vita utile dei farmaci di ultima istanza e offrire nuove opzioni contro infezioni ospedaliere altrimenti intrattabili.
Citazione: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
Parole chiave: resistenza agli antibiotici, Acinetobacter baumannii, colistina, batteriocine, terapia combinata