Clear Sky Science · sv
Kombinationer av kolistin och bakteriociner förhindrar urval av kolistinresistens i Acinetobacter baumannii
Varför detta spelar roll för sjukhusinfektioner
Läkemedelsresistenta infektioner som förvärvas på sjukhus blir allt svårare att behandla. En av de mest oroande bovarna är en bakterie kallad Acinetobacter baumannii, som kan stå emot nästan alla tillgängliga antibiotika. Läkare tvingas ofta använda kolistin, ett potent "sista utvägen"-läkemedel. Men även kolistin börjar misslyckas när bakterierna utvecklar resistens. Denna studie undersöker om kombinationen av kolistin med naturliga bakteriella peptider, så kallade bakteriociner, både kan döda dessa envisa mikrober mer effektivt och bromsa uppkomsten av resistens.
De hårdföra mikroberna som överlistar antibiotika
Forskarna fokuserade på flera nyligen isolerade kliniska stammar av A. baumannii, tagna från riktiga patienter och redan resistenta mot många vanliga läkemedel. Genetiska analyser visade att dessa stammar var varierade, både i sitt DNA och i vilka resistensgener de bar. Standardtester bekräftade att de flesta fortfarande var känsliga för kolistin, medan en stam var starkt resistent. När forskarna försökte kombinera kolistin med andra konventionella antibiotika som ofta används på sjukhus, såsom tigecyklin eller imipenem, gav parningarna högst en additiv effekt, inte den verkliga synergism som kraftigt skulle kunna öka bakteriedödandet och dämpa resistensutveckling.
Naturens bakterievapen går med i kampen
Många bakterier tillverkar egna små proteinvapen, kallade bakteriociner, för att försvara sig mot konkurrenter. Teamet screenade en panel av dessa molekyler och fann att flera som produceras av ofarliga grampositiva bakterier kunde hämma A. baumannii, om än endast vid höga doser. De valde ut två små, helixformade peptider—Lacticin Z och Enterocin L50—för fördjupade studier. I provrörsmodeller av membran fäste båda starkt vid blandningar av lipider som efterliknar A. baumannii:s inre membran och kunde göra hål i dessa artificiella vesiklar. Helt intakta bakterier påverkades dock mycket mindre, vilket tyder på att bakteriens yttre ytskikt fungerar som en sköld som förhindrar peptiderna från att nå sitt föredragna mål.
Kolistin öppnar dörren, bakteriocinerna fullbordar jobbet
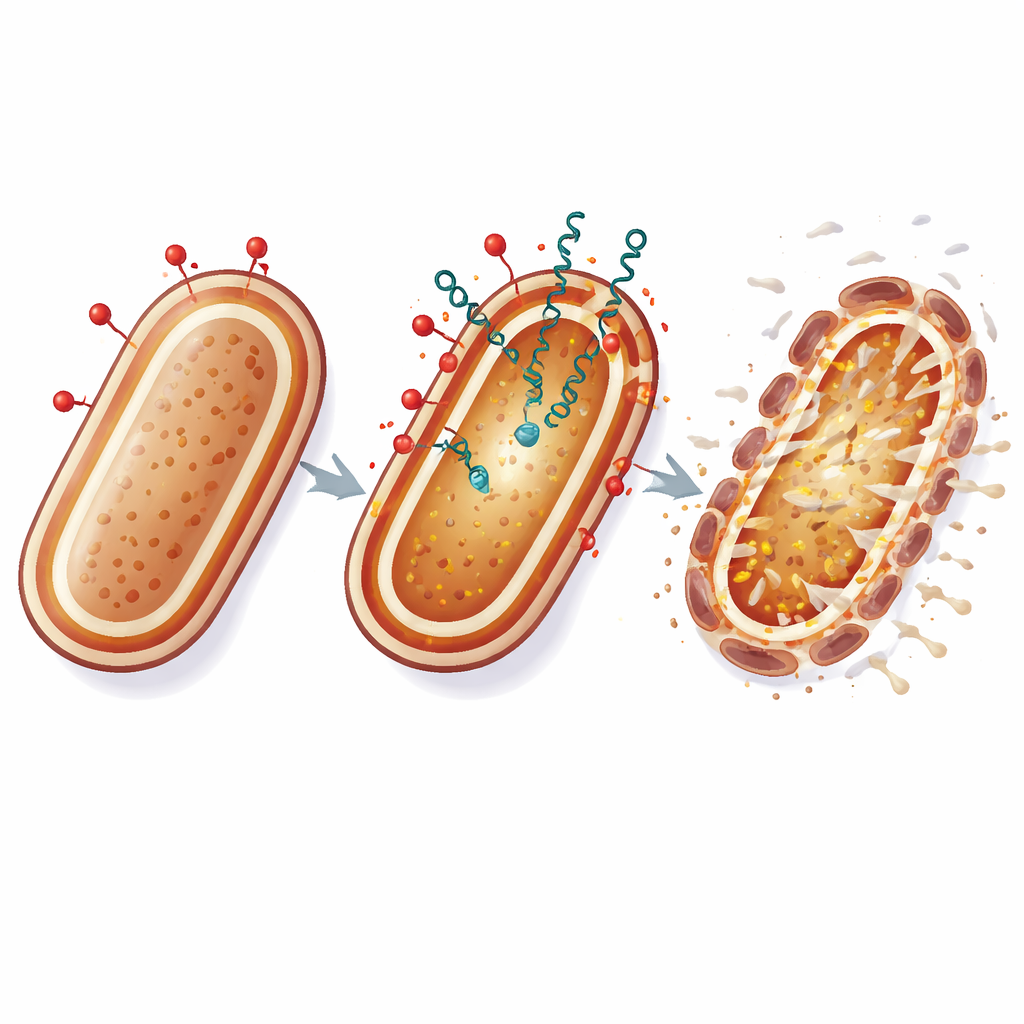
Kolistin verkar genom att binda till en lipidkomponent i det yttre skiktet hos gramnegativa bakterier och störa membranstrukturen. I A. baumannii visade författarna att kolistin inte bara gör det yttre membranet läckande utan också rubbar det inre membranets elektriska potential och uttömmer cellens ATP, dess huvudsakliga energivaluta. Ensam behandling med kolistin lyckades ofta inte utplåna alla celler i en odling: vissa bakterier överlevde och med tiden uppträdde mutanter med förändringar i specifika membranrelaterade gener som blev starkt resistenta. När forskarna tillsatte låga, i annat fall inaktiva doser av Lacticin Z eller Enterocin L50 tillsammans med kolistin sjönk bakterieöverlevnaden dramatiskt. Kombinationen förhindrade eller minskade också starkt den återväxt som vanligtvis signalerar framväxten av resistenta mutanter, även när de efterliknade stammar som delvis förlorat sina typiska ytskiktsmolekyler.
Att angripa cellkapseln från två håll
För att förstå hur detta partnerskap fungerar undersökte teamet olika sätt att försvaga bakterieytan. Kemikalier som blockerar syntesen av det yttre skiktets lipid (lipid A) eller som destabiliserar det yttre membranet gjorde A. baumannii mer sårbar för bakteriocinerna, vilket stödjer idén att när den yttre skölden komprometteras kan peptiderna nå och skada det inre membranet. Bakteriocinerna ökade också aktiviteten hos ett yttre cellväggs–riktat antibiotikum, imipenem, när det läkemedlet redan börjat störa höljet. Viktigt är att kombinationen av kolistin med Lacticin Z eller Enterocin L50 inte bara dödade fler celler utan också kraftigt minskade framkomsten av stabila, genetiskt resistenta mutanter. De överlevande cellerna tenderade att vara tillfälligt toleranta snarare än permanent resistenta.
Vad detta kan innebära för framtida behandlingar
I vardagstermer fungerar kolistin som ett brytjärn som bryskt öppnar bakteriens yttre rustning, medan bakteriociner glider in genom sprickorna och attackerar det inre membranes livsuppehållande funktioner. Genom att slå mot cellhöljet på två sårbara punkter samtidigt blir det mycket svårare för A. baumannii att anpassa sig med enkla genetiska justeringar. Även om dessa experiment gjordes i laboratoriemiljö tyder resultaten på att noggrant utvalda kombinationer av traditionella antibiotika och naturliga bakteriella peptider skulle kunna förlänga nyttan av sista utvägens läkemedel och erbjuda nya alternativ mot annars obotliga sjukhusinfektioner.
Citering: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
Nyckelord: antibiotikaresistens, Acinetobacter baumannii, kolistin, bakteriociner, kombinationsbehandling