Clear Sky Science · es
Combinaciones de colistina y bacteriocinas evitan la selección de resistencia a la colistina en Acinetobacter baumannii
Por qué esto importa para las infecciones hospitalarias
Las infecciones resistentes a fármacos adquiridas en hospitales son cada vez más difíciles de tratar. Uno de los culpables más preocupantes es una bacteria llamada Acinetobacter baumannii, que puede resistir casi todos los antibióticos disponibles. Con frecuencia, los médicos deben recurrir a la colistina, un fármaco potente de “último recurso”. Pero incluso la colistina comienza a fallar a medida que las bacterias desarrollan resistencia. Este estudio explora si asociar la colistina con péptidos bacterianos naturales llamados bacteriocinas puede tanto matar estos microbios difíciles de manera más eficaz como frenar la aparición de resistencia.
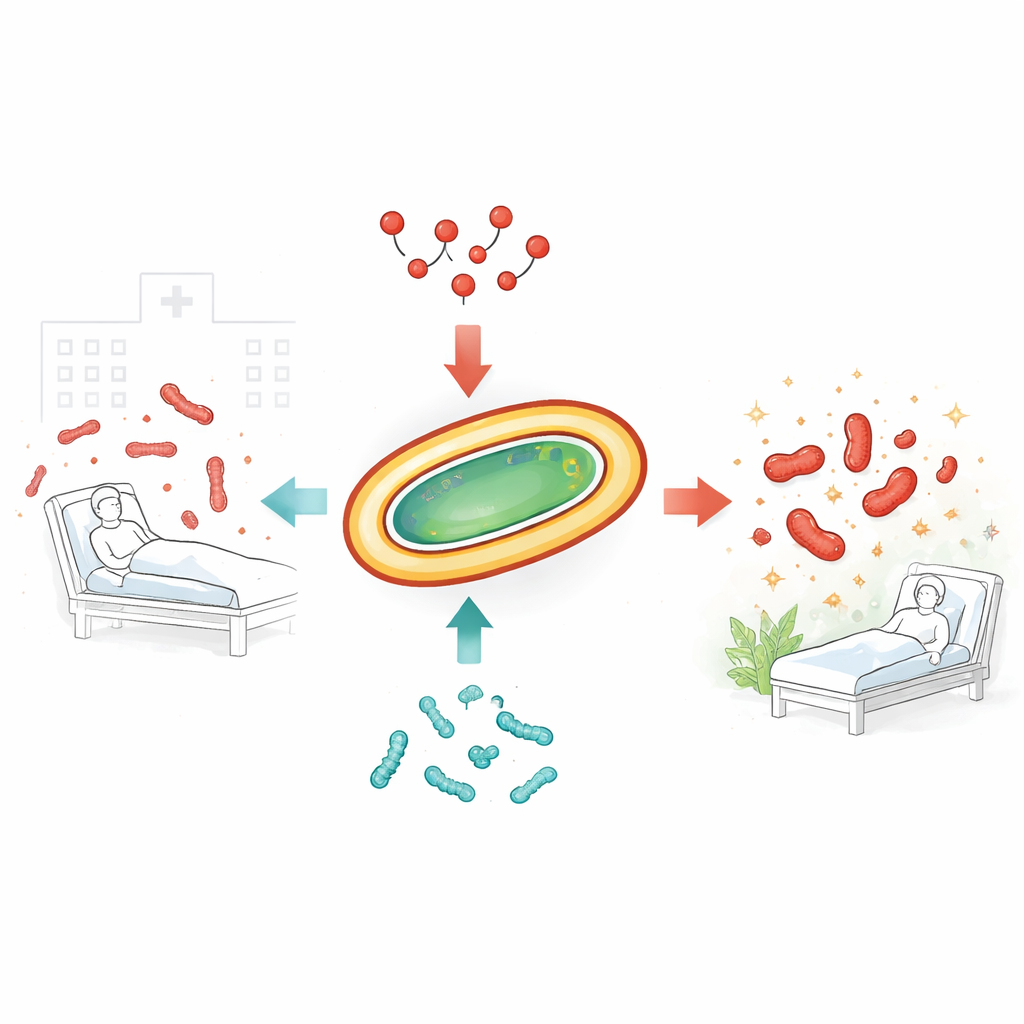
Los gérmenes resistentes que burlan a los antibióticos
Los investigadores se centraron en varios aislados clínicos recientes de A. baumannii, recogidos de pacientes reales y ya resistentes a muchos fármacos de uso común. El análisis genético mostró que estas cepas eran diversas, tanto en su ADN como en los tipos de genes de resistencia que portaban. Pruebas estándar confirmaron que la mayoría seguían siendo sensibles a la colistina, mientras que una cepa era altamente resistente. Cuando los científicos intentaron combinar colistina con otros antibióticos convencionales usados en hospitales, como tigeciclina o imipenem, las combinaciones produjeron en el mejor de los casos un efecto aditivo, no la verdadera sinergia que podría aumentar significativamente la eliminación bacteriana y frenar la resistencia.
Armas bacterianas naturales se unen a la lucha
Muchas bacterias fabrican sus propias pequeñas armas proteicas, llamadas bacteriocinas, para defenderse de competidores. El equipo cribó un panel de estas moléculas y encontró que varias producidas por bacterias Gram-positivas no patógenas podían inhibir A. baumannii, aunque solo a dosis altas. Seleccionaron dos péptidos pequeños y helicoidales —Lacticin Z y Enterocin L50— para un estudio más profundo. En modelos de membrana en tubo de ensayo, ambos se unieron con fuerza a mezclas de grasas que imitan la membrana interna de A. baumannii y pudieron perforar estos vesículas artificiales. Sin embargo, las bacterias intactas resultaron mucho menos afectadas, lo que sugiere que la capa externa de la bacteria actúa como un escudo que impide que los péptidos alcancen su blanco preferente.
La colistina abre la puerta, las bacteriocinas rematan el trabajo
La colistina actúa al unirse a un componente lipídico del recubrimiento externo de las bacterias Gram-negativas y al perturbar la estructura de sus membranas. En A. baumannii, los autores mostraron que la colistina no solo hace que la membrana externa sea permeable, sino que también altera el potencial eléctrico de la membrana interna y agota la reserva de ATP de la célula, su principal moneda energética. Por sí sola, el tratamiento con colistina a menudo no logró eliminar todas las células en un cultivo: algunas bacterias sobrevivieron y, con el tiempo, aparecieron mutantes con cambios en genes relacionados con la membrana que se volvieron altamente resistentes. Cuando los investigadores añadieron dosis bajas, por sí mismas inactivas, de Lacticin Z o Enterocin L50 junto con colistina, la supervivencia bacteriana cayó drásticamente. La combinación también previno o redujo en gran medida el rebrote que habitualmente señaliza la aparición de mutantes resistentes, incluso cuando se imitaban cepas que habían perdido parcialmente sus moléculas características de la capa externa.
Atacar la envoltura celular desde dos frentes
Para entender cómo funciona esta asociación, el equipo exploró diferentes formas de debilitar la superficie bacteriana. Sustancias químicas que bloquean la síntesis del lípido de la capa externa (lipid A) o que desestabilizan la membrana externa hicieron a A. baumannii más vulnerable a las bacteriocinas, lo que respalda la idea de que, una vez comprometido el escudo externo, los péptidos pueden alcanzar y dañar la membrana interna. Las bacteriocinas también potenciaron la actividad de un antibiótico que actúa sobre la pared celular externa, el imipenem, cuando ese fármaco ya había comenzado a perturbar la envoltura. De forma importante, combinar colistina con Lacticin Z o Enterocin L50 no solo mató más células sino que también redujo drásticamente la aparición de mutantes genéticamente estables y resistentes. Las células supervivientes tendieron a mostrar una tolerancia transitoria más que una resistencia permanente.
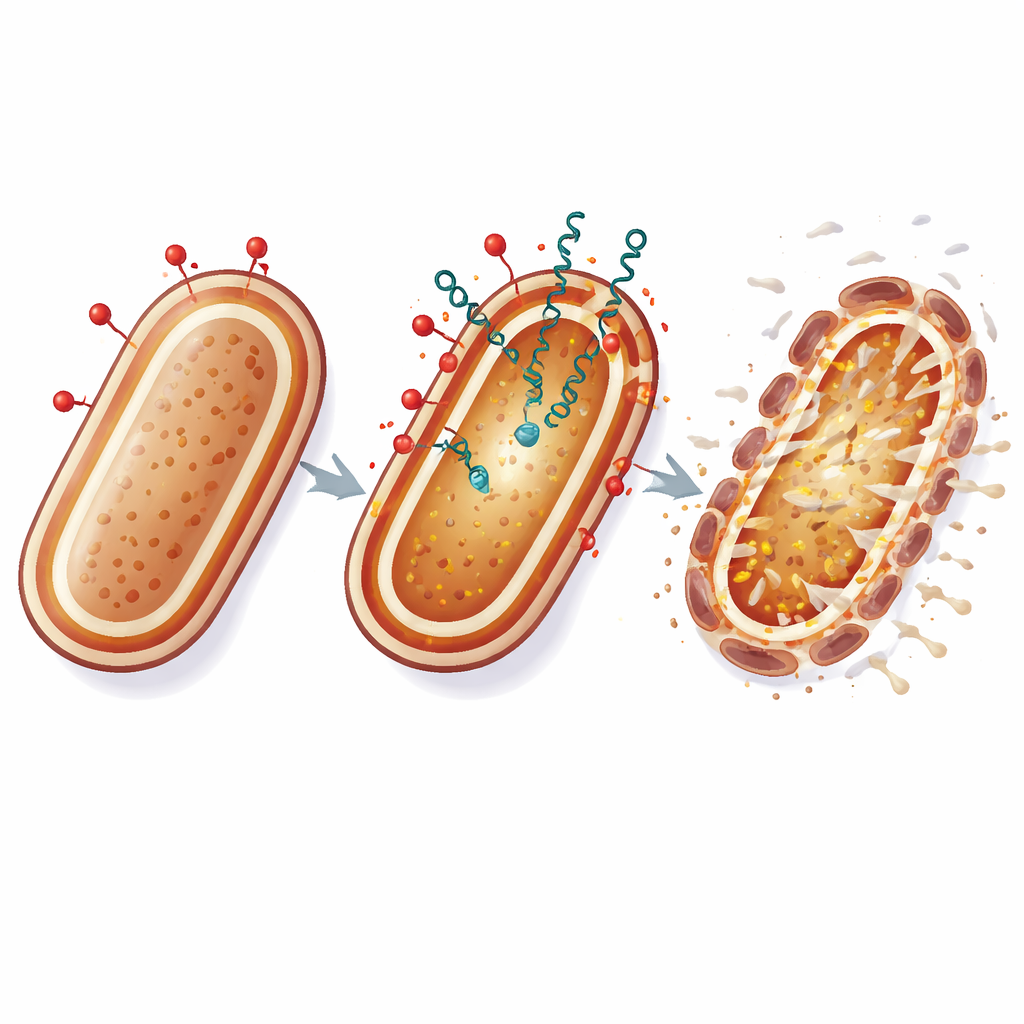
Qué podría significar esto para tratamientos futuros
En términos cotidianos, la colistina actúa como una palanca que abre la armadura externa de la bacteria, mientras que las bacteriocinas se deslizan por las grietas y atacan la membrana interna que sostiene la vida. Al golpear la envoltura celular en dos puntos vulnerables a la vez, esta estrategia dificulta mucho que A. baumannii se adapte mediante simples cambios genéticos. Aunque estos experimentos se realizaron en el laboratorio, los resultados sugieren que combinaciones cuidadosamente seleccionadas de antibióticos tradicionales con péptidos bacterianos naturales podrían prolongar la vida útil de los fármacos de último recurso y ofrecer nuevas opciones contra infecciones hospitalarias que de otro modo serían intratables.
Cita: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
Palabras clave: resistencia a antibióticos, Acinetobacter baumannii, colistina, bacteriocinas, terapia combinada