Clear Sky Science · ru
Комбинации колистина и бактериоцинов предотвращают отбор устойчивости к колистину у Acinetobacter baumannii
Почему это важно для инфекций в больницах
Инфекции, приобретённые в больницах, становясь устойчивыми к препаратам, всё труднее лечить. Одним из самых тревожных возбудителей является бактерия Acinetobacter baumannii, которая может противостоять почти всем доступным антибиотикам. Врачи нередко вынуждены прибегать к колистину — мощному препарату «последней инстанции». Но даже колистин начинает терять эффективность, поскольку бактерии эволюционируют и приобретают устойчивость. В этом исследовании изучали, может ли сочетание колистина с природными бактериальными пептидами — бактерицинами — одновременно более эффективно убивать эти упорные микробы и замедлять появление устойчивости.
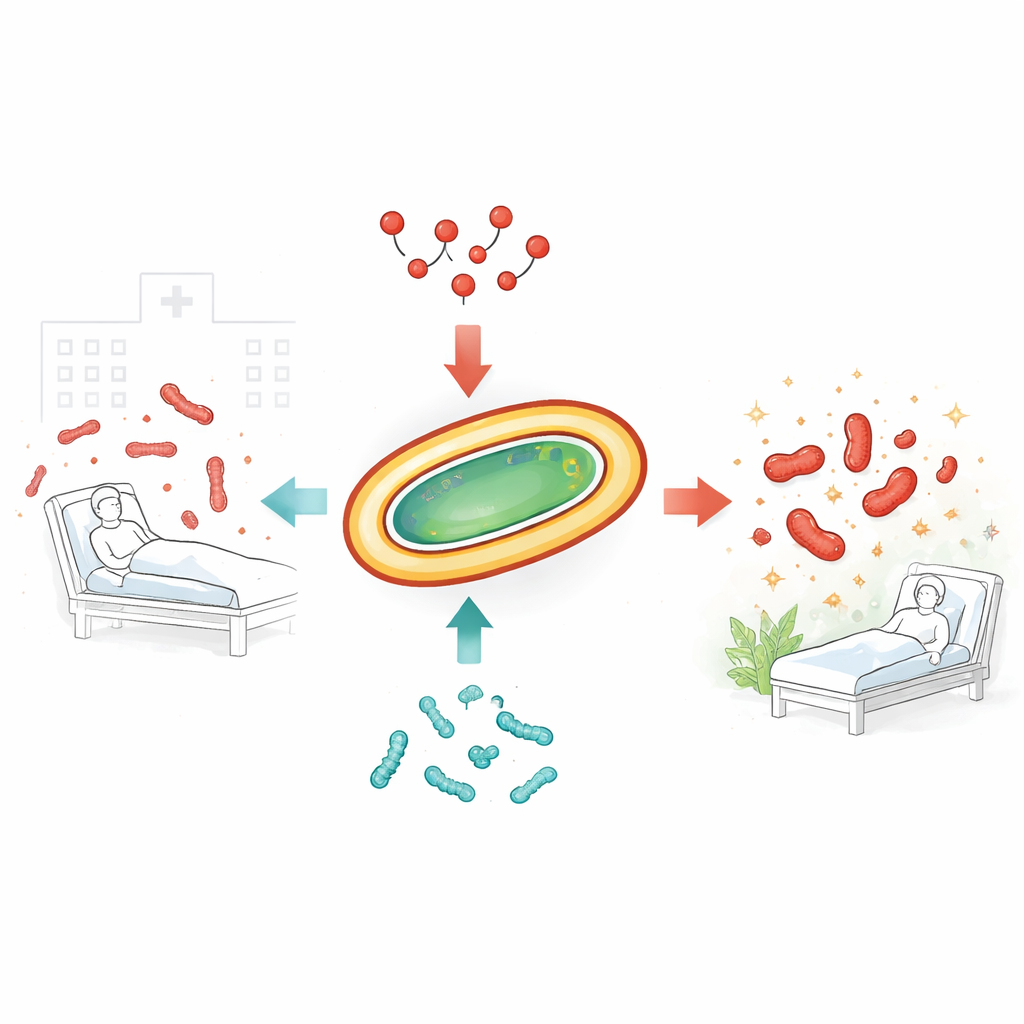
Упорные микробы, которые перехитривают антибиотики
Учёные сосредоточились на нескольких недавних клинических изолятах A. baumannii, выделенных от реальных пациентов и уже устойчивых ко многим часто используемым препаратам. Генетический анализ показал, что эти штаммы были разнообразны как по ДНК, так и по наборам генов устойчивости. Стандартные тесты подтвердили, что большинство всё ещё чувствительны к колистину, тогда как один штамм оказался высокоустойчивым. Когда исследователи пробовали сочетать колистин с другими обычными антибиотиками, применяемыми в больницах, такими как тигециклин или имипенем, эти пары давали в лучшем случае аддитивный эффект, но не истинную синергию, которая могла бы значительно усилить уничтожение и сдержать развитие устойчивости.
Природное бактериальное оружие вступает в бой
Многие бактерии вырабатывают собственные небольшие белковые «оружия», называемые бактерицинами, чтобы отгонять конкурентов. Команда проэкрановала панель таких молекул и обнаружила, что несколько бактериоцинов, продуцируемых безвредными грамположительными бактериями, могли ингибировать A. baumannii, хотя только в высоких дозах. Для более глубокой работы были выбраны два небольших спиральных пептида — Lacticin Z и Enterocin L50. В моделях мембран in vitro оба сильно связывались с смесями липидов, имитирующими внутреннюю мембрану A. baumannii, и могли проделывать в этих искусственных везикулах отверстия. Однако целые бактерии подвергались воздействию гораздо меньше, что указывает на то, что наружный поверхностный слой бактерии действует как щит, не давая пептидам добраться до их мишени.
Колистин открывает дверь, бактерицины завершают работу
Колистин действует, связываясь с липидным компонентом наружного покрытия грамотрицательных бактерий и нарушая структуру их мембран. В A. baumannii авторы показали, что колистин не только делает наружную мембрану проницаемой, но и нарушает электрический потенциал внутренней мембраны и истощает запас ATP, основную энергетическую валюту клетки. Сам по себе колистин часто не уничтожал все клетки в культуре: некоторые бактерии выживали, и со временем появлялись мутанты с изменениями в конкретных генах, связанных с мембраной, которые становились высокоустойчивыми. Когда исследователи добавляли низкие, иначе неактивные дозы Lacticin Z или Enterocin L50 вместе с колистином, выживаемость бактерий резко падала. Такая комбинация также предотвращала или значительно уменьшала регенерацию, обычно сигнализирующую о появлении устойчивых мутантов, даже при моделировании штаммов, частично потерявших типичные молекулы наружного слоя.
Атака по оболочке клетки с двух сторон
Чтобы понять, как работает это партнёрство, команда исследовала различные способы ослабления поверхностного слоя бактерии. Химические вещества, блокирующие синтез наружного липида (липид А) или дестабилизирующие наружную мембрану, делали A. baumannii более уязвимой к бактерицинам, что подтверждает идею о том, что при нарушении наружного щита пептиды могут добраться до внутренней мембраны и повредить её. Бактерицины также усиливали активность антибиотика, направленного на наружную клеточную стенку — имипенема, когда этот препарат уже начинал нарушать оболочку. Важно, что сочетание колистина с Lacticin Z или Enterocin L50 не только убивало больше клеток, но и резко уменьшало появление стабильных, генетически устойчивых мутантов. Выжившие клетки, как правило, были временно толерантными, а не постоянно устойчивыми.
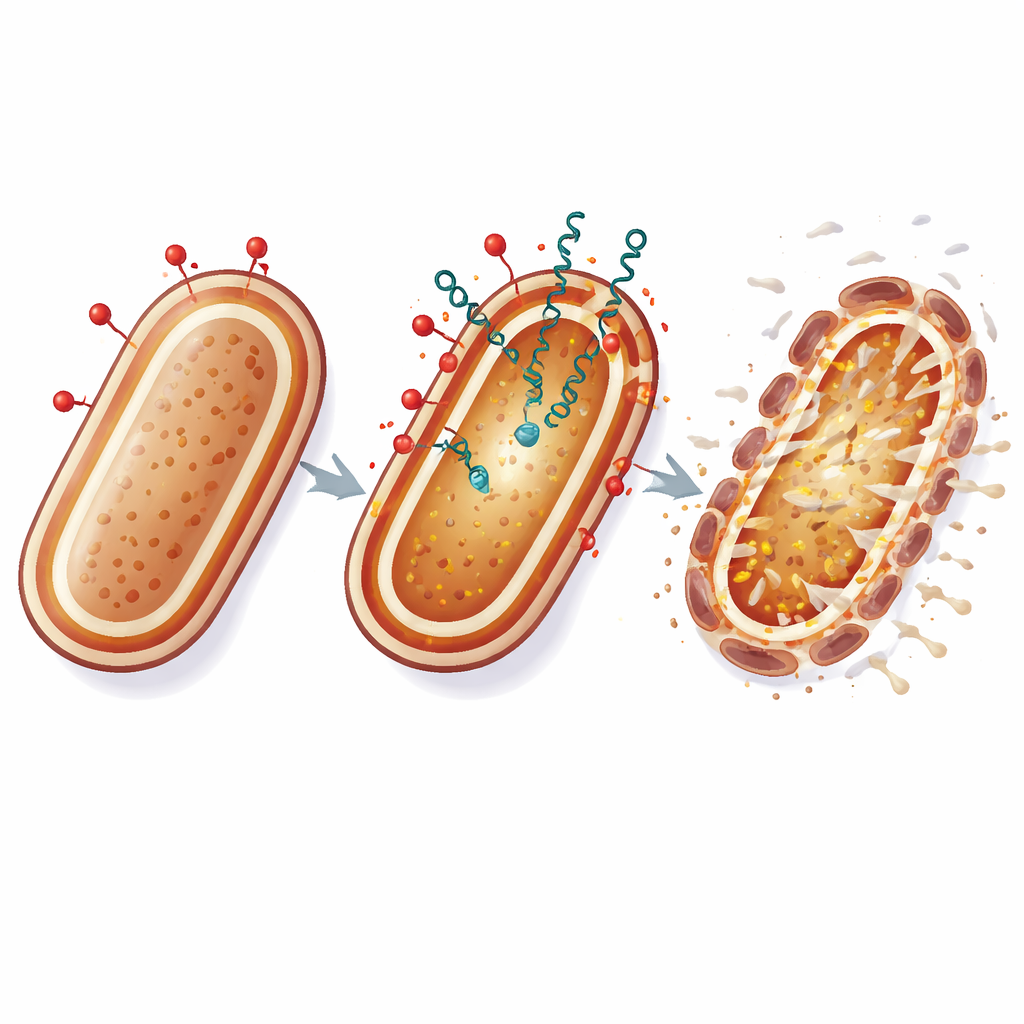
Что это может означать для будущих методов лечения
Проще говоря, колистин действует как монтировка, приподнимающая внешнюю броню бактерии, а бактерицины пробираются в образовавшиеся трещины и атакуют внутреннюю, жизненно важную мембрану. Нанесение удара по оболочке клетки в двух уязвимых точках одновременно делает адаптацию A. baumannii посредством простых генетических изменений значительно более трудной. Хотя эти эксперименты проводились в лаборатории, результаты указывают, что тщательно подобранные комбинации традиционных антибиотиков с природными бактериальными пептидами могут продлить срок полезного применения препаратов последней инстанции и предложить новые опции против иначе неизлечимых больничных инфекций.
Цитирование: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
Ключевые слова: антибиотикорезистентность, Acinetobacter baumannii, колистин, бактерицины, комбинационная терапия