Clear Sky Science · nl
Combinaties van colistine en bacteriocines voorkomen de selectie van colistine‑resistentie in Acinetobacter baumannii
Waarom dit belangrijk is voor ziekenhuisinfecties
In het ziekenhuis opgelopen, medicijnresistente infecties worden almaar moeilijker te behandelen. Een van de meest zorgwekkende daders is een bacterie genaamd Acinetobacter baumannii, die bijna alle beschikbare antibiotica kan weerstaan. Artsen moeten vaak terugvallen op colistine, een krachtig ‘‘laatste redmiddel’’-middel. Maar zelfs colistine begint zijn effect te verliezen nu de bacteriën resistentie ontwikkelen. Deze studie onderzoekt of het combineren van colistine met natuurlijke bacteriële peptiden, bacteriocines genoemd, deze hardnekkige microben effectiever kan doden en tegelijk de opkomst van resistentie kan vertragen.
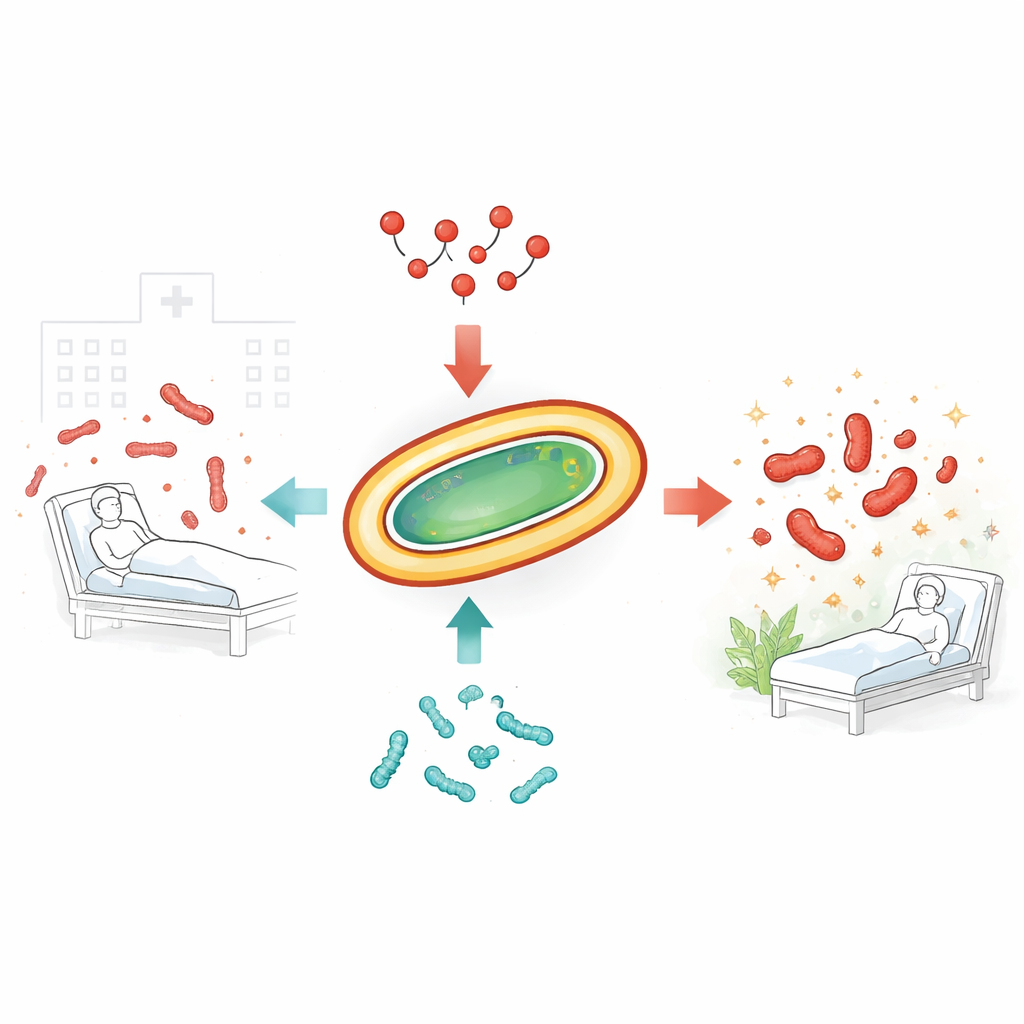
De taaie kiemen die antibiotica te slim af zijn
De onderzoekers richtten zich op meerdere recente klinische isolaten van A. baumannii, verzameld van echte patiënten en reeds resistent tegen veelgebruikte middelen. Genetische analyse toonde aan dat deze stammen divers waren, zowel in hun DNA als in de soorten resistentiegenen die ze droegen. Standaardtests bevestigden dat de meeste nog steeds gevoelig waren voor colistine, terwijl één stam sterk resistent bleek. Toen de wetenschappers probeerden colistine te combineren met andere conventionele antibiotica die vaak in ziekenhuizen worden gebruikt, zoals tigecycline of imipenem, leverden die combinaties hooguit een additief effect op, geen echte synergie die het doden flink zou verhogen en resistentie zou tegengaan.
Natuurlijke bacteriewapens sluiten zich bij de strijd aan
Veel bacteriën maken hun eigen kleine eiwitwapens, bacteriocines genoemd, om concurrenten te verdrijven. Het team screende een reeks van deze moleculen en vond dat verschillende, geproduceerd door onschuldige Gram‑positieve bacteriën, A. baumannii konden remmen, hoewel alleen bij hoge doses. Ze selecteerden twee kleine, helical peptiden—Lacticin Z en Enterocin L50—voor nader onderzoek. In reageerbuismodellen van membranen hechtten beide sterk aan mengsels van vetten die de binnenmembraan van A. baumannii nabootsen en konden gaten prikken in deze kunstmatige vesikels. Intacte bacteriën reageerden echter veel minder, wat suggereert dat de buitenste oppervlaktelaag van de bacterie als schild fungeert en voorkomt dat de peptiden hun favoriete doel bereiken.
Colistine opent de deur, bacteriocines maken de klus af
Colistine werkt door te binden aan een lipidecomponent in de buitenlaag van Gram‑negatieve bacteriën en hiermee de structuur van hun membranen te verstoren. Bij A. baumannii toonden de auteurs aan dat colistine niet alleen de buitenmembraan lekkend maakt maar ook de elektrische lading van de binnenmembraan verstoort en de ATP‑voorraad van de cel, haar belangrijkste energiebron, uitput. Alleen was colistinebehandeling vaak niet in staat alle cellen in een cultuur uit te roeien: sommige bacteriën overleefden en na verloop van tijd verschenen mutanten met veranderingen in specifieke membraan‑gerelateerde genen die zeer resistent werden. Wanneer de onderzoekers lage, op zichzelf inactieve doses Lacticin Z of Enterocin L50 toevoegden samen met colistine, daalde de bacteriële overleving dramatisch. De combinatie verhinderde of verminderde ook sterk de hergroei die normaal het opkomen van resistente mutanten aangeeft, zelfs wanneer de stammen waren nagebootst die gedeeltelijk hun gebruikelijke buitenlaagmoleculen hadden verloren.
De celomhulling van twee kanten aanvallen
Om te begrijpen hoe deze samenwerking werkt, onderzocht het team verschillende manieren om het bacteriële oppervlak te verzwakken. Chemische stoffen die de synthese van de buitenlaaglipide (lipid A) blokkeren of die de buitenmembraan destabiliseren, maakten A. baumannii kwetsbaarder voor de bacteriocines, wat de gedachte ondersteunt dat zodra het buitenste schild is aangetast, de peptiden het binnenmembraan kunnen bereiken en beschadigen. De bacteriocines versterkten ook de werkzaamheid van een antibioticum dat het buitenste celwandgebied aanvalt, imipenem, wanneer dat middel al begon het omhulsel te verstoren. Belangrijk is dat de combinatie van colistine met Lacticin Z of Enterocin L50 niet alleen meer cellen doodde maar ook scherp vermindering gaf van het verschijnen van stabiele, genetisch resistente mutanten. De overlevende cellen bleken eerder tijdelijk tolerant dan permanent resistent.
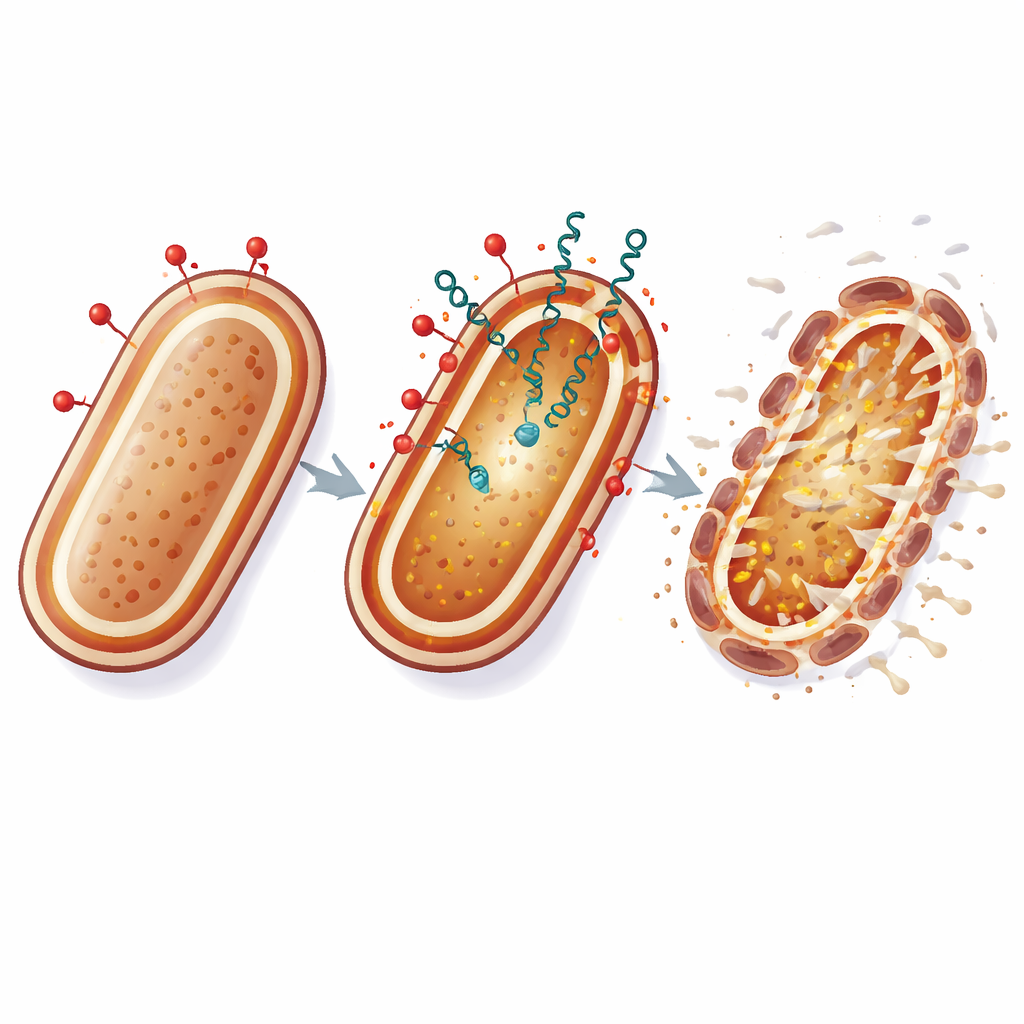
Wat dit zou kunnen betekenen voor toekomstige behandelingen
In gewone bewoordingen werkt colistine als een koevoet die het buitenste pantser van de bacterie opentrekt, terwijl bacteriocines door de scheuren glippen en het binnenmembraan, dat het leven ondersteunt, aanvallen. Door de celomhulling op twee kwetsbare punten tegelijk te treffen, wordt het voor A. baumannii veel moeilijker te wennen via eenvoudige genetische aanpassingen. Hoewel deze experimenten in het laboratorium zijn uitgevoerd, suggereren de resultaten dat zorgvuldig gekozen combinaties van traditionele antibiotica met natuurlijke bacteriële peptiden de bruikbare levensduur van laatste‑redmiddelmiddelen kunnen verlengen en nieuwe opties kunnen bieden tegen anders onbehandelbare ziekenhuisinfecties.
Bronvermelding: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
Trefwoorden: antibioticaresistentie, Acinetobacter baumannii, colistine, bacteriocines, combinatietherapie