Clear Sky Science · ar
مجموعات من الكولستين والباكتريوسينات تمنع اختيار مقاومة الكولستين في Acinetobacter baumannii
لماذا هذا مهم لعدوى المستشفيات
تصبح العدوى المقاومة للأدوية المكتسبة في المستشفيات أكثر صعوبة في العلاج. أحد المسببات الأكثر إثارة للقلق هو بكتيريا تسمى Acinetobacter baumannii، التي تستطيع مقاومة معظم المضادات الحيوية المتاحة تقريباً. يضطر الأطباء غالباً للاعتماد على الكولستين، دواء قوي يعتبر «ملاذاً أخيراً». لكن حتى الكولستين بدأ يفقد فعاليته مع تطور البكتيريا لمقاومة ضده. تستقصي هذه الدراسة ما إذا كان الجمع بين الكولستين وببتيدات بكتيرية طبيعية تسمى باكتريوسينات يمكن أن يقتل هذه الجراثيم العنيدة بشكل أكثر فعالية ويبطئ في الوقت نفسه ظهور المقاومة.
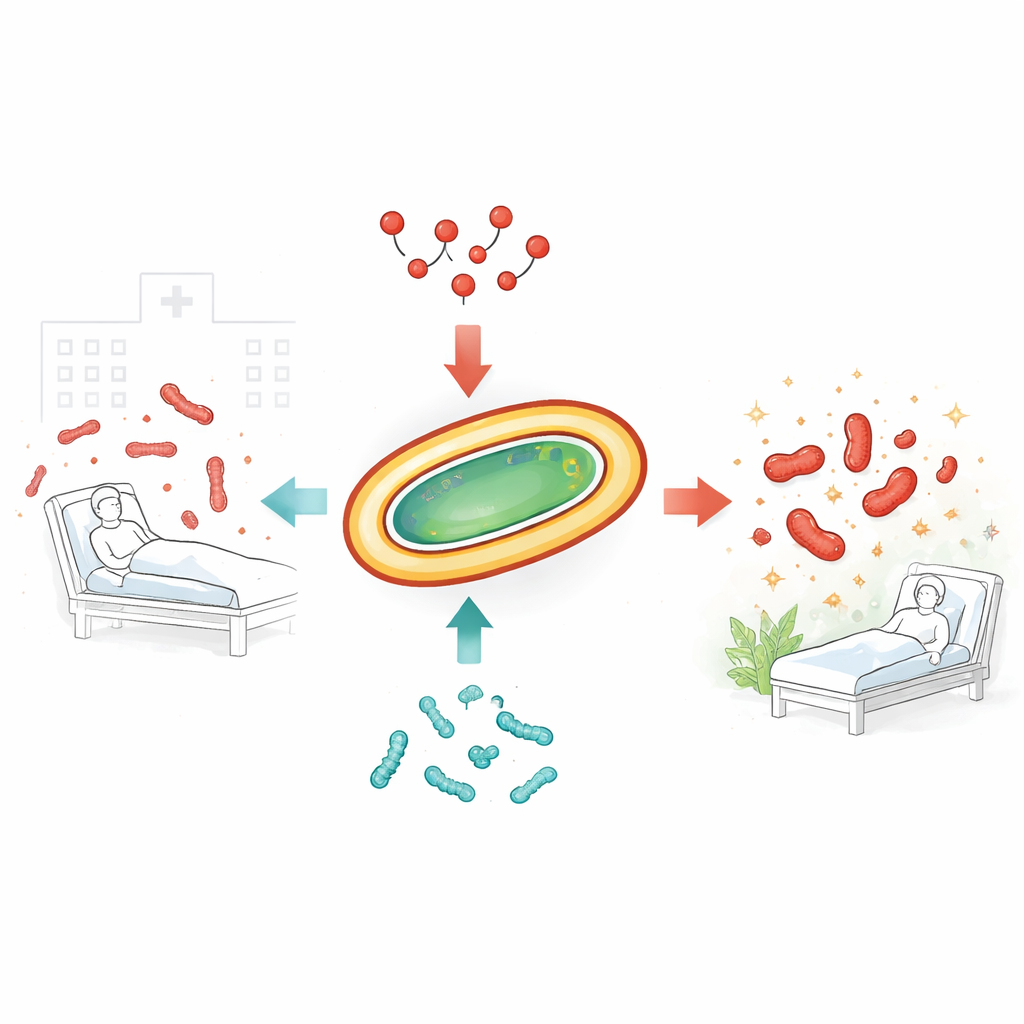
الجراثيم العنيدة التي تتغلب على المضادات الحيوية
ركز الباحثون على عدة عزلات سريرية حديثة من A. baumannii، جمعت من مرضى حقيقيين وكانت مقاومة بالفعل للعديد من الأدوية الشائعة الاستخدام. أظهر التحليل الجيني أن هذه السلالات كانت متباينة، سواء في حمضها النووي أو في أنواع جينات المقاومة التي تحملها. أكدت الاختبارات المعيارية أن معظمها ما زال حساساً للكولستين، بينما كانت إحدى السلالات مقاومة بشدة. عندما جرب العلماء الجمع بين الكولستين ومضادات حيوية تقليدية أخرى مستخدمة في المستشفيات، مثل التيجيسيكلين أو الإيميبينيم، أظهرت التركيبة في أحسن الأحوال تأثيراً إضافياً، وليس تآزرًا حقيقياً يمكنه تعزيز القتل بشكل ملحوظ وكبح المقاومة.
انضمام أسلحة بكتيرية طبيعية إلى القتال
تنتج العديد من البكتيريا أسلحتها البروتينية الصغيرة الخاصة، المسماة باكتريوسينات، لصد المنافسين. فحص الفريق لوحة من هذه الجزيئات ووجد أن عدة منها، المنتجة بواسطة بكتيريا إيجابية الغرام غير ضارة، يمكنها تثبيط A. baumannii، وإن كان ذلك فقط بجرعات عالية. اختاروا ببتيدين صغيرين حلزونيين—Lacticin Z وEnterocin L50—لدراسة أعمق. في نماذج غشائية أنبوبية، ارتبط كلاهما بقوة بخليط من الدهون يحاكي الغشاء الداخلي لـ A. baumannii وكان قادرًا على فتح ثقوب في هذه الحويصلات الاصطناعية. مع ذلك، كانت البكتيريا السليمة أقل تأثراً بكثير، مما يشير إلى أن طبقة السطح الخارجية للبكتيريا تعمل كدرع يمنع الببتيدات من الوصول إلى الهدف المفضل لها.
الكولستين يفتح الباب والباكتريوسينات تُكمل المهمة
يعمل الكولستين عن طريق الارتباط بمركب دهني في الغلاف الخارجي للبكتيريا سالبة الغرام وتعطيل بنية أغشيتها. في A. baumannii، أظهر المؤلفون أن الكولستين لا يجعل الغشاء الخارجي مسربًا فحسب، بل يخل أيضاً بالشحنة الكهربائية للغشاء الداخلي ويستنزف مخزون الخلية من ATP، عملتها الرئيسية للطاقة. بمفرده، غالباً ما يفشل علاج الكولستين في القضاء على كل الخلايا في مزرعة: بقا من البكتيريا تنجو ومع مرور الوقت تظهر طفرات في جينات مرتبطة بالغشاء وتصبح شديدة المقاومة. عندما أضاف الباحثون جرعات منخفضة، كانت خاملة بحد ذاتها، من Lacticin Z أو Enterocin L50 مع الكولستين، انخفضت بقاء البكتيريا بشكل كبير. كما منعت التركيبة أو قللت بشدة من إعادة النمو التي عادة ما تشير إلى ظهور طفرات مقاومة، حتى عندما محاكوا سلالات فقدت جزئياً جزيئات طبقتها الخارجية النموذجية.
استهداف غلاف الخلية من جهتين
لفهم كيف يعمل هذا التعاون، فحص الفريق طرقًا مختلفة لإضعاف سطح البكتيريا. المواد الكيميائية التي تمنع تخليق الدهن الخارجي (الليبد A) أو التي تزعزع استقرار الغشاء الخارجي جعلت A. baumannii أكثر عرضة للباكتريوسينات، مما يدعم الفكرة بأن مؤقتة حين يضعف الدرع الخارجي يمكن للببتيدات الوصول إلى الغشاء الداخلي وإلحاق الضرر به. عززت الباكتريوسينات أيضاً فعالية مضاد حيوي يستهدف جدار الخلية الخارجي، الإيميبينيم، عندما كان ذلك الدواء قد بدأ بالفعل في إزعاج الغلاف. والأهم من ذلك، أن الجمع بين الكولستين وLacticin Z أو Enterocin L50 لم يقضِ على خلايا أكثر فحسب، بل قلل أيضاً بشكل حاد من ظهور طفرات مستقرة ذات مقاومة جينية. الخلايا الناجية كانت تميل لأن تكون متسامحة بشكل عابر بدلاً من مقاومة دائمة.
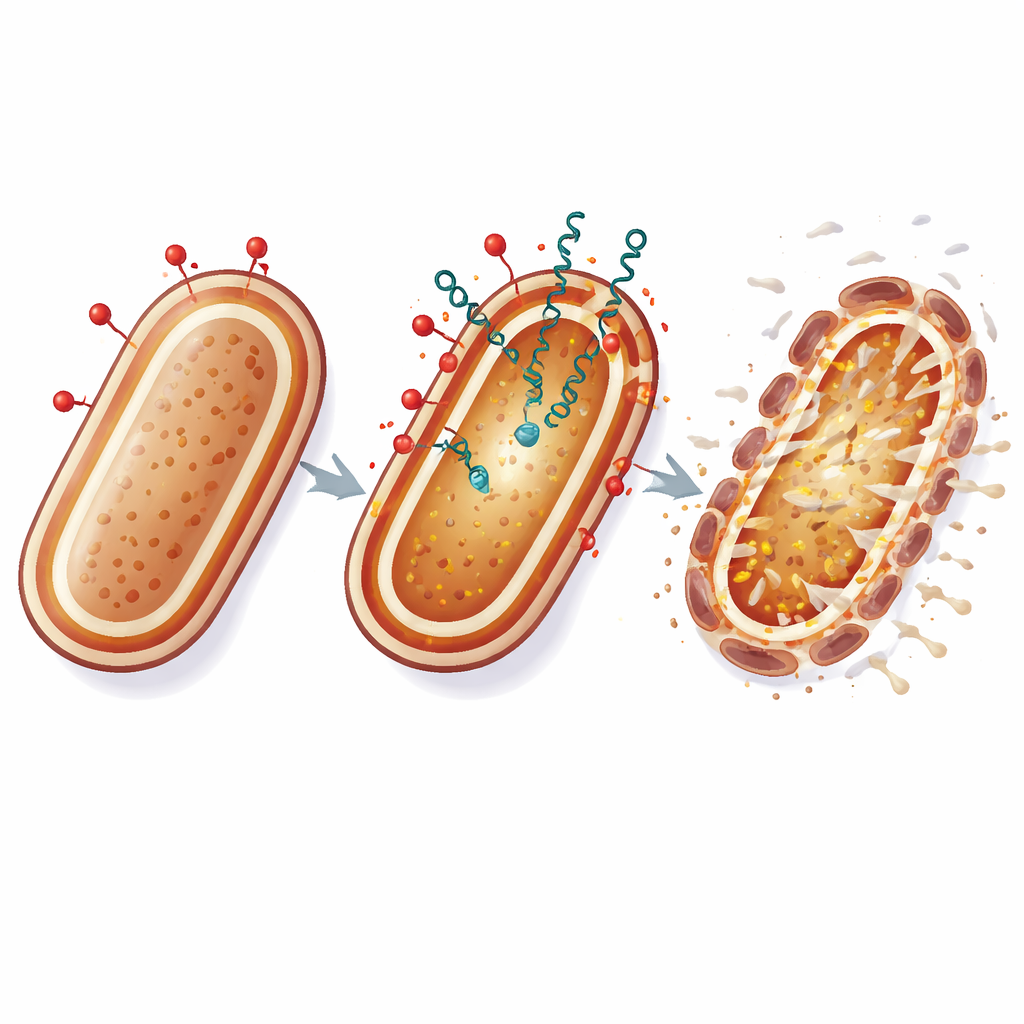
ماذا قد يعني هذا للعلاجات المستقبلية
بعبارات بسيطة، يعمل الكولستين بمثابة رافعة تفتح درع البكتيريا الخارجي، بينما تتسلل الباكتريوسينات من خلال الشقوق وتهاجم غشاء دعم الحياة الداخلي. من خلال ضرب غلاف الخلية من نقطتين ضعيفتين في آن واحد، يجعل هذا النهج من الصعب جداً على A. baumannii التكيّف عبر تغييرات جينية بسيطة. رغم أن هذه التجارب أُجريت في المختبر، تشير النتائج إلى أن مجموعات مختارة بعناية من المضادات الحيوية التقليدية مع الببتيدات البكتيرية الطبيعية قد تطيل العمر الفعّال للأدوية الملاذ الأخير وتوفر خيارات جديدة ضد عدوى المستشفيات التي قد تكون غير قابلة للعلاج بخلاف ذلك.
الاستشهاد: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
الكلمات المفتاحية: مقاومة المضادات الحيوية, Acinetobacter baumannii, كولستين, باكتريوسينات, العلاج التراكبي