Clear Sky Science · fr
Combinaisons de colistine et de bactériocines empêchant la sélection de résistances à la colistine chez Acinetobacter baumannii
Pourquoi c’est important pour les infections nosocomiales
Les infections résistantes aux médicaments contractées à l’hôpital deviennent de plus en plus difficiles à traiter. L’un des coupables les plus inquiétants est une bactérie appelée Acinetobacter baumannii, capable de résister à presque tous les antibiotiques disponibles. Les médecins doivent souvent recourir à la colistine, un antibiotique puissant considéré comme un « dernier recours ». Mais même la colistine commence à perdre de son efficacité à mesure que les bactéries développent des résistances. Cette étude examine si associer la colistine à des peptides bactériens naturels, appelés bactériocines, peut à la fois tuer ces microbes tenaces plus efficacement et ralentir l’apparition de résistances.
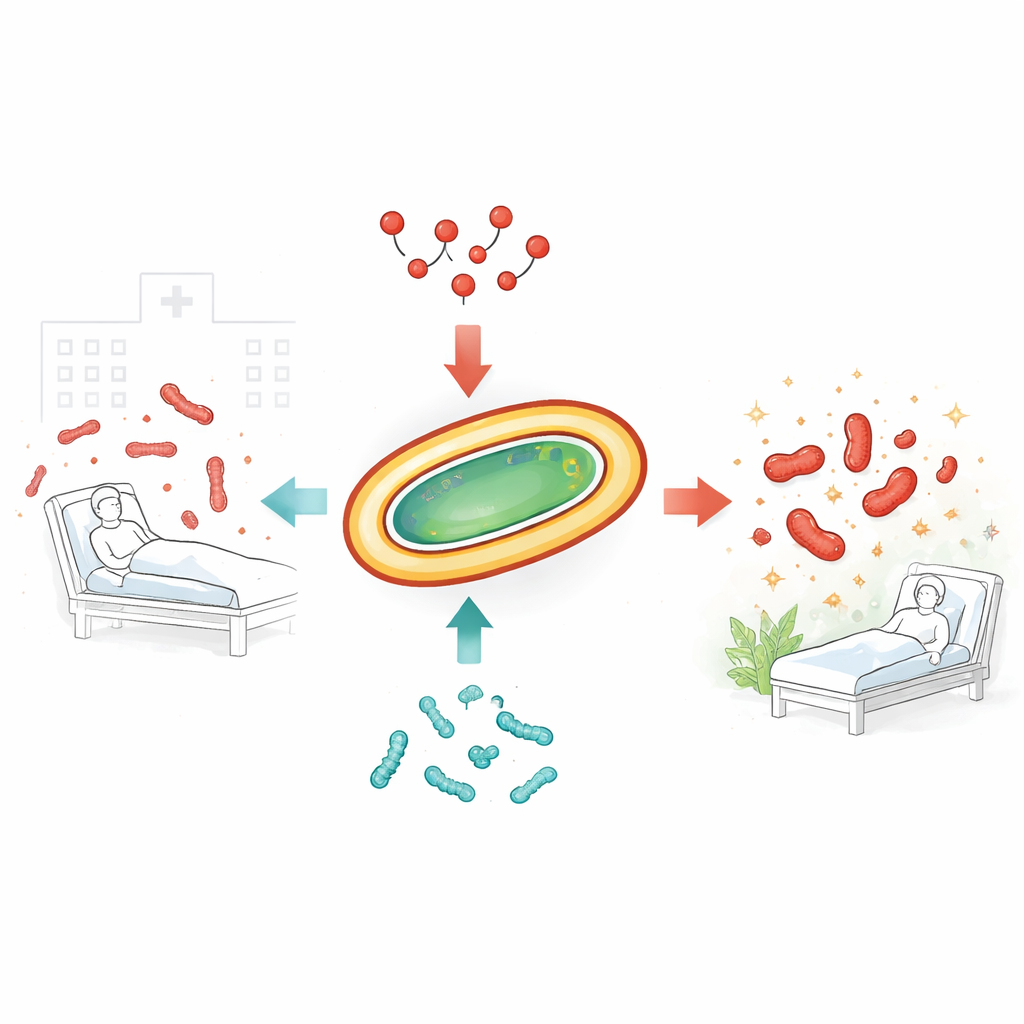
Les germes coriaces qui prennent de l’avance sur les antibiotiques
Les chercheurs se sont concentrés sur plusieurs isolats cliniques récents d’A. baumannii, prélevés chez de vrais patients et déjà résistants à de nombreux médicaments couramment utilisés. L’analyse génétique a montré que ces souches étaient diverses, tant au niveau de leur ADN que des types de gènes de résistance qu’elles portaient. Des tests standards ont confirmé que la plupart restaient encore sensibles à la colistine, tandis qu’une souche était fortement résistante. Lorsque les scientifiques ont essayé d’associer la colistine à d’autres antibiotiques classiques souvent utilisés en milieu hospitalier, comme la tigécycline ou l’imipénem, ces combinaisons ont au mieux produit un effet additif, et non une vraie synergie susceptible d’augmenter fortement l’élimination bactérienne et de freiner la résistance.
Des armes bactériennes naturelles entrent en scène
Be nombreuses bactéries produisent leurs propres petites armes protéiques, appelées bactériocines, pour éliminer les concurrents. L’équipe a dépisté un panel de ces molécules et a constaté que plusieurs produites par des bactéries Gram-positives non pathogènes pouvaient inhiber A. baumannii, bien que seulement à des doses élevées. Ils ont sélectionné deux petits peptides hélicoïdaux — la Lacticine Z et l’Enterocine L50 — pour une étude approfondie. Dans des modèles membranaires en éprouvette, les deux se lièrent fortement à des mélanges lipidiques imitant la membrane interne d’A. baumannii et purent percer des vésicules artificielles. Cependant, les bactéries intactes furent bien moins affectées, suggérant que la couche externe de la bactérie fait office de bouclier, empêchant les peptides d’atteindre leur cible privilégiée.
La colistine ouvre la porte, les bactériocines finissent le travail
La colistine agit en se liant à un composant lipidique de l’enveloppe externe des bactéries Gram-négatives et en perturbant la structure de leurs membranes. Chez A. baumannii, les auteurs ont montré que la colistine rend non seulement la membrane externe perméable, mais perturbe aussi la charge électrique de la membrane interne et vide les réserves d’ATP de la cellule, sa principale monnaie énergétique. Traité seul, la colistine n’éliminait souvent pas toutes les cellules d’une culture : certaines survivaient et, avec le temps, des mutants présentant des modifications de gènes liés à la membrane apparaissaient et devenaient fortement résistants. Lorsque les chercheurs ajoutèrent de faibles doses — autrement inactives — de Lacticine Z ou d’Enterocine L50 en combinaison avec la colistine, la survie bactérienne chuta de façon spectaculaire. La combinaison empêcha ou réduisit fortement la repousse qui signale habituellement l’émergence de mutants résistants, même lorsque les souches étudiées imitaient des variants ayant partiellement perdu leurs molécules habituelles de la couche externe.
Viser l’enveloppe cellulaire sur deux fronts
Pour comprendre comment fonctionne ce partenariat, l’équipe a étudié différentes façons d’affaiblir la surface bactérienne. Des produits chimiques bloquant la synthèse du lipide de la couche externe (lipide A) ou déstabilisant la membrane externe rendaient A. baumannii plus vulnérable aux bactériocines, soutenant l’idée que, une fois le bouclier externe compromis, les peptides peuvent atteindre et endommager la membrane interne. Les bactériocines potentialisaient aussi l’activité d’un antibiotique ciblant la paroi externe, l’imipénem, lorsque ce dernier avait déjà commencé à perturber l’enveloppe. Fait important, combiner la colistine avec la Lacticine Z ou l’Enterocine L50 non seulement tua davantage de cellules, mais réduisit aussi fortement l’apparition de mutants stables et génétiquement résistants. Les cellules survivantes avaient tendance à présenter une tolérance transitoire plutôt qu’une résistance permanente.
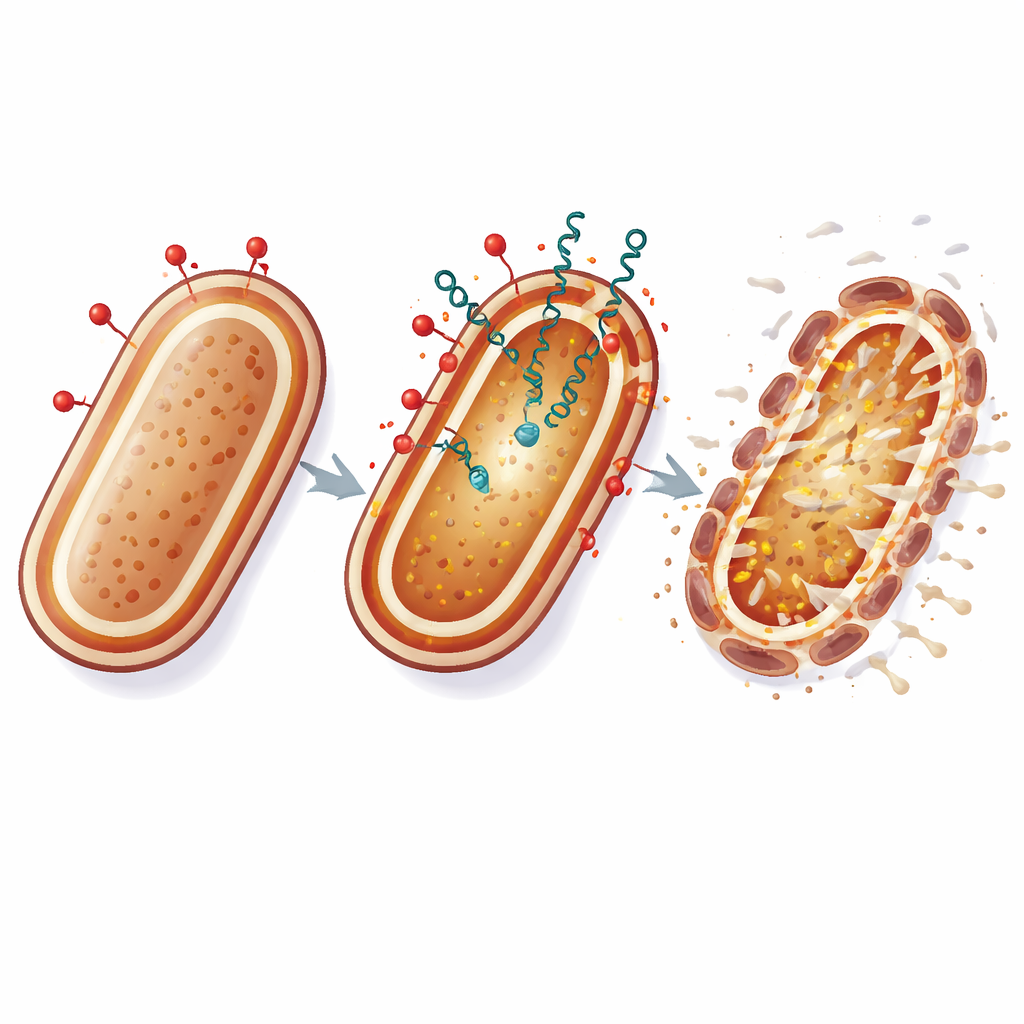
Ce que cela pourrait signifier pour les traitements futurs
En termes concrets, la colistine agit comme un pied-de-biche qui entrouvre l’armure externe de la bactérie, tandis que les bactériocines se glissent par les fissures et attaquent la membrane interne, essentielle à la vie cellulaire. En frappant l’enveloppe cellulaire à deux points vulnérables simultanément, cette stratégie rend beaucoup plus difficile pour A. baumannii de s’adapter par de simples modifications génétiques. Bien que ces expériences aient été réalisées en laboratoire, les résultats suggèrent que des combinaisons soigneusement choisies d’antibiotiques traditionnels et de peptides bactériens naturels pourraient prolonger l’efficacité des médicaments de dernier recours et offrir de nouvelles options contre des infections nosocomiales autrement intraitables.
Citation: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
Mots-clés: résistance aux antibiotiques, Acinetobacter baumannii, colistine, bactériocines, thérapie combinée