Clear Sky Science · he
שילובים של קוליסטין ובקטריוצינים מונעים את המצרוף של עמידות לקוליסטין ב‑Acinetobacter baumannii
מדוע זה חשוב לזיהומי בתי חולים
זיהומים עמידים לתרופות הנרכשים בבתי חולים הופכים צפופים יותר וקשים יותר לטיפול. אחד הגורמים המדאיגים ביותר הוא חיידק בשם Acinetobacter baumannii, שיכול להתגבר על כמעט כל האנטיביוטיקות הזמינות. רופאים נאלצים לעתים קרובות להישען על קוליסטין, תרופה חזקה שהיא לעתים קרובות "במילוי אחרון". אך גם קוליסטין מתחיל להיכשל ככל שהחיידקים מתפתחים לעמידות. המחקר הזה בוחן האם שילוב קוליסטין עם פפטידים חיידקיים טבעיים הנקראים בקטריוצינים יכול להרוג את המיקרובים העיקשים הללו ביעילות רבה יותר ולעכב את התפתחות העמידות.
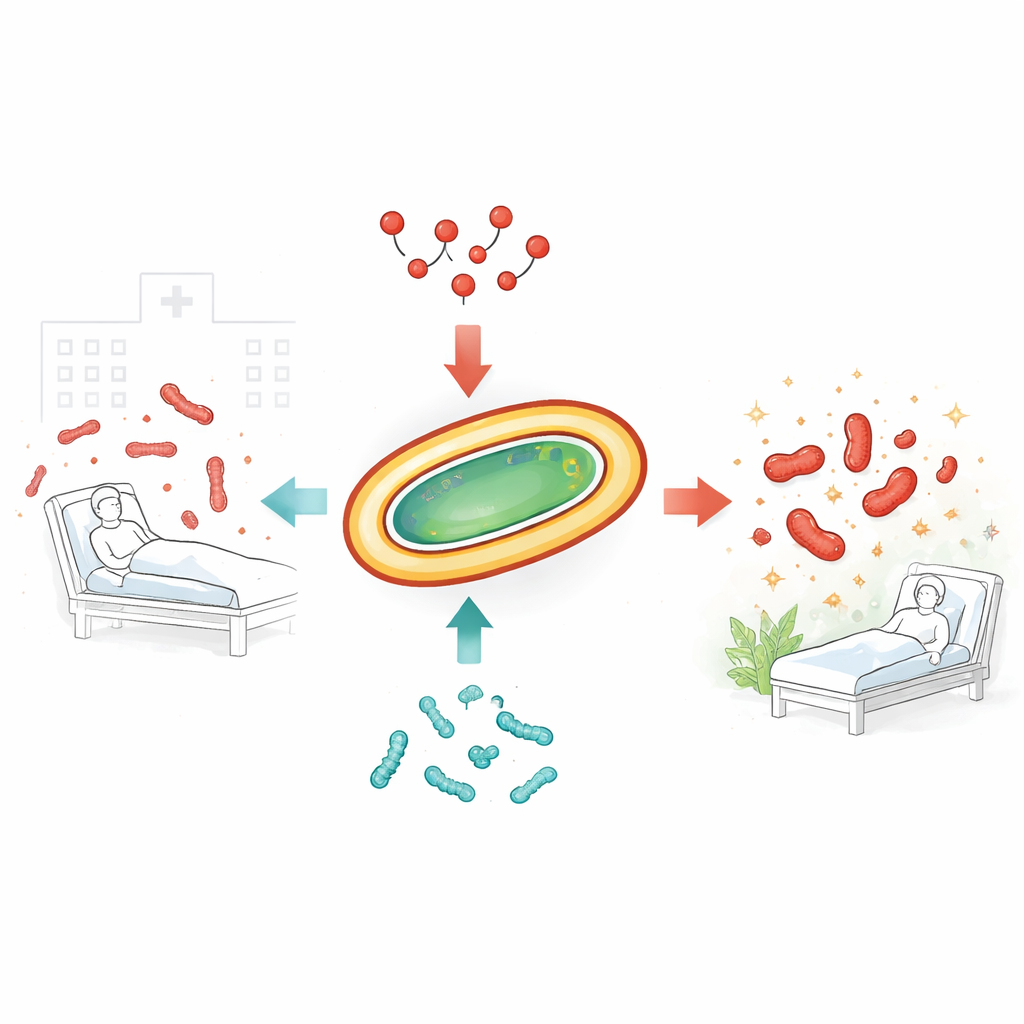
החיידקים הקשים שמעקפים אנטיביוטיקות
החוקרים התמקדו בכמה מבודדים קליניים של A. baumannii שנבדפו לאחרונה, שנלקחו מחולים אמיתיים וכבר עמידים למגוון תרופות נפוצות. ניתוח גנטי הראה שהזנים האלה מגוונים, הן בדנ"א והן בסוגי הגנים שמקנים עמידות. בדיקות סטנדרטיות אישרו שלרוב הזנים עדיין יש רגישות יחסית לקוליסטין, בעוד שזן אחד היה עמיד ברמה גבוהה. כשניסו החוקרים לשלב קוליסטין עם אנטיביוטיקות קונבנציונליות נוספות שנמצאות בשימוש בבתי חולים, כגון טיגציקלין או אימיפנם, השילובים הניבו לכל היותר אפקט מצטבר, ולא סינרגיה אמיתית שיכולה להגביר באופן משמעותי את ההשמדה ולעצור את העמידות.
נשקים טבעיים של חיידקים מצטרפים לקרב
חיידקים רבים מייצרים נשקי חלבון זעירים משלהם, הנקראים בקטריוצינים, כדי להדוף מתחרים. הצוות סרק לוח מקריונים של מולקולות אלה וגילה שכמה מתוכן המיוצרות על‑ידי חיידקי גרם‑חיוביים ידידותיים הצליחו לעכב את A. baumannii, אם כי רק במינונים גבוהים. בחרו שני פפטידים קטנים, בעלי מבנה הליקאלי — Lacticin Z ו‑Enterocin L50 — ללימוד מעמיק יותר. במודלים ממברנאליים בצינורות ניסוי, שניהם התחברו בעוצמה לתערובות שומניות המדמות את הממברנה הפנימית של A. baumannii ויכלו ליצור חורים בכיסיות המלאכותיות הללו. עם זאת, חיידקים שלמים הושפעו פחות באופן משמעותי, מה שמרמז ששכבת החוצץ החיצונית של החיידק פועלת כמגן ומונעת מהפפטידים להגיע למטרה המועדפת שלהם.
קוליסטין פותח את הדלת, בקטריוצינים משלימים את העבודה
קוליסטין פועל על ידי קשירה לרכיב שומני בציפוי החיצוני של חיידקי גרם‑שליליים והפרעה במבנה הממברנות שלהם. ב‑A. baumannii, המחברים הראו שקוליסטין לא רק עושה את הממברנה החיצונית דליפה אלא גם מופר את המטען החשמלי של הממברנה הפנימית ומרוקן את מאגרי ה‑ATP של התא, מטבע האנרגיה העיקרי שלו. לבדו, טיפול בקוליסטין לרוב לא השמיד את כל התאים בתרבית: חלק מהחיידקים שרדו ובמשך הזמן הופיעו מוטנטים עם שינויים בגנים קשורים לממברנה שהפכו לעמידים מאוד. כאשר החוקרים הוסיפו מינונים נמוכים, שבמצב אחר לא היו פעילים, של Lacticin Z או Enterocin L50 יחד עם קוליסטין, ההישרדות החיידקית צנחה באופן דרמטי. השילוב גם מנע או קיצר משמעותית את הצמיחה החוזרת שאופיינית להופעת מוטנטים עמידים, אפילו כאשר הם חיקו זנים שאיבדו באופן חלקי את המולקולות הטיפוסיות של השכבה החיצונית שלהם.
מיקוד מעטפת התא משני כיוונים
כדי להבין איך השותפות הזו פועלת, הצוות בחן דרכים שונות להחליש את פני השטח של החיידק. כימיקלים שחוסמים את הסינתזה של הליפיד החיצוני (ליפיד A) או שמייצבים את הממברנה החיצונית עשו את A. baumannii פגיע יותר לבקטריוצינים, ותמכו ברעיון שברגע שהמגן החיצוני נפגע, הפפטידים יכולים להגיע ולפגוע בממברנה הפנימית. הבקטריוצינים גם הגבירו את פעילותה של אנטיביוטיקה הפוגעת בדופן החיצונית של התא, אימיפנם, כאשר תרופה זו כבר החלה להפריע למעטפת. חשוב לציין, שילוב קוליסטין עם Lacticin Z או Enterocin L50 לא רק הרג יותר תאים אלא גם הקטין באופן חמור את הופעתם של מוטנטים גנטיים עמידים וקבועים. התאים ששרדו נטו להיות בעלי סבלנות חולפת יותר מאשר בעלי עמידות קבועה.
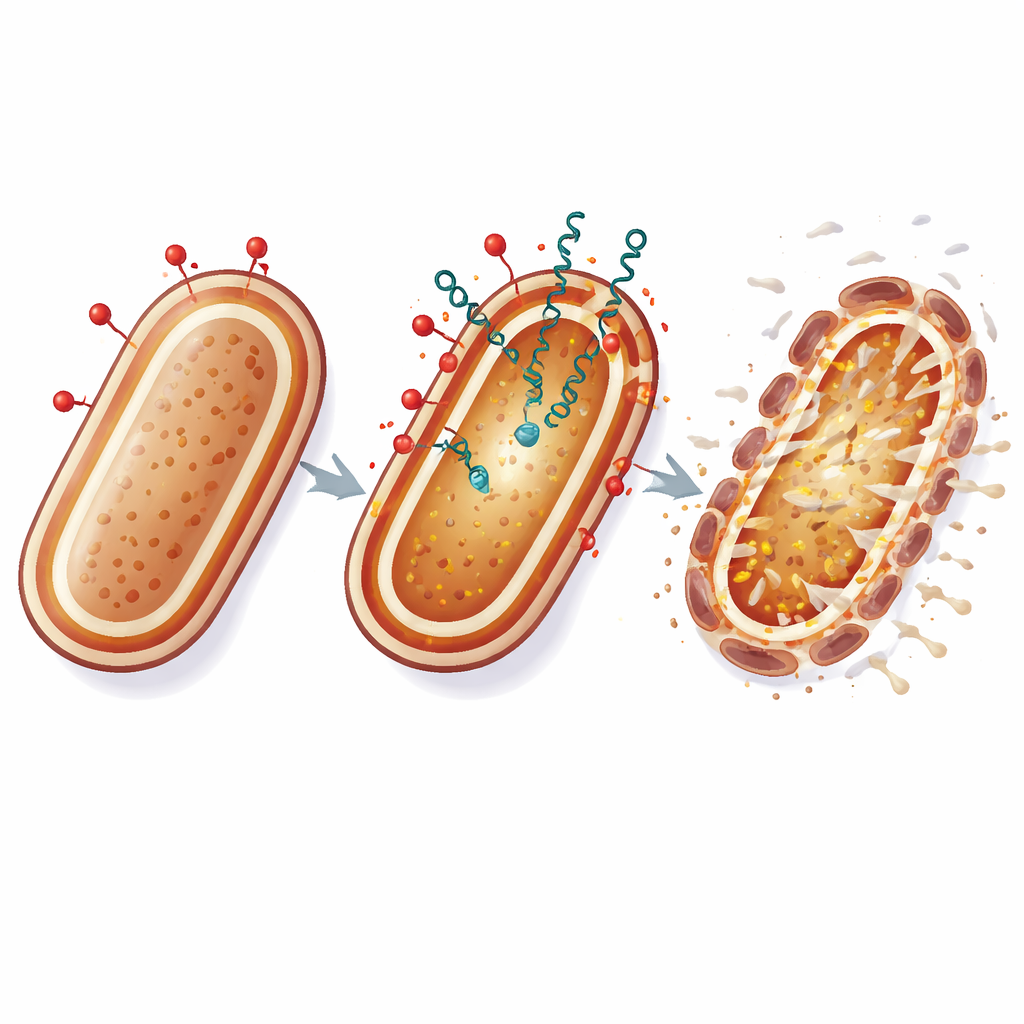
מה זה יכול להצביע לגבי טיפולים בעתיד
במונחים יומיומיים, קוליסטין פועל כמו מוט פריצה שפותח את שריון החיצוני של החיידק, בעוד הבקטריוצינים מתגנבים דרך הסדקים ותוקפים את ממברנת התמיכה הפנימית. על ידי פגיעה במעטפת התא בשני מקומות פגיעים בו‑זמנית, האסטרטגיה הזו מקשה על A. baumannii להסתגל באמצעות שינויים גנטיים פשוטים. אף על פי שהניסויים הללו נעשו במעבדה, התוצאות מרמזות כי שילובים נבחרים בקפידה של אנטיביוטיקות מסורתיות עם פפטידים חיידקיים טבעיים עשויים להאריך את חיי השימוש של תרופות המילוט האחרונות ולהציע אפשרויות חדשות נגד זיהומים בית‑חולים שמתקשים לטיפול בדרך אחרת.
ציטוט: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
מילות מפתח: עמידות לאנטיביוטיקה, Acinetobacter baumannii, קוליסטין, בקטריוצינים, טיפול משולב