Clear Sky Science · pt
Combinações de colistina e bacteriocinas evitam a seleção de resistência à colistina em Acinetobacter baumannii
Por que isso importa para infecções hospitalares
Infecções resistentes a medicamentos adquiridas em hospitais estão cada vez mais difíceis de tratar. Um dos agentes mais preocupantes é a bactéria Acinetobacter baumannii, que consegue resistir a quase todos os antibióticos disponíveis. Os médicos frequentemente precisam recorrer à colistina, um fármaco poderoso de “último recurso”. Mas mesmo a colistina tem começado a falhar à medida que as bactérias evoluem resistência. Este estudo investiga se associar a colistina a peptídeos bacterianos naturais chamados bacteriocinas pode tanto matar esses micróbios persistentes de forma mais eficaz quanto desacelerar o surgimento da resistência.
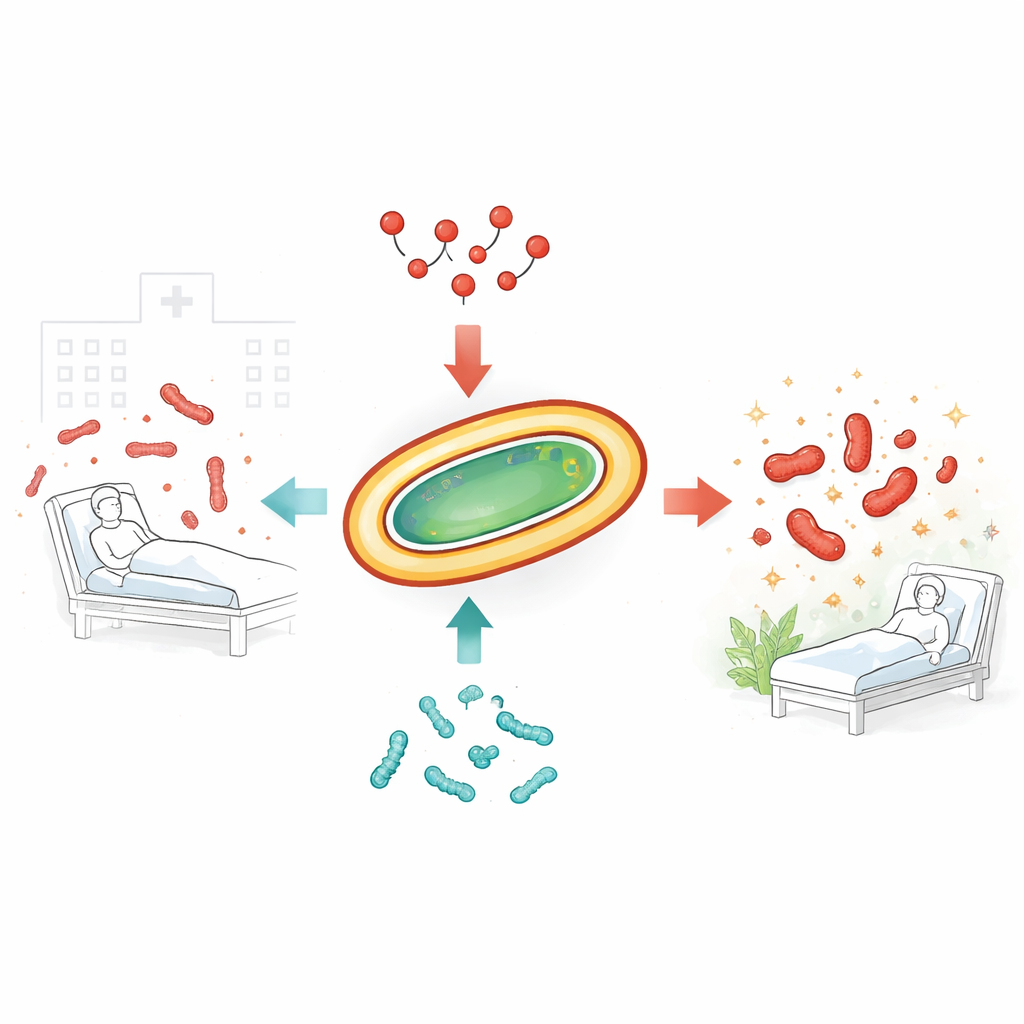
Os germes difíceis que driblam os antibióticos
Os pesquisadores concentraram-se em vários isolados clínicos recentes de A. baumannii, coletados de pacientes reais e já resistentes a muitos medicamentos de uso comum. A análise genética mostrou que essas cepas eram diversas, tanto em seu DNA quanto nos tipos de genes de resistência que carregavam. Testes padrão confirmaram que a maioria ainda era sensível à colistina, enquanto uma cepa era altamente resistente. Quando os cientistas tentaram combinar colistina com outros antibióticos convencionais usados em hospitais, como tigeciclina ou imipeném, as combinações produziram na melhor das hipóteses um efeito aditivo, não a sinergia verdadeira que poderia aumentar significativamente a capacidade de eliminação e conter a resistência.
Armas bacterianas naturais entram na luta
Muitas bactérias produzem suas próprias pequenas armas proteicas, chamadas bacteriocinas, para afastar concorrentes. A equipe triou um painel dessas moléculas e descobriu que várias produzidas por bactérias Gram-positivas inofensivas podiam inibir A. baumannii, embora apenas em doses altas. Selecionaram dois pequenos peptídeos helicoidais—Lacticin Z e Enterocin L50—foram escolhidos para estudo mais aprofundado. Em modelos de membrana em tubo de ensaio, ambos se ligaram fortemente a misturas de lipídios que imitam a membrana interna de A. baumannii e puderam perfurar essas vesículas artificiais. No entanto, bactérias intactas foram muito menos afetadas, sugerindo que a camada externa da bactéria atua como um escudo, impedindo que os peptídeos alcancem seu alvo preferencial.
Colistina abre a porta, bacteriocinas concluem o trabalho
A colistina atua ligando-se a um componente lipídico no revestimento externo de bactérias Gram-negativas e perturbando a estrutura de suas membranas. Em A. baumannii, os autores mostraram que a colistina não só torna a membrana externa permeável, mas também desregula a carga elétrica da membrana interna e esgota o suprimento de ATP da célula, sua principal moeda energética. Sozinha, a colistina frequentemente não conseguiu eliminar todas as células em uma cultura: algumas bactérias sobreviviam e, ao longo do tempo, surgiam mutantes com alterações em genes relacionados à membrana que se tornavam altamente resistentes. Quando os pesquisadores adicionaram doses baixas, por si só inativas, de Lacticin Z ou Enterocin L50 juntamente com a colistina, a sobrevivência bacteriana caiu dramaticamente. A combinação também preveniu ou reduziu muito o regrowth que normalmente sinaliza o surgimento de mutantes resistentes, mesmo quando eles imitavam cepas que haviam perdido parcialmente suas moléculas típicas da camada externa.
Alvejar o envelope celular por dois lados
Para entender como essa parceria funciona, a equipe investigou diferentes maneiras de enfraquecer a superfície bacteriana. Produtos químicos que bloqueiam a síntese do lipídio da camada externa (lipídio A) ou que desestabilizam a membrana externa tornaram A. baumannii mais vulnerável às bacteriocinas, sustentando a ideia de que, uma vez comprometido o escudo externo, os peptídeos podem atingir e danificar a membrana interna. As bacteriocinas também aumentaram a atividade de um antibiótico que mira a parede celular externa, o imipeném, quando esse fármaco já havia começado a perturbar o envelope. Importante, combinar colistina com Lacticin Z ou Enterocin L50 não apenas matou mais células, mas também reduziu drasticamente o aparecimento de mutantes geneticamente resistentes e estáveis. As células sobreviventes tendiam a ser temporariamente tolerantes em vez de permanentemente resistentes.
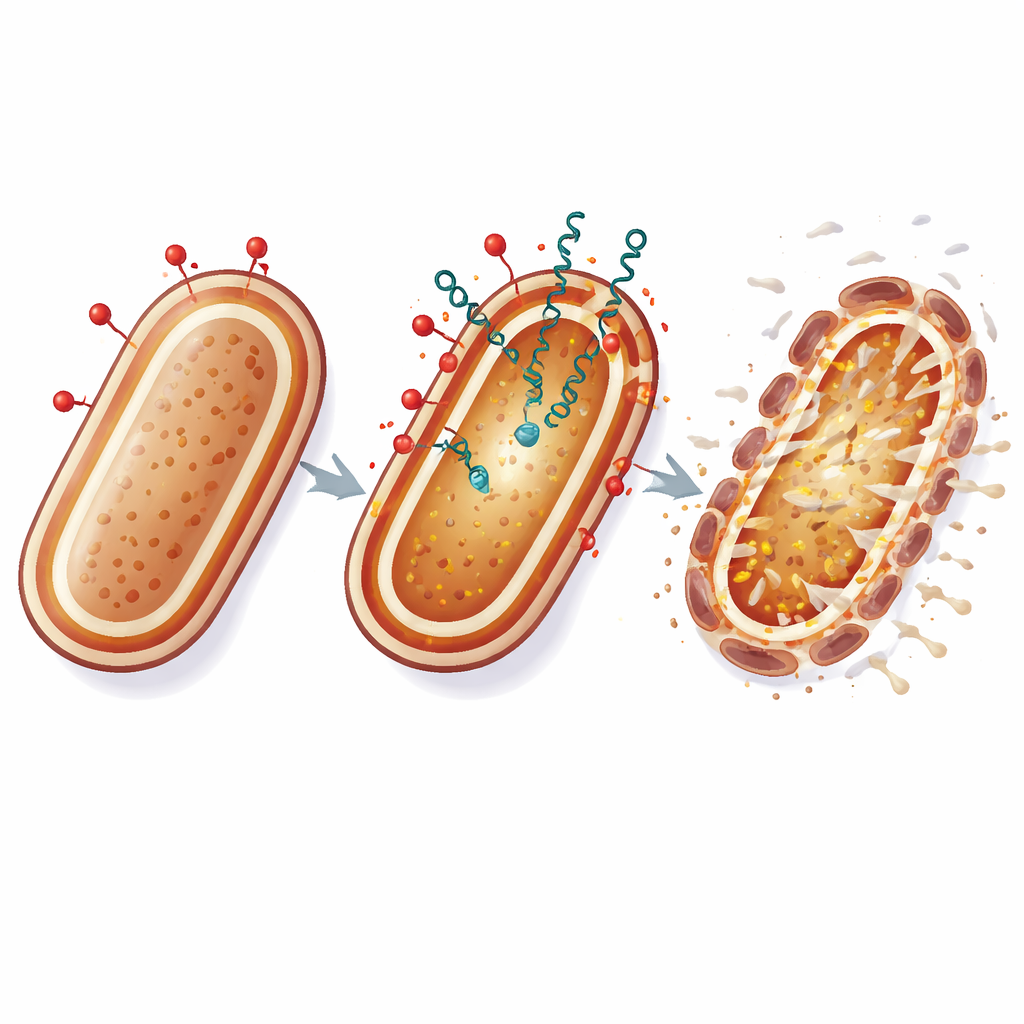
O que isso pode significar para tratamentos futuros
Em termos cotidianos, a colistina age como uma alavanca que abre a armadura externa da bactéria, enquanto as bacteriocinas escorregam pelas frestas e atacam a membrana interna que sustenta a vida. Ao atingir o envelope celular em dois pontos vulneráveis ao mesmo tempo, essa estratégia torna muito mais difícil para A. baumannii se adaptar por meio de simples alterações genéticas. Embora esses experimentos tenham sido feitos em laboratório, os resultados sugerem que combinações bem escolhidas de antibióticos tradicionais com peptídeos bacterianos naturais podem estender a vida útil de fármacos de último recurso e oferecer novas opções contra infecções hospitalares que, de outra forma, seriam intratáveis.
Citação: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
Palavras-chave: resistência a antibióticos, Acinetobacter baumannii, colistina, bacteriocinas, terapia combinada