Clear Sky Science · pl
Połączenia kolistyny i bakteriocyn zapobiegają selekcji oporności na kolistynę w Acinetobacter baumannii
Dlaczego to ma znaczenie w zakażeniach szpitalnych
Zakażenia oporne na leki nabywane w szpitalach stają się coraz trudniejsze do leczenia. Jednym z najbardziej niepokojących sprawców jest bakteria Acinetobacter baumannii, potrafiąca znosić niemal wszystkie dostępne antybiotyki. Lekarze często muszą sięgać po kolistynę — silny lek „ostatniej szansy”. Jednak nawet kolistyna coraz częściej zawodzi, ponieważ bakterie rozwijają oporność. Badanie to analizuje, czy łączenie kolistyny z naturalnymi peptydami bakteryjnymi zwanymi bakteriocynami może zarówno skuteczniej zabijać te uporczywe drobnoustroje, jak i opóźniać narastanie oporności.
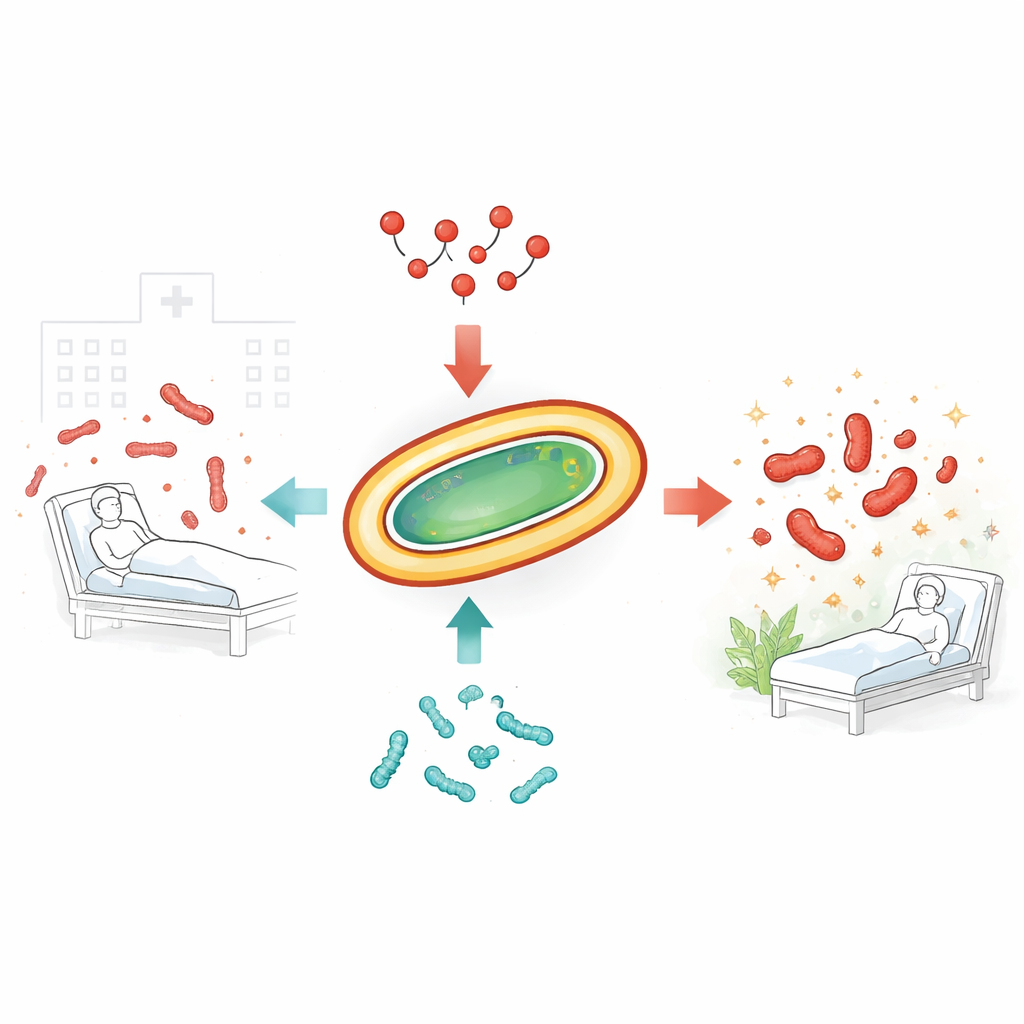
Uporczywe zarazki, które przechytrzają antybiotyki
Naukowcy skupili się na kilku niedawnych izolatów klinicznych A. baumannii, pobranych od prawdziwych pacjentów i już opornych na wiele powszechnie stosowanych leków. Analiza genetyczna wykazała, że szczepy te były zróżnicowane zarówno pod względem DNA, jak i typów genów odpornościowych, które nosiły. Standardowe testy potwierdziły, że większość nadal była wrażliwa na kolistynę, podczas gdy jeden szczep był wysoce oporny. Gdy badacze próbowali łączyć kolistynę z innymi konwencjonalnymi antybiotykami często używanymi w szpitalach, takimi jak tigecyklina czy imipenem, połączenia te dawały co najwyżej efekt addycyjny, a nie prawdziwą synergię, która mogłaby istotnie zwiększyć zabijanie i powstrzymać rozwój oporności.
Naturalne brońki bakteryjne włączają się do walki
Wiele bakterii wytwarza własne maleńkie białkowe „brońki” — bakteriocyny — by odpierać konkurentów. Zespół przesiewał panel tych związków i odkrył, że kilka produkowanych przez niegroźne bakterie Gram-dodatnie może hamować A. baumannii, choć tylko przy wysokich dawkach. Wybrali dwa małe, helikalne peptydy — Lacticin Z i Enterocin L50 — do głębszych badań. W modelach membran in vitro oba silnie wiązały się z mieszaninami lipidów imitujących wewnętrzną błonę A. baumannii i potrafiły przebijać otwory w tych sztucznych wakuolach. Jednak intactne bakterie były znacznie mniej dotknięte, co sugeruje, że zewnętrzna warstwa bakterii działa jak tarcza, uniemożliwiając peptydom dotarcie do ich preferowanego celu.
Kolistyna otwiera drzwi, bakteriocyny kończą robotę
Kolistyna działa poprzez wiązanie się z komponentem lipidowym w zewnętrznej powłoce bakterii Gram-ujemnych i zaburzanie struktury ich błon. U A. baumannii autorzy pokazali, że kolistyna nie tylko powoduje przeciekanie błony zewnętrznej, lecz także zakłóca ładunek elektryczny błony wewnętrznej i wyczerpuje zapasy ATP komórki, jej głównej waluty energetycznej. Sama kolistyna często nie była w stanie wyeliminować wszystkich komórek w hodowli: część bakterii przetrwała i z upływem czasu pojawiały się mutacje w konkretnych genach związanych z błonami, które dawały wysoką oporność. Gdy badacze dodali niskie, same w sobie nieaktywne dawki Lacticin Z lub Enterocin L50 razem z kolistyną, przeżywalność bakterii gwałtownie spadła. Kombinacja ta zapobiegała lub znacznie ograniczała ponowny wzrost, który zwykle sygnalizuje pojawienie się opornych mutantów, nawet gdy naśladowano szczepy częściowo pozbawione typowych zewnętrznych cząsteczek warstwy.
Atak na osłonę komórkową z dwóch stron
Aby zrozumieć mechanizm współdziałania, zespół badał różne sposoby osłabiania powierzchni bakterii. Chemikalia blokujące syntezę zewnętrznego lipidu (lipidu A) lub destabilizujące błonę zewnętrzną uczyniły A. baumannii bardziej podatnym na bakteriocyny, co wspiera hipotezę, że po naruszeniu zewnętrznej tarczy peptydy mogą dotrzeć do i uszkodzić błonę wewnętrzną. Bakteriocyny zwiększały także aktywność antybiotyku celującego w zewnętrzną ścianę komórkową, imipenemu, gdy ten lek już zaczął naruszać otoczkę. Co ważne, łączenie kolistyny z Lacticin Z lub Enterocin L50 nie tylko zabijało więcej komórek, lecz także ostro zmniejszało pojawianie się trwałych, genetycznie odpornych mutantów. Przetrwałe komórki miały raczej charakter przejściowej tolerancji niż stałej oporności.
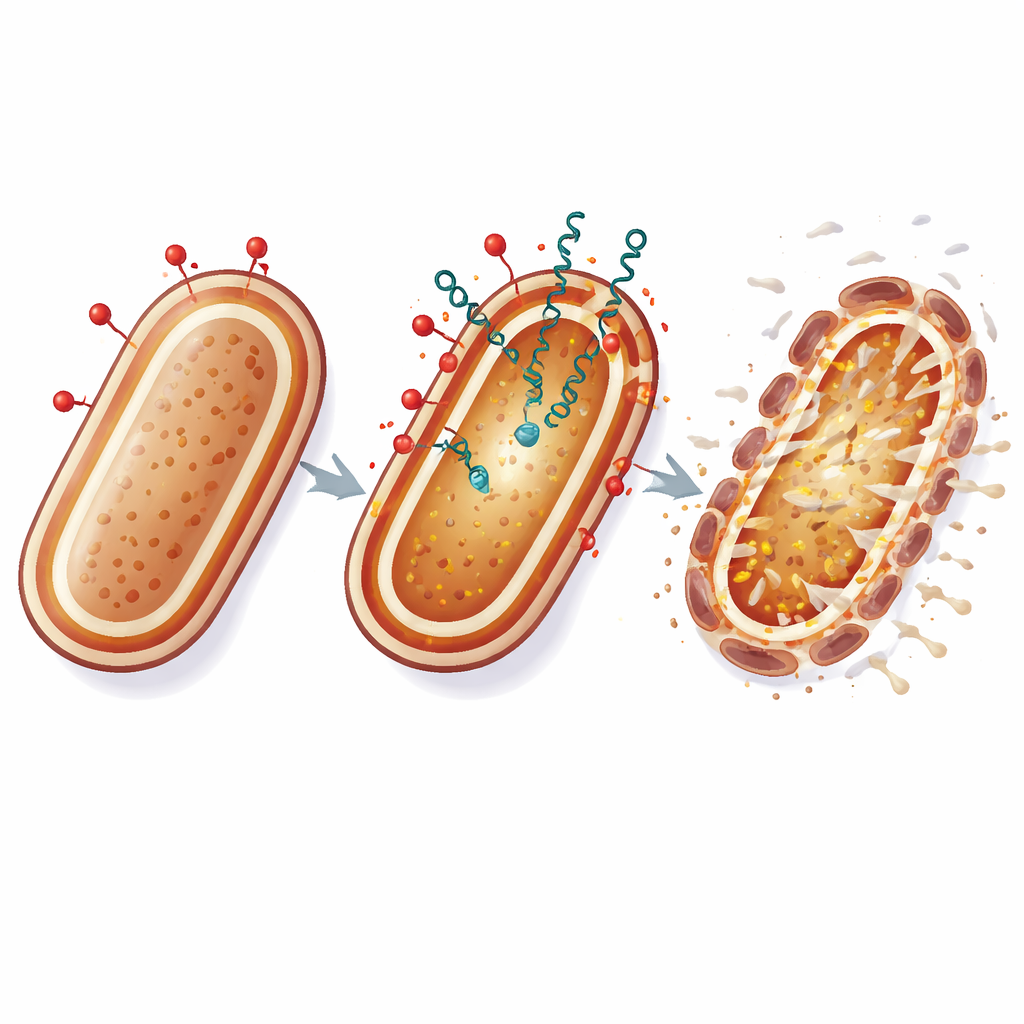
Co to może znaczyć dla przyszłych terapii
Mówiąc prościej, kolistyna działa jak łom, który rozdziera zewnętrzną zbroję bakterii, podczas gdy bakteriocyny wślizgują się przez szczeliny i atakują wewnętrzną, kluczową błonę podtrzymującą życie. Uderzając w osłonę komórkową w dwóch wrażliwych punktach jednocześnie, ta strategia znacząco utrudnia A. baumannii adaptację przez proste genetyczne modyfikacje. Chociaż eksperymenty przeprowadzono w laboratorium, wyniki sugerują, że starannie dobrane kombinacje tradycyjnych antybiotyków z naturalnymi peptydami bakteryjnymi mogą wydłużyć użyteczność leków ostatniej szansy i zaoferować nowe opcje przeciwko inaczej nieuleczalnym zakażeniom szpitalnym.
Cytowanie: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
Słowa kluczowe: oporność na antybiotyki, Acinetobacter baumannii, kolistyna, bakteriocyny, terapia skojarzona