Clear Sky Science · de
Kombinationen aus Colistin und Bakteriocinen verhindern die Selektion von Colistinresistenz in Acinetobacter baumannii
Warum das für Krankenhausinfektionen wichtig ist
In Krankenhäusern erworbene, medikamentenresistente Infektionen werden zunehmend schwerer zu behandeln. Einer der beunruhigendsten Erreger ist das Bakterium Acinetobacter baumannii, das gegen fast alle verfügbaren Antibiotika immun sein kann. Ärztinnen und Ärzte müssen häufig auf Colistin zurückgreifen, ein starkes „letztes Mittel“. Doch selbst Colistin versagt zunehmend, weil die Bakterien Resistenzen entwickeln. Die vorliegende Studie untersucht, ob die Kombination von Colistin mit natürlichen bakteriellen Peptiden, sogenannten Bakteriocinen, diese hartnäckigen Keime wirksamer töten und gleichzeitig das Entstehen von Resistenzen verlangsamen kann.
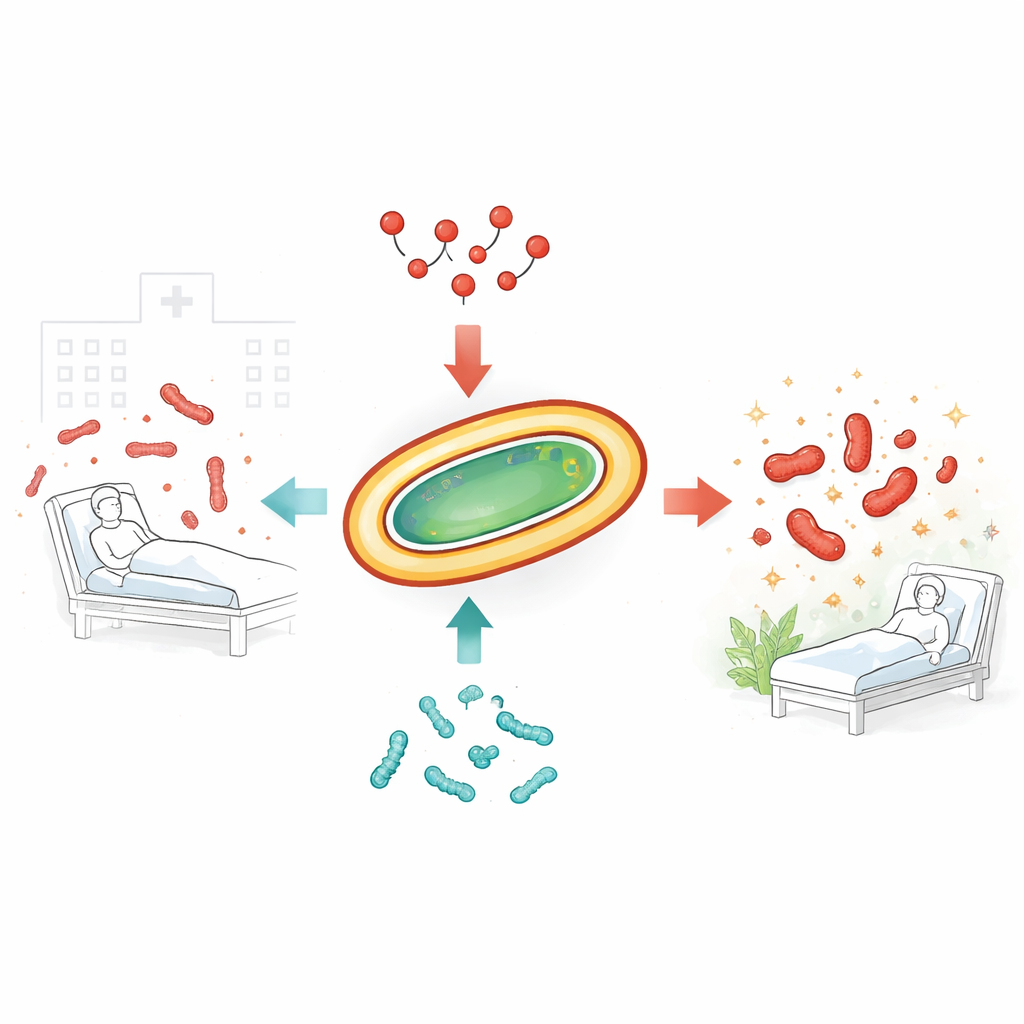
Die zähen Keime, die Antibiotika überlisten
Die Forschenden konzentrierten sich auf mehrere aktuelle klinische Isolate von A. baumannii, die von realen Patientinnen und Patienten stammten und bereits gegenüber vielen gebräuchlichen Wirkstoffen resistent waren. Genetische Analysen zeigten, dass diese Stämme vielfältig waren, sowohl in ihrer DNA als auch in den Arten der getragenen Resistenzgene. Standardtests bestätigten, dass die meisten noch empfindlich gegenüber Colistin waren, während ein Stamm hochgradig resistent war. Als die Wissenschaftler Colistin mit anderen konventionellen Antibiotika kombinierten, die in Krankenhäusern oft verwendet werden, wie Tigecyclin oder Imipenem, ergaben die Paarungen bestenfalls einen additiven Effekt, aber keine echte Synergie, die das Abtöten deutlich verstärken und die Resistenzbildung eindämmen könnte.
Natürliche bakterielle Waffen schließen sich dem Kampf an
Viele Bakterien produzieren winzige Proteinwaffen, sogenannte Bakteriocine, um Konkurrenten abzuwehren. Das Team screente eine Reihe dieser Moleküle und fand, dass mehrere von harmlosen Gram-positiven Bakterien produzierte Bakteriocine A. baumannii hemmen konnten, wenn auch nur in hohen Dosen. Sie wählten zwei kleine, helikale Peptide – Lacticin Z und Enterocin L50 – für vertiefte Untersuchungen aus. In Modell-Systemen mit Membranmimetika hefteten sich beide stark an Fettgemische, die der inneren Membran von A. baumannii ähneln, und konnten Löcher in diese künstlichen Vesikel stanzen. Intakte Bakterien waren jedoch deutlich weniger betroffen, was darauf hindeutet, dass die äußere Oberflächenschicht des Bakteriums als Schutz wirkt und verhindert, dass die Peptide ihr bevorzugtes Ziel erreichen.
Colistin öffnet die Tür, Bakteriocine vollenden die Arbeit
Colistin wirkt, indem es an eine Lipidkomponente in der äußeren Hülle gramnegativer Bakterien bindet und die Struktur ihrer Membranen stört. Bei A. baumannii zeigten die Autorinnen und Autoren, dass Colistin nicht nur die äußere Membran durchlässig macht, sondern auch das Membranpotenzial der inneren Membran stört und den ATP-Vorrat der Zelle, ihre Hauptenergiequelle, entleert. Allein angewandt gelangte Colistin oft nicht dazu, alle Zellen einer Kultur zu eliminieren: Einige Bakterien überlebten, und mit der Zeit traten Mutanten mit Veränderungen in spezifischen membranbezogenen Genen auf, die hochgradige Resistenz vermittelten. Wenn die Forschenden niedrige, sonst inaktive Dosen von Lacticin Z oder Enterocin L50 zusammen mit Colistin gaben, sank das Überleben der Bakterien dramatisch. Die Kombination verhinderte oder verringerte zudem deutlich das nachfolgende Nachwachsen, das üblicherweise das Aufkommen resistenter Mutanten signalisiert – selbst bei Stämmen, die teilweise ihre typischen äußeren Schichtmoleküle verloren hatten.
Die Zellhülle von zwei Seiten angreifen
Um zu verstehen, wie diese Partnerschaft wirkt, untersuchte das Team verschiedene Wege, die bakterielle Oberfläche zu schwächen. Chemikalien, die die Synthese des äußeren Lipids (Lipid A) blockieren oder die äußere Membran destabilisieren, machten A. baumannii anfälliger für die Bakteriocine und stützten die Idee, dass die Peptide, sobald der äußere Schutz kompromittiert ist, die innere Membran erreichen und schädigen können. Die Bakteriocine erhöhten außerdem die Wirksamkeit eines außen an der Zellwand angreifenden Antibiotikums, Imipenem, wenn dieses Medikament bereits begonnen hatte, die Hülle zu stören. Wichtig ist, dass die Kombination von Colistin mit Lacticin Z oder Enterocin L50 nicht nur mehr Zellen abtötete, sondern auch das Auftreten stabiler, genetisch resistenter Mutanten deutlich reduzierte. Die überlebenden Zellen zeigten eher vorübergehende Toleranz als dauerhafte Resistenz.
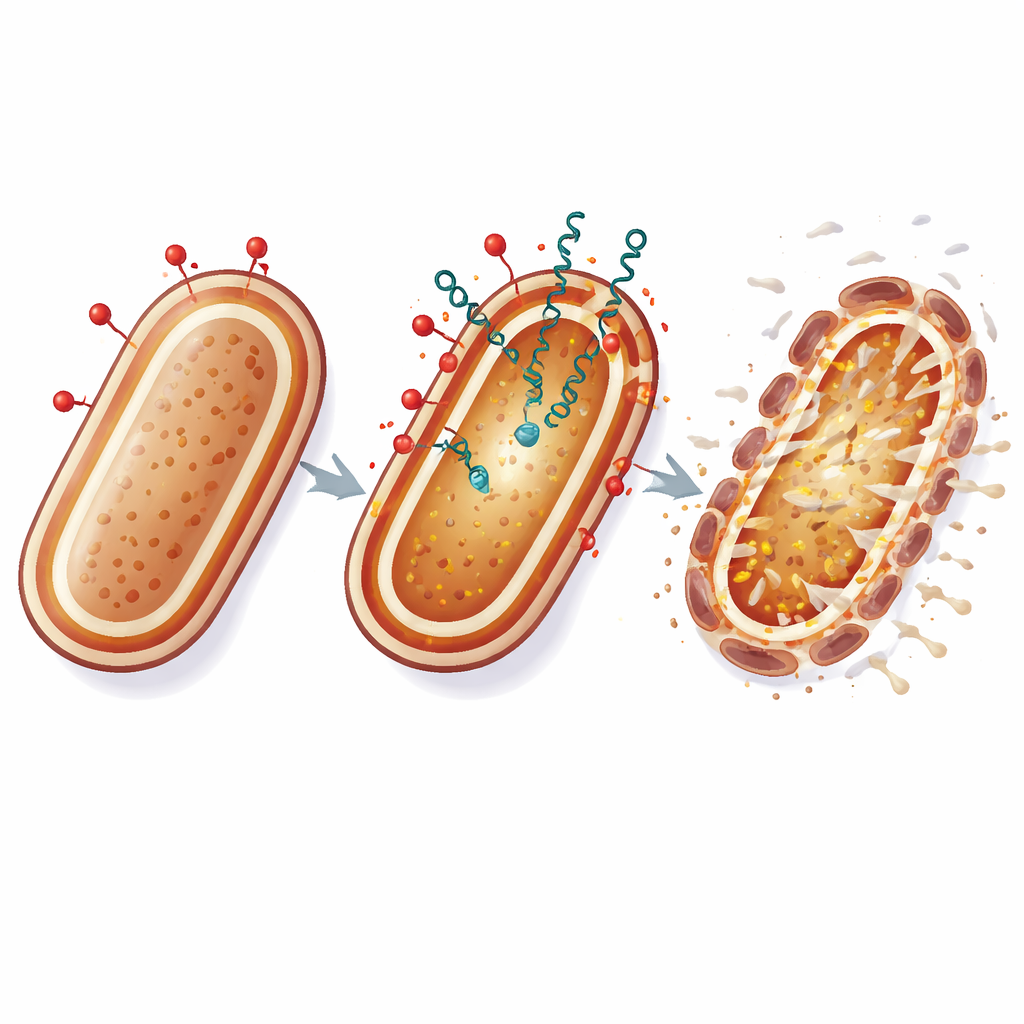
Was das für künftige Behandlungen bedeuten könnte
Anschaulich wirkt Colistin wie ein Brecheisen, das die äußere Rüstung des Bakteriums aufrechtert, während Bakteriocine durch die entstandenen Spalten schlüpfen und die lebenswichtige innere Membran angreifen. Indem die Zellhülle an zwei verwundbaren Stellen gleichzeitig getroffen wird, erschwert diese Strategie A. baumannii die Anpassung durch einfache genetische Veränderungen erheblich. Obwohl diese Experimente im Labor durchgeführt wurden, deuten die Ergebnisse darauf hin, dass sorgfältig gewählte Kombinationen aus traditionellen Antibiotika und natürlichen bakteriellen Peptiden die Nutzungsdauer von Reserveantibiotika verlängern und neue Optionen gegen sonst schwer behandelbare Krankenhausinfektionen bieten könnten.
Zitation: Rubio, T., zur Nedden, T., Zedek, S. et al. Combinations of colistin and bacteriocins prevent the selection of colistin resistance in Acinetobacter baumannii. Commun Biol 9, 599 (2026). https://doi.org/10.1038/s42003-026-09883-6
Schlüsselwörter: antibiotikaresistenz, Acinetobacter baumannii, Colistin, Bakteriocine, Kombinationstherapie