Clear Sky Science · zh
被泰勒虫(Theileria annulata)转化的巨噬细胞中H3K27me3标记的表观遗传景观
为什么一种牛寄生虫对癌症生物学重要
热带泰勒虫病是一种由蜱传播的寄生虫Theileria annulata引起的严重牛病。寄生虫进入宿主后,将某些白细胞转变为不断分裂、能移动的细胞,这些细胞的行为很像癌细胞。被转化的细胞在体内扩散并驱动疾病。有趣的是,当这类受感染细胞在体外长期培养时,它们的扩散能力会逐渐丧失。本文提出了一个简单但意义深远的问题:在感染细胞丧失侵袭性时,其DNA包装(染色质)发生了哪些变化,这对更广泛的类癌生长有什么启示?
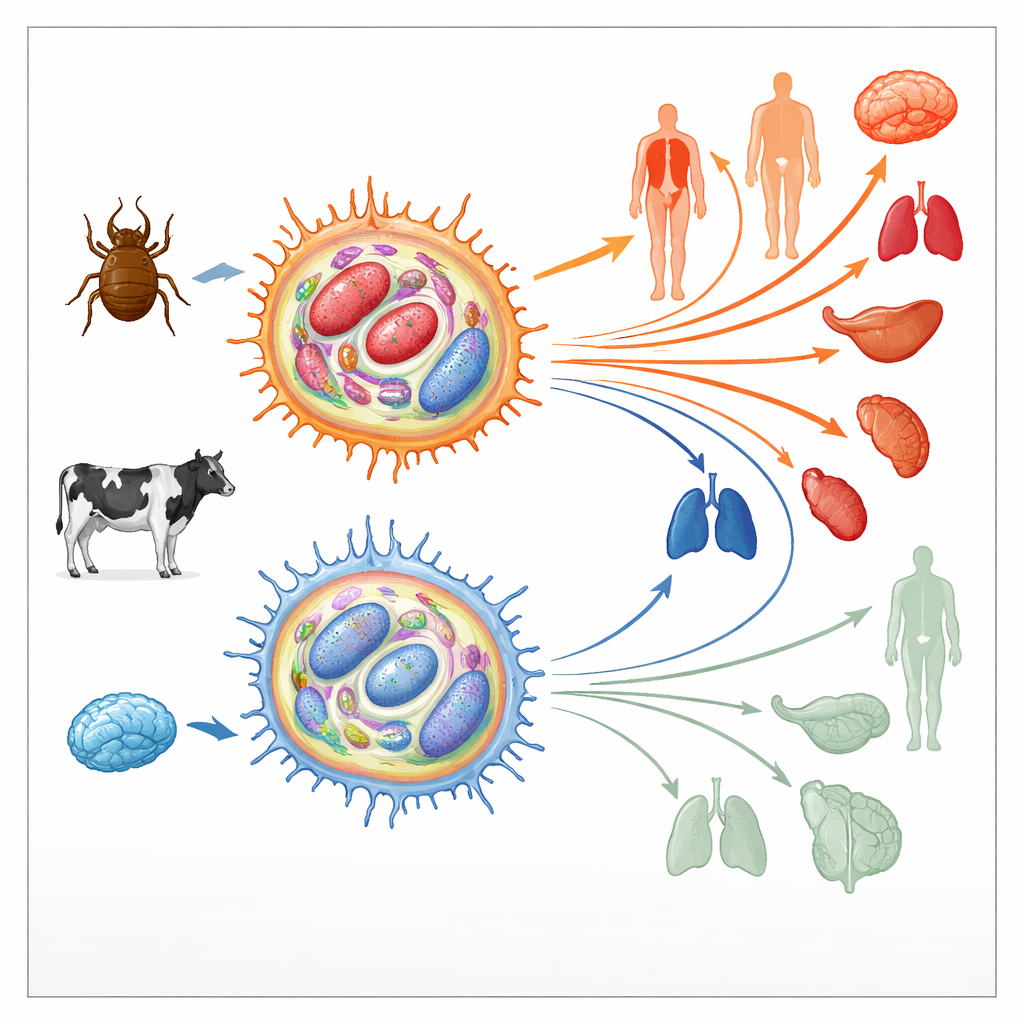
寄生虫如何改造宿主免疫细胞
Theileria annulata寄居于牛的免疫细胞——巨噬细胞内。在那里,它操控通常控制细胞死亡、增殖和运动的关键信号通路,将宿主细胞推入一种类似肿瘤的状态。这些被劫持的细胞随后可以无限分裂并穿行组织,从而扩散寄生虫。早期培养时,这类受感染的巨噬细胞高度“毒力”,在动物体内易于扩散。但经过数百次细胞分裂后,它们的扩散能力急剧下降;它们变得“减毒”,甚至被用作活疫苗。由于在人类癌症中也会发生类似的由侵袭性向低侵袭性状态的转变,作者考察了细胞表观遗传景观——那些在不改变DNA序列情况下开关基因的化学标记——的变化是否可能是这一开关的基础。
聚焦一种强效的基因沉默标记
研究聚焦于组蛋白上的一种特定化学标签H3K27me3。该标签由被称为多梳抑制复合体2(PRC2)的蛋白复合体添加,以关闭控制细胞身份和发育的基因而著称。作者使用染色质免疫沉淀后测序(ChIP-seq)绘制了H3K27me3在牛基因组中于毒力型和减毒型受感染巨噬细胞的分布图。同时他们也绘制了与基因激活相关的H3K4me3作为比较。他们确认抗体检测的是宿主细胞的H3K27me3,而非寄生虫自身的组蛋白,因此这些图谱反映的是牛细胞而非微生物的变化。
从尖锐峰到广泛沉默域
总体来看,减毒细胞中的H3K27me3含量更高,而激活标记H3K4me3则更低。然而比总量更引人注目的是分布模式的变化。在毒力型巨噬细胞中,H3K27me3呈现在基因起始位点附近的窄峰,这种构型常与精确的PRC2驱动基因控制相关。在减毒细胞中,该标记扩展成广泛的区域,向周围区域延伸,有时覆盖许多相邻基因。一个生动的例子是参与巨噬细胞粘附的SKAP2基因:在毒力细胞中它带有一小块局部的H3K27me3,而在减毒细胞中它处于一个超过500千碱基的大型抑制域内并被强烈下调。全基因组范围内,这种扩展很常见,表明随着细胞从毒力向减毒行为转变,染色质包装方式发生了整体重塑。
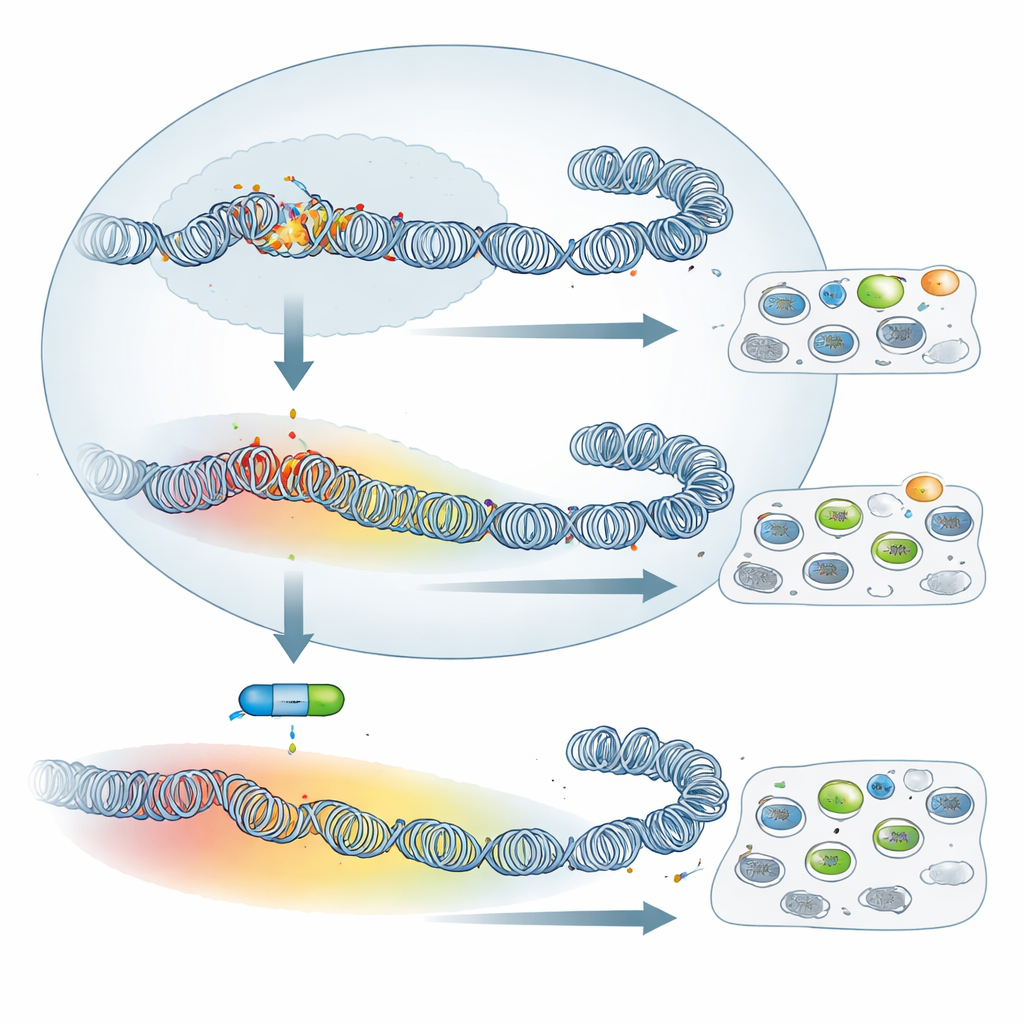
阻断沉默机器的影响有限
鉴于这种广泛的重构,人们可能会预期抑制PRC2并擦除H3K27me3会显著改变这些细胞的行为。团队用UNC1999(一种抑制PRC2酶活性的药物)处理了毒力型和减毒型巨噬细胞,并确认H3K27me3大体丧失。然而经典的类似肿瘤特性几乎没有改变:细胞在培养皿中与纤连蛋白的黏附能力以及在免疫缺陷小鼠中的扩散能力,均未被该药物显著影响。当作者通过RNA测序检查基因表达时,发现被重新激活的基因在毒力细胞中远多于减毒细胞。换句话说,尽管减毒细胞具有更广泛的H3K27me3覆盖,但其基因沉默对PRC2的依赖性较低。尽管如此,一小部分共同基因,包括已知或疑似的肿瘤抑制子如颗粒酶A(Granzyme A)和抑制素结合蛋白(Follistatin),在两种细胞类型中都可被该抑制剂重唤醒,表明核心的PRC2程序仍然存在。
对疾病和治疗的意义
这项工作表明,当寄生虫转化的巨噬细胞失去扩散能力时,其表观遗传景观发生了深刻重塑:一种关键的沉默标记从尖锐峰扩展成宽广的域,但这并不等同于对基因的更强压制。相反,减毒细胞中的全局PRC2驱动抑制趋于减弱,而一小部分关键基因仍依赖该机制保持沉默。对于畜牧业健康而言,研究结果提示单纯针对PRC2不太可能成为控制由Theileria引起的肿瘤的有效方法。更广泛地说,该研究展示了感染如何将宿主细胞推动到类癌的表观遗传状态,以及染色质结构的剧烈变化并不总是带来直接明了的功能后果。理解这些细微的表观遗传转变,可能有助于改进未来在传染病与癌症中调整基因调控的策略。
引用: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
关键词: 表观遗传学, 泰勒虫, 巨噬细胞, 组蛋白修饰, PRC2