Clear Sky Science · he
נוף אפיגנטי של סימן H3K27me3 במקרופאגים שהומרו על־ידי Theileria annulata
מדוע טפיל בקר חשוב לביולוגיית סרטן
תיילריוזיס טרופי היא מחלה קשה של בקר הנגרמת על־ידי הטפיל Theileria annulata, המועבר על־ידי קרציות. לאחר כניסתו לגוף בעל־החיים, הטפיל הופך תאי דם לבנים מסוימים לתאים שגדלים ללא הפסקה וניידים, שמתנהגים במובנים רבים כמו סרטן. תאים מומרים אלה מתפשטים בגוף וגורמים למחלה. באופן מרתק, כאשר תאים כאלה שמדביקים במעבדה מגדלים זמן רב, הם בהדרגה מאבדים את יכולת ההתפשטות שלהם. המאמר שואל שאלה פשוטה אך רחבת היקף: אילו שינויים באריזת ה‑DNA של התאים המודבקים מלווים את אובדן האגרסיביות הזה, ומה זה מלמד אותנו על גדילה דמוית־סרטן בצורה רחבה יותר?
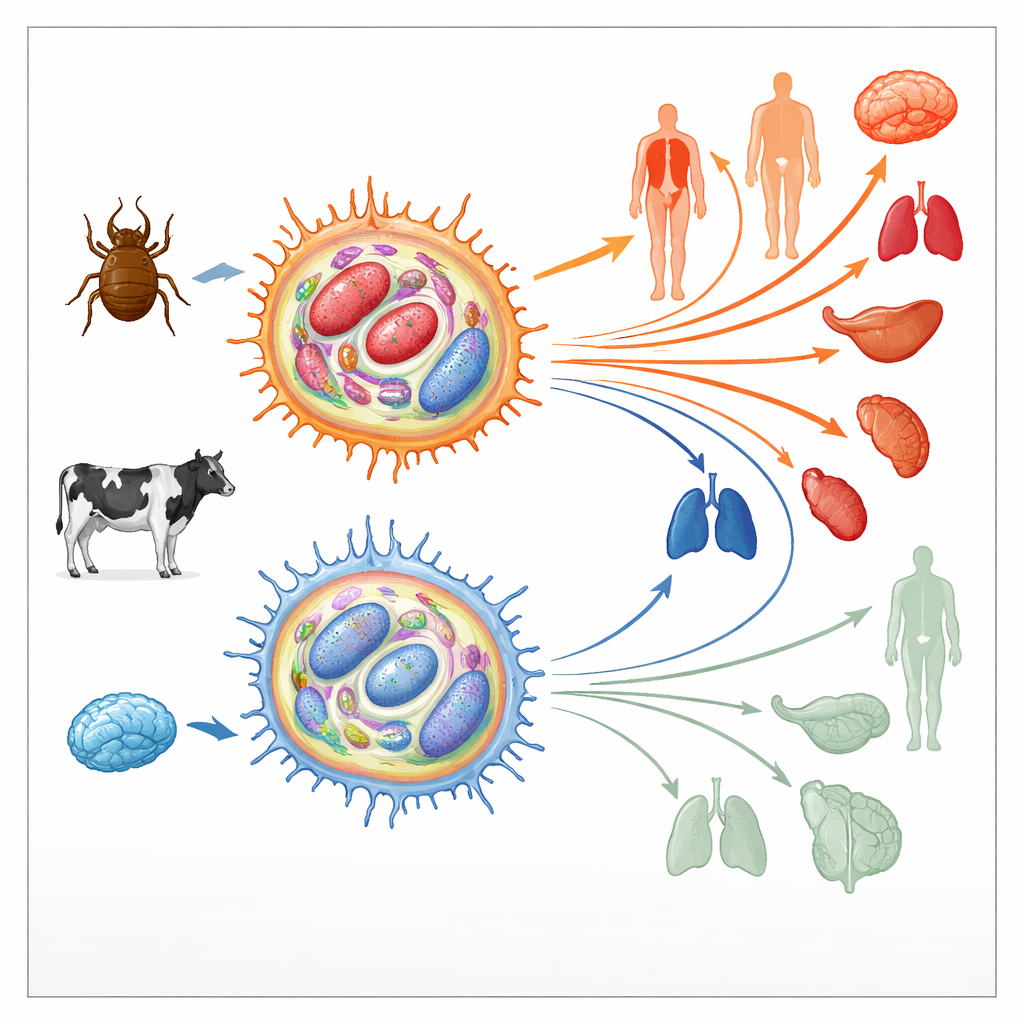
כיצד הטפיל מחדש את תאי החיסון של המארח
Theileria annulata חי בתוך תאי חיסון פריים של בקר הקרויים מקרופאגים. שם הוא משתלט על מסלולי איתות מרכזיים שבאופן רגיל שולטים במוות התא, החלוקה והתנועה, ודוחף את תא המארח למצב דמוי־גידול. תאים שנחטפו אלה יכולים להתחלק ללא הגבלה ולהתנייד דרך רקמות, ולהפיץ את הטפיל. בתחילת הגידול בתרבית, מקרופאגים מודבקים כאלה הם מאוד "ורלנטיים" — כלומר הם מתפשטים בקלות בחיות. לאחר מאות מחזורי חלוקה, עם זאת, יכולת ההתפשטות שלהם צונחת באופן חדה; הם נעשים "מתוערים" ומשמשים אפילו כחיסונים חיים. מאחר שמעברים דומים ממצב אגרסיבי לפחות אגרסיבי מתרחשים גם בסרטן האנושי, המחברים חקרו האם שינויים בנוף האפיגנטי של התאים — הסימנים הכימיים המסייעים להדליק או לכבות גנים בלי לשנות רצף ה‑DNA — עשויים לעמוד בבסיס המעבר הזה.
מיקוד בסמן עוצמתי לדיכוי גנים
המחקר מתמקד בתג כימי ספציפי על חלבוני היסטון, שנקרא H3K27me3. תג זה נוסף על‑ידי קומפלקס חלבוני הידוע כ‑Polycomb Repressive Complex 2 (PRC2) ומפורסם בכיבוי גנים השולטים בזהות תא ובהתפתחות. באמצעות המשיכה של כרומטין ואחריה רציפתו (ChIP‑seq), המחברים מיפו היכן נמצא H3K27me3 ברחבי הגנום של בקר בתאים מודבקים ורלנטיים לעומת מתוערים. הם גם מיפו את H3K4me3, סמן המשויך לגנים פעילים, לצורך השוואה. הם אימתו שהנוגדן שלהם מזהה את גרסת ה‑H3K27me3 של תא המארח אך לא את ההיסטונים של הטפיל, כך שהמפות משקפות שינויים בתא הבקר ולא במיקרוב.
מפיקים חדים לדומיינים שקטים ורחבים
כמות כוללת של H3K27me3 הייתה גבוהה יותר בתאים המתוערים, בעוד שהסמן המפעיל H3K4me3 היה נמוך יותר. יותר בולט מהכמויות הכוללות היה השינוי בתבנית. במקרופאגים ורלנטיים, H3K27me3 יצר שיאים צרים שממוקמים בסמוך לנקודות תחילת גנים, תצורה שנקשרת לעתים קרובות לבקרת גנים מדויקת מונעת על‑ידי PRC2. בתאים מתוערים, התג התפשט ויצר דומיינים רחבים שנטו להיכנס לאזורים הסובבים, לעיתים לכסות גנים שכנים רבים. דוגמה ברורה היא הגן SKAP2, המעורב בהיקשרות של מקרופאגים: בתאים ורלנטיים הוא נושא טלאי מקומי קטן של H3K27me3, אך בתאים מתוערים הוא נמצא בתוך דומיין רפרסיבי שאורך יותר מ‑500 קילובס וגורם לדיכוי חזק שלו. ברחבי הגנום, התפשטות כזו הייתה שכיחה, דבר שמרמז על עיצוב מחדש מקיף של אופן אריזת ה‑DNA כאשר התאים עוברים ממצב ורלנטי למתוער.
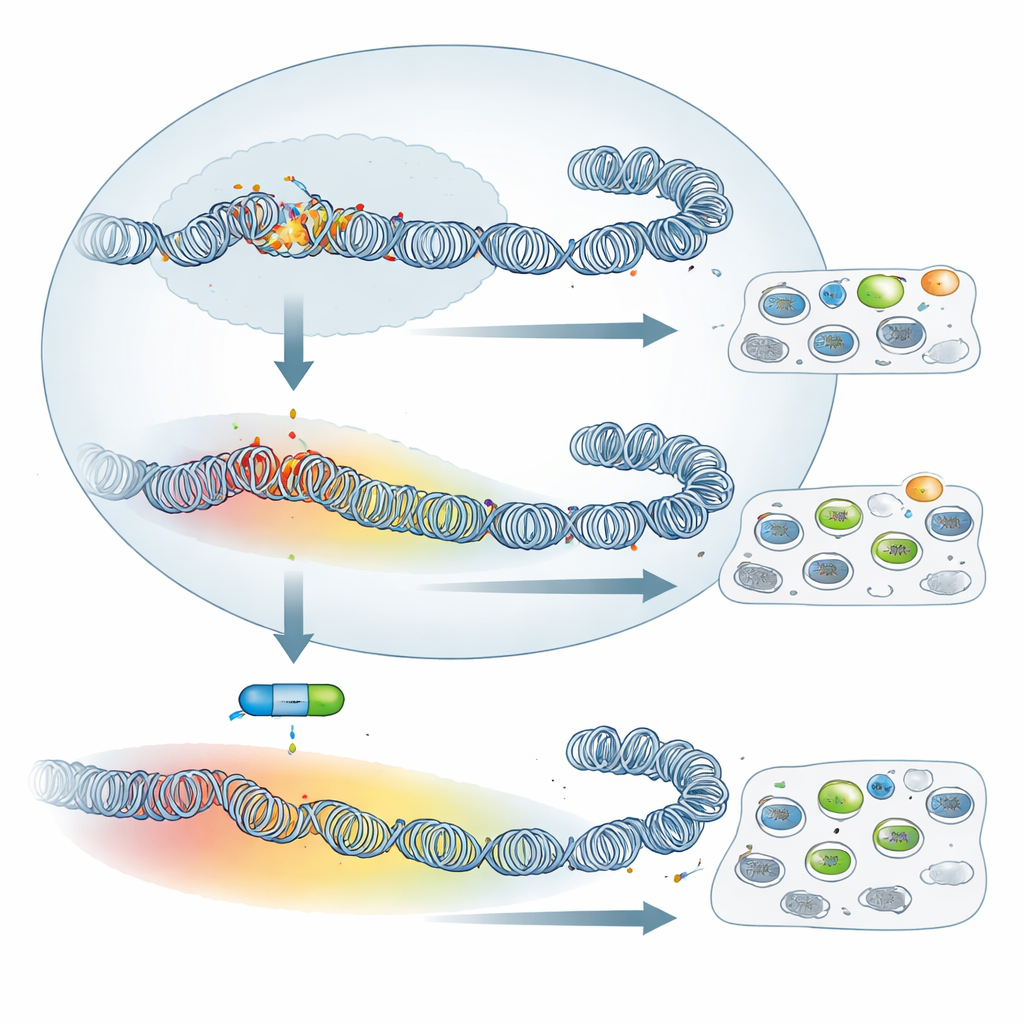
חסימת מכונת הכיבוי משפיעה במידה מוגבלת
לאור העיצוב מחדש הנרחב הזה, אפשר היה לצפות שכיבוי PRC2 — ובכך מחיקת H3K27me3 — ישנה באופן דרמטי את התנהגות התאים. הקבוצה טיפלה הן בתאים ורלנטיים והן בתאים מתוערים ב‑UNC1999, תרופה המעכבת את הפעילות האנזימטית של PRC2, ואישרה כי H3K27me3 אכן אבד ברובו. עם זאת, התכונות הקלאסיות דמויות־הגידול השתנו במעט: היכולת של התאים להידבק לפיברונקטין במנה, והקיבולת שלהם להתפשט בעכברים חסרי חיסון, לא הושפעו משמעותית על‑ידי התרופה. כאשר המחברים בחנו פעילות גנים בריצוף RNA, הם מצאו שרבים יותר גנים הופעלו מחדש בתאים ורלנטיים מאשר בתאים מתוערים. במילים אחרות, אף על‑פי שתאים מתוערים נושאים כיסוי רחב יותר של H3K27me3, הדיכוי הגנטי שלהם תלוי פחות ב‑PRC2. עם זאת, קבוצה קטנה משותפת של גנים, כולל מדכאי גידול ידועים או חשודים כגון גרנזים A ופוליסטטין, הועוררה מחדש על‑ידי המעכב בשני סוגי התאים, מה שמראה שתוכנית מרכזית של PRC2 נשמרת.
מובן הדבר למחלה ולטיפול
עבודה זו מראה שכאשר מקרופאגים שהומרו על‑ידי טפיל מאבדים את יכולת ההתפשטות שלהם, הנוף האפיגנטי שלהם מעוצב מחדש באופן עמוק: סמן כיבוי מרכזי מתפשט משיאים חדים לדומיינים רחבים, אך הדבר אינו מתורגם לפשטות לכיבוי חזק יותר של גנים. במקום זאת, הדיכוי הגלובלי המונע על‑ידי PRC2 מוחלש בתאים מתוערים, בעוד שקבוצת משנה של גנים חיוניים עדיין תלויה במכונה זו כדי להישאר כבויים. עבור בריאות הבקר, הממצאים מרמזים כי מיקוד ב‑PRC2 לבדו ככל הנראה לא יהיה דרך יעילה לשלוט בגידולים הנגרמים על‑ידי Theileria בחיות. ביתר דיוק, המאמר מדגים כיצד זיהום יכול לדחוף תאי מארח למצבים אפיגנטיים דמויי‑סרטן, וכיצד שינויים דרמטיים במבנה הכרומטין אינם תמיד מובילים לתוצאות פונקציונליות פשוטות וברורות. הבנת השינויים האפיגנטיים העדינים האלה עשויה לסייע בעדכון אסטרטגיות עתידיות שמטרתן לכוונן את ויסות הגנים גם במחלות זיהומיות וגם בסרטן.
ציטוט: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
מילות מפתח: אפיגנטיקה, Theileria, מקרופאגים, שינוי היסטון, PRC2