Clear Sky Science · de
Epigenetische Landschaft der H3K27me3-Markierung in von Theileria annulata verwandten Makrophagen
Warum ein Rindparasiten für die Krebsbiologie relevant ist
Die tropische Theileriose ist eine schwere Rinderkrankheit, verursacht durch den Parasiten Theileria annulata, der von Zecken übertragen wird. Einmal im Tier angekommen, verwandelt der Parasit bestimmte weiße Blutzellen in unaufhörlich teilende, mobile Zellen, die sich in vielen Eigenschaften wie Krebs verhalten. Diese transformierten Zellen verbreiten sich im Körper und treiben die Krankheit voran. Auffällig ist, dass solche infizierten Zellen bei langem Kultivieren im Labor nach und nach ihre Ausbreitungsfähigkeit verlieren. Die vorliegende Arbeit stellt eine einfache, aber weitreichende Frage: Welche Veränderungen in der DNA-Verpackung der infizierten Zellen begleiten diesen Verlust an Aggressivität, und was lehrt uns das allgemein über krebsähnliches Wachstum?
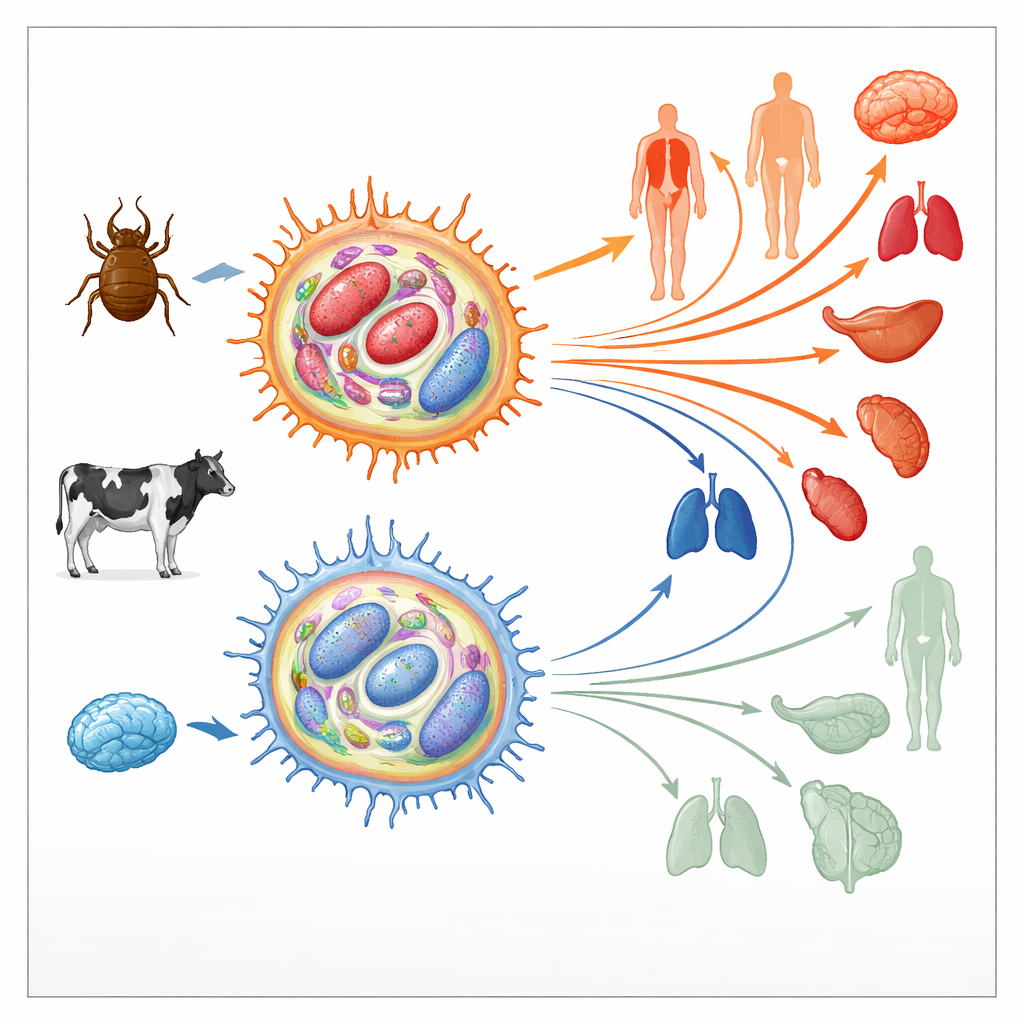
Wie der Parasit Wirts-Immunzellen umfunktioniert
Theileria annulata lebt in bovinen Immunzellen, sogenannten Makrophagen. Dort manipuliert er zentrale Signalwege, die normalerweise Zelltod, Zellteilung und Bewegung steuern, und treibt die Wirtszelle in einen tumorähnlichen Zustand. Diese gekaperten Zellen können sich dann unbegrenzt teilen und durch Gewebe wandern und so den Parasiten verbreiten. Früh im Kulturverlauf sind solche infizierten Makrophagen hoch „virulent“, das heißt, sie verbreiten sich leicht in Tieren. Nach mehreren Hundert Zellteilungen sinkt jedoch ihre Ausbreitungsfähigkeit stark; sie werden „attenuiert“ und werden sogar als Lebendimpfstoffe genutzt. Da ähnliche Übergänge von aggressiven zu weniger aggressiven Zuständen auch bei menschlichen Krebserkrankungen vorkommen, untersuchten die Autoren, ob Veränderungen in der epigenetischen Landschaft der Zellen — die chemischen Markierungen, die Gene an- oder ausschalten, ohne die DNA-Sequenz zu verändern — dieser Umschaltung zugrunde liegen könnten.
Fokus auf ein mächtiges Gen-Silencing-Zeichen
Die Studie konzentriert sich auf eine spezifische chemische Markierung an Histonproteinen, genannt H3K27me3. Diese Markierung wird von einem Proteinkomplex namens Polycomb Repressive Complex 2 (PRC2) hinzugefügt und ist bekannt dafür, Gene zu unterdrücken, die Zellidentität und Entwicklung steuern. Mithilfe von Chromatin-Immunpräzipitation gefolgt von Sequenzierung (ChIP-seq) kartierten die Autoren, wo H3K27me3 im bovinen Genom in virulenten gegenüber attenuierten, parasiteninfizierten Makrophagen vorkommt. Zum Vergleich kartierten sie auch H3K4me3, eine Markierung, die mit aktiven Genen assoziiert ist. Sie bestätigten, dass ihr Antikörper die Wirtszellform von H3K27me3 erkennt, nicht jedoch die Histone des Parasiten, sodass die Karten Veränderungen in der Kuhzelle und nicht des Mikrobenmaterials widerspiegeln.
Von scharfen Peaks zu breiten stillen Domänen
Die Gesamtmenge an H3K27me3 war in attenuierten Zellen höher, während die aktivierende Markierung H3K4me3 geringer war. Auffälliger als die absoluten Mengen war jedoch die Veränderung im Muster. In virulenten Makrophagen bildete H3K27me3 enge Peaks, zentriert in der Nähe von Transkriptionsstartstellen — eine Konfiguration, die häufig mit präziser, PRC2-getriebener Genregulation verbunden ist. In attenuierten Zellen breitete sich die Markierung aus und bildete breite Domänen, die weit in umliegende Regionen reichten und manchmal viele benachbarte Gene umfassten. Ein anschauliches Beispiel ist das Gen SKAP2, das an der Adhäsion von Makrophagen beteiligt ist: In virulenten Zellen trägt es einen kleinen lokalen H3K27me3-Patch, in attenuierten Zellen liegt es jedoch innerhalb einer >500 Kilobasen großen Domäne dieser repressiven Markierung und ist stark herunterreguliert. Solches Ausbreiten war genomweit häufig und deutet auf ein umfassendes Umbauen der DNA-Verpackung hin, wenn Zellen vom virulenten in den attenuierten Zustand übergehen.
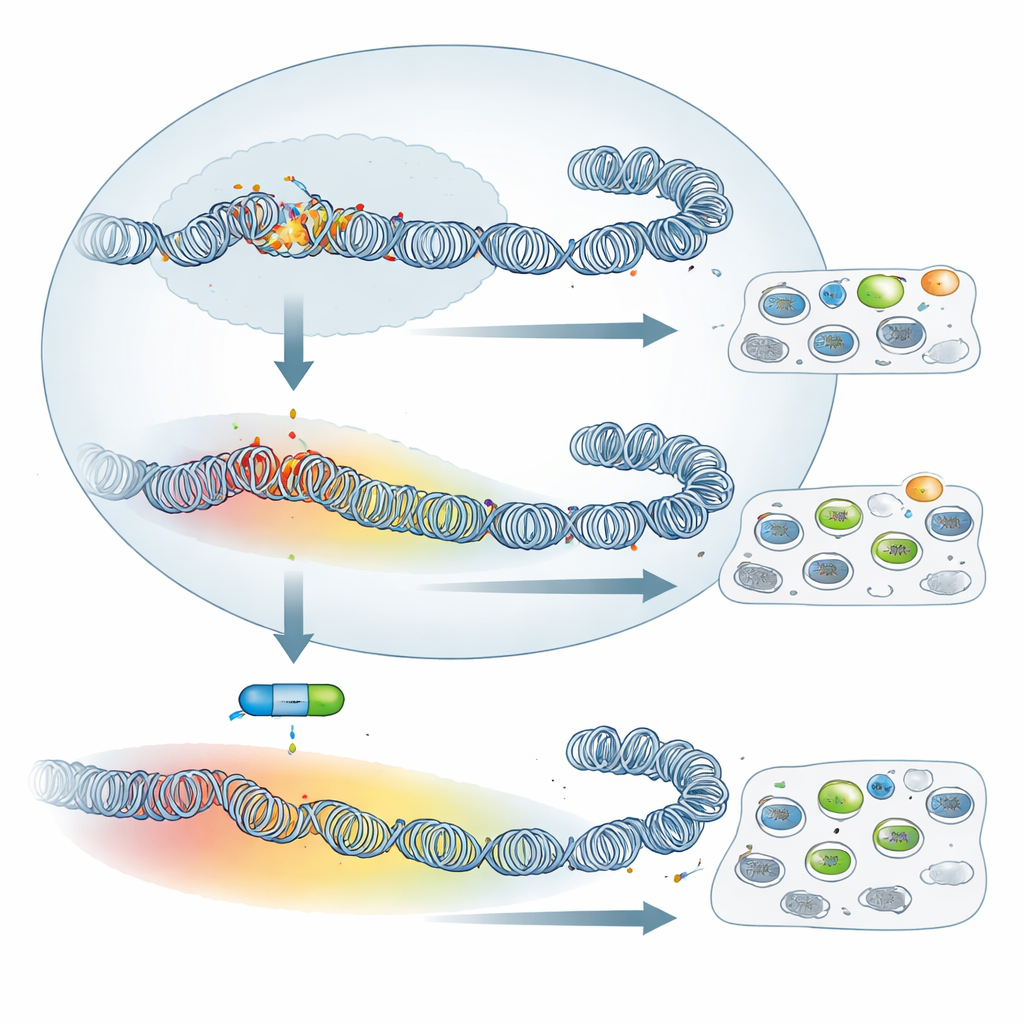
Das Abschalten der Silencing-Maschinerie hat begrenzte Wirkung
Angesichts dieser weitreichenden Umkonfiguration könnte man erwarten, dass das Abschalten von PRC2 — und damit das Entfernen von H3K27me3 — das Verhalten dieser Zellen drastisch ändert. Das Team behandelte sowohl virulente als auch attenuierte Makrophagen mit UNC1999, einem Wirkstoff, der die Enzymaktivität von PRC2 hemmt, und bestätigte, dass H3K27me3 weitgehend verloren ging. Dennoch blieben klassische tumorähnliche Merkmale kaum verändert: Die Fähigkeit der Zellen, an Fibronectin in einer Schale zu haften, und ihre Kapazität, sich in immundefizienten Mäusen auszubreiten, wurden durch das Medikament nicht signifikant beeinträchtigt. Bei der Untersuchung der Genaktivität mittels RNA-Sequenzierung fanden die Autoren, dass in virulenten Zellen deutlich mehr Gene reaktiviert wurden als in attenuierten. Anders ausgedrückt: Obwohl attenuierte Zellen eine breitere H3K27me3-Abdeckung zeigen, hängt ihr Gen-Silencing weniger stark von PRC2 ab. Dennoch wurde eine kleine gemeinsame Gruppe von Genen, darunter bekannte oder vermutete Tumorsuppressoren wie Granzyme A und Follistatin, durch den Inhibitor in beiden Zelltypen wieder aktiviert, was zeigt, dass ein Kernprogramm von PRC2 weiterhin wirkt.
Was das für Krankheit und Therapie bedeutet
Diese Arbeit zeigt, dass sich die epigenetische Landschaft parasite-veränderter Makrophagen tiefgreifend umgestaltet, wenn sie ihre Ausbreitungsfähigkeit verlieren: Eine zentrale Silencing-Markierung breitet sich von scharfen Peaks zu weiten Domänen aus, doch dies führt nicht zu einer einfachen, stärkeren Genabschaltung. Stattdessen ist die globale PRC2-getriebene Repression in attenuierten Zellen gedämpft, während eine Untergruppe wichtiger Gene weiterhin auf diese Maschinerie angewiesen ist, um ausgeschaltet zu bleiben. Für die Tiergesundheit deuten die Ergebnisse darauf hin, dass die alleinige Zielrichtung auf PRC2 wenig erfolgversprechend sein dürfte, um Theileria-induzierte Tumoren bei Tieren zu kontrollieren. Allgemeiner verdeutlicht die Studie, wie eine Infektion Wirtszellen in krebsähnliche epigenetische Zustände treiben kann und wie dramatische Veränderungen in der Chromatinstruktur nicht immer klaren funktionalen Folgen entsprechen. Das Verständnis dieser feinen epigenetischen Verschiebungen könnte helfen, künftige Strategien zur Feinabstimmung der Genregulation sowohl bei Infektionskrankheiten als auch bei Krebs zu verfeinern.
Zitation: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
Schlüsselwörter: Epigenetik, Theileria, Makrophagen, Histonmodifikation, PRC2