Clear Sky Science · ru
Эпигенетический ландшафт метки H3K27me3 в макрофагах, трансформированных Theileria annulata
Почему паразит крупного рогатого скота важен для изучения рака
Тропическая теилериоз — тяжелое заболевание крупного рогатого скота, вызываемое паразитом Theileria annulata, передающимся через клещей. Попав в организм, паразит превращает определенные лейкоциты в бесконечно делящиеся, подвижные клетки, которые по поведению очень похожи на раковые. Эти трансформированные клетки распространяются по организму и инициируют болезнь. Интригует тот факт, что при длительном культивировании такие инфицированные клетки постепенно теряют способность к распространению. В статье поставлен простой, но далеко идущий вопрос: какие изменения в упаковке ДНК хозяина сопровождают эту потерю агрессивности и что это может рассказать нам о ракообразном росте в целом?
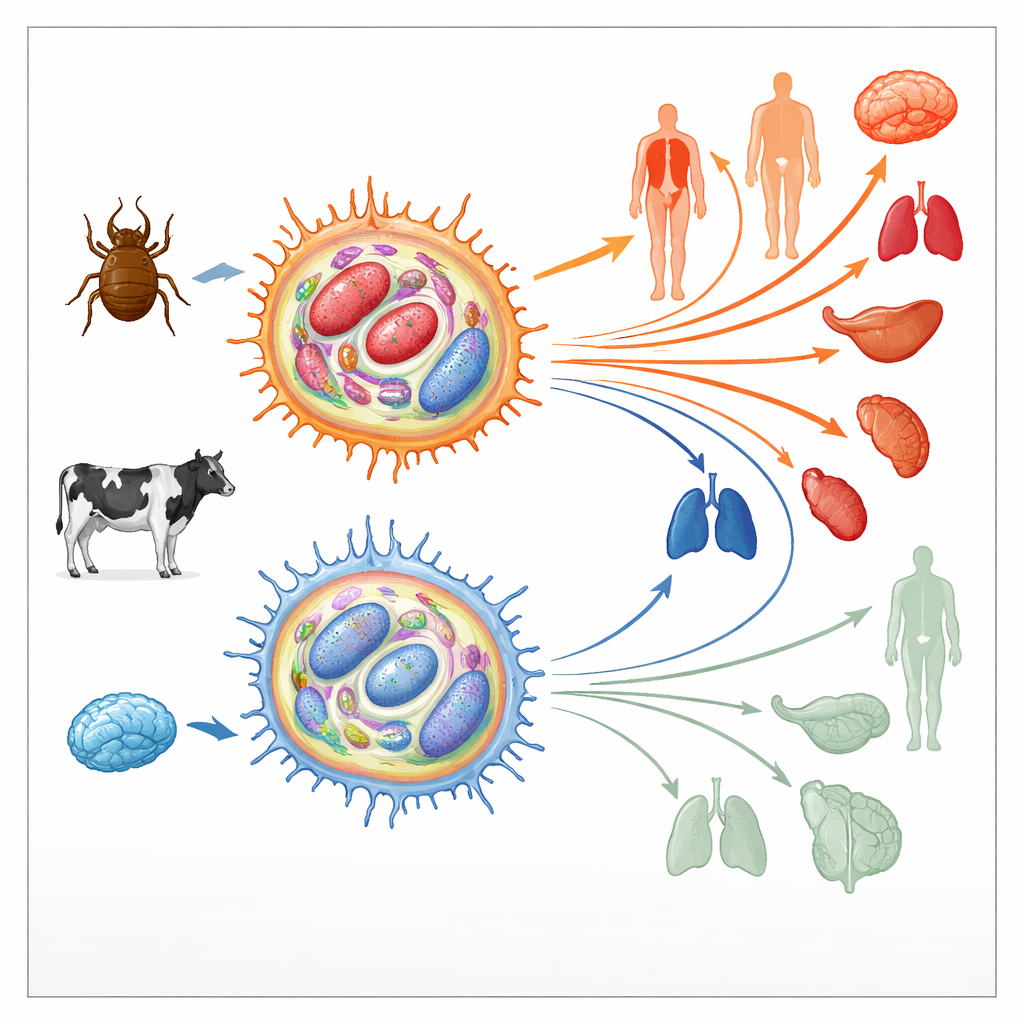
Как паразит перенастраивает иммунные клетки хозяина
Theileria annulata живет внутри бычьих иммунных клеток — макрофагов. Там он вмешивается в ключевые сигнальные пути, которые обычно контролируют гибель, деление и движение клеток, подталкивая клетку хозяина в состояние, напоминающее опухоль. Такие захваченные клетки способны бесконтрольно делиться и мигрировать по тканям, распространяя паразита. В начале культивирования инфицированные макрофаги очень «вирулентны», то есть легко диссеминируют в живом животном. Однако после сотен делений их способность к распространению резко падает; они становятся «аттенуированными» и даже используются как живые вакцины. Поскольку аналогичные переходы от агрессивного к менее агрессивному состоянию наблюдаются и при человеческих раках, авторы проверили, не лежат ли в основе этого переключения изменения эпигенетического ландшафта — химических меток, которые помогают включать или выключать гены без изменения последовательности ДНК.
Фокус на мощной метке выключения генов
Исследование сосредоточено на конкретной химической метке в белках гистонов — H3K27me3. Эту метку наносит белковый комплекс, известный как Polycomb Repressive Complex 2 (PRC2), и она прославлена способностью выключать гены, регулирующие идентичность клеток и развитие. С помощью хроматин-иммунопреципитации с последующим секвенированием (ChIP-seq) авторы картировали, где именно располагается H3K27me3 по всему геному быка в вирулентных и аттенуированных инфицированных макрофагах. Для сравнения они также картировали H3K4me3 — метку, связанную с активными генами. Они подтвердили, что их антитело распознает версию H3K27me3 клетки хозяина, но не гистоны самого паразита, поэтому карты отражают изменения в клетке крупного рогатого скота, а не в микроорганизме.
От узких пиков к широким молчаливым доменам
Общее количество H3K27me3 было выше в аттенуированных клетках, тогда как активирующая метка H3K4me3 — ниже. Однако более примечательным, чем суммарные уровни, оказалось изменение в паттерне распределения метки. В вирулентных макрофагах H3K27me3 образовывала узкие пики, сосредоточенные около сайтов начала транскрипции генов — конфигурация, часто связанная с точным контролем генов, опосредованным PRC2. В аттенуированных клетках метка распространялась, образуя широкие домены, которые простирались далеко в прилегающие регионы и иногда покрывали многочисленные соседние гены. Наглядный пример — ген SKAP2, участвующий в адгезии макрофагов: в вирулентных клетках он несет небольшой локальный участок H3K27me3, а в аттенуированных оказывается внутри домена репрессии >500 килобаз и сильно подавлен. По всему геному такое распространение было распространенным, что свидетельствует о масштабном ремоделировании упаковки ДНК при переходе клеток от вирулентного к аттенуированному состоянию.
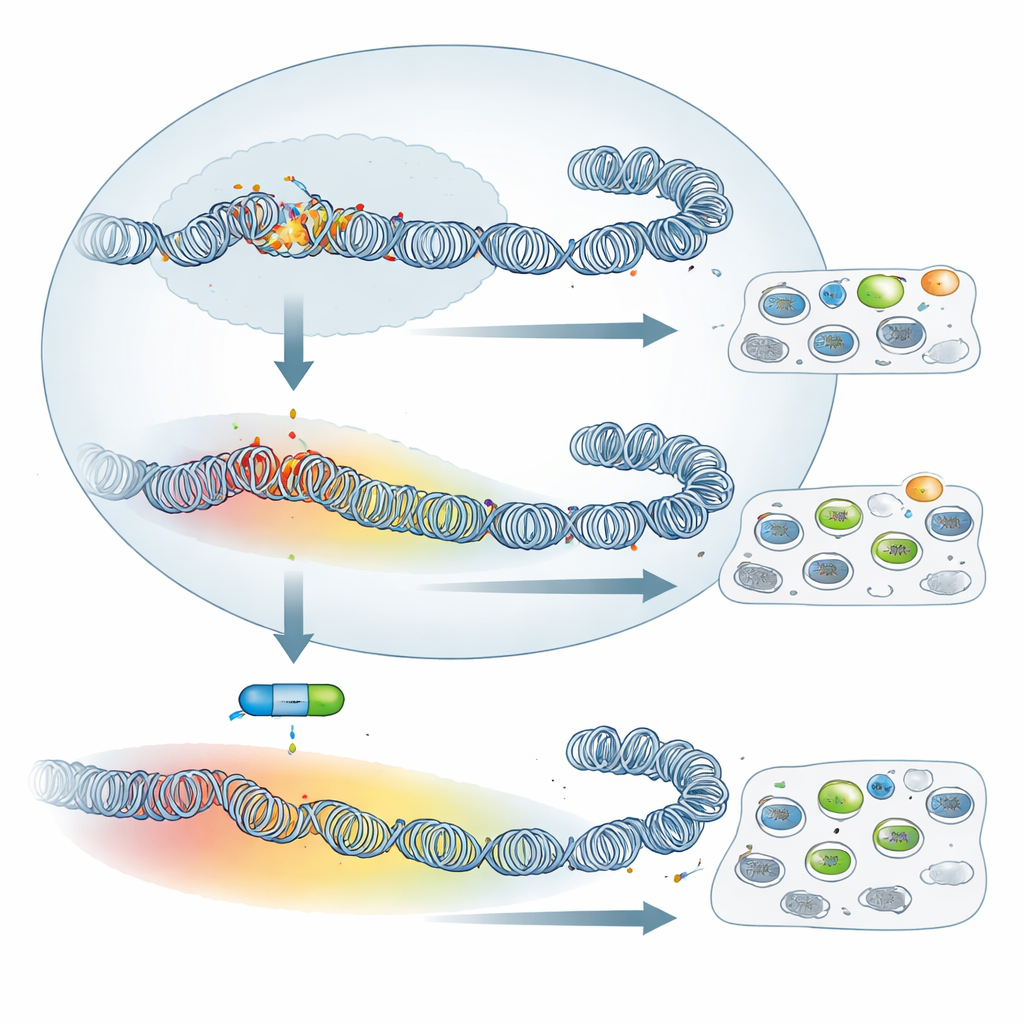
Блокирование механизма молчания дает ограниченный эффект
Учитывая такое масштабное перестроение, можно было ожидать, что выключение PRC2 — и, следовательно, стирание H3K27me3 — кардинально изменит поведение этих клеток. Команда обработала вирулентные и аттенуированные макрофаги UNC1999 — препаратом, ингибирующим ферментативную активность PRC2 — и подтвердила, что H3K27me3 в значительной степени исчезла. Тем не менее классические опухолевоподобные признаки практически не изменились: способность клеток прикрепляться к фибронектину в чашке и их потенциал к диссеминации у иммунодефицитных мышей существенно не пострадали от действия препарата. При исследовании транскрипции методом РНК‑секвенирования авторы обнаружили, что гораздо больше генов реактивируется в вирулентных, чем в аттенуированных клетках. Иными словами, хотя у аттенуированных клеток H3K27me3 покрывает более широкие участки, их генетическое подавление в меньшей степени зависит от PRC2. Тем не менее небольшая общая группа генов, включающая известные или предполагаемые супрессоры опухолей, такие как гранзим A и фоллистатин, была вновь активирована ингибитором в обеих популяциях, что показывает, что ядро программы PRC2 сохраняется.
Что это значит для болезни и лечения
Работа показывает, что по мере того как паразит‑трансформированные макрофаги теряют способность распространяться, их эпигенетический ландшафт претерпевает глубокие изменения: ключевая метка репрессии распространяется от узких пиков в широкие домены, но это не выливается в простое и однозначное усиление подавления генов. Скорее глобальная PRC2‑опосредованная репрессия ослаблена в аттенуированных клетках, тогда как подмножество важных генов по‑прежнему требует этого механизма, чтобы оставаться выключенными. Для здравоохранения животных результаты указывают на то, что таргетирование только PRC2 вряд ли будет эффективным способом контроля опухолей, вызванных Theileria, у скота. В более широком контексте исследование иллюстрирует, как инфекция может переводить клетки хозяина в эпигенетические состояния, сходные с раковыми, и как драматические изменения в структуре хроматина не всегда имеют простые функциональные последствия. Понимание этих тонких эпигенетических сдвигов может помочь уточнить будущие стратегии, направленные на корректировку регуляции генов как в инфекционных заболеваниях, так и при раке.
Цитирование: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
Ключевые слова: эпигенетика, Theileria, макрофаги, модификация гистонов, PRC2