Clear Sky Science · nl
Epigenetisch landschap van de H3K27me3-markering in door Theileria annulata getransformeerde macrofagen
Waarom een rundparasiet van belang is voor kankerbiologie
Tropische theileriose is een ernstige ziekte bij runderen veroorzaakt door de parasiet Theileria annulata, overgedragen door teken. Eenmaal in het dier verandert de parasiet bepaalde witte bloedcellen in eindeloos delende, mobiel wordende cellen die sterk op kankerachtig gedrag lijken. Deze getransformeerde cellen verspreiden zich door het lichaam en veroorzaken ziekte. Intrigerend genoeg verliezen zulke geïnfecteerde cellen, als ze lange tijd in het laboratorium worden gekweekt, geleidelijk hun vermogen om zich te verspreiden. Dit artikel stelt een eenvoudige maar verstrekkende vraag: welke veranderingen in de DNA‑verpakking van de geïnfecteerde cellen gaan gepaard met dit verlies aan agressiviteit, en wat leert dat ons over kankerachtig celgedrag in het algemeen?
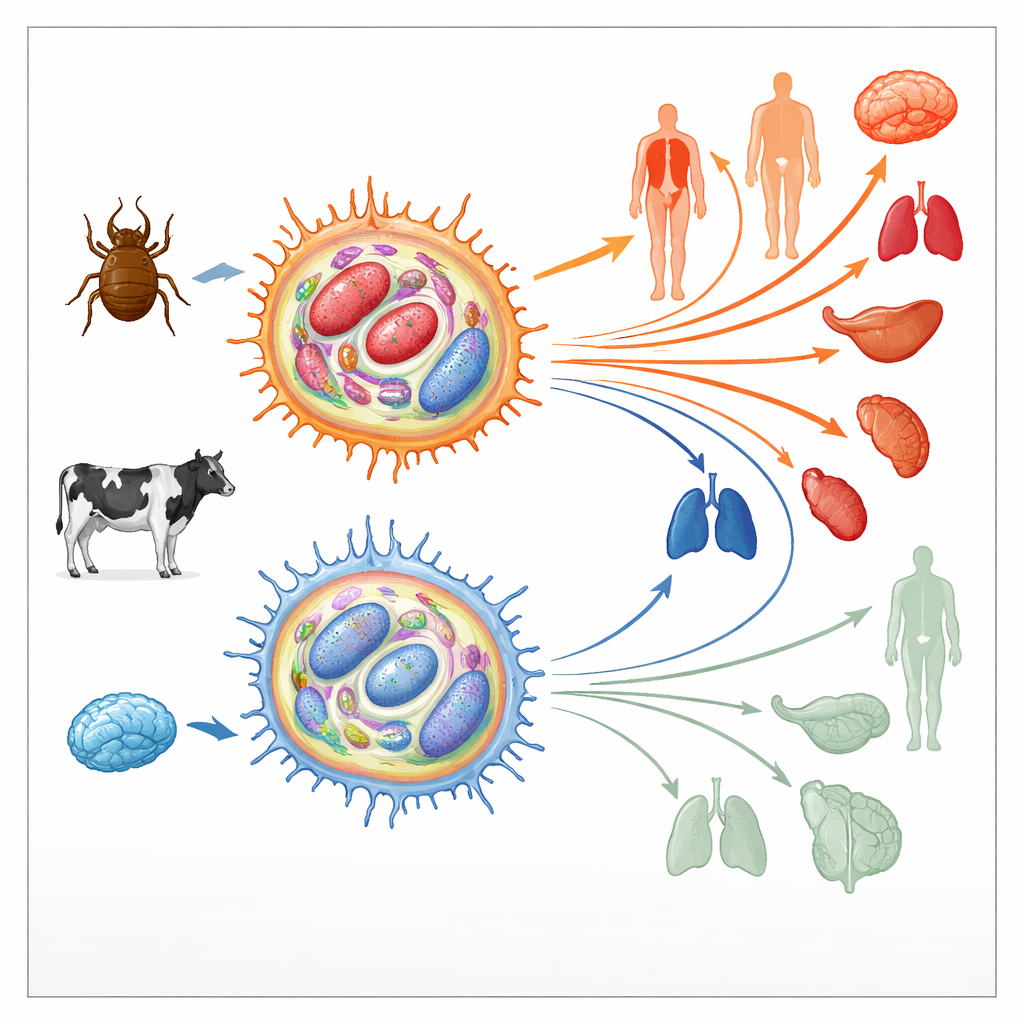
Hoe de parasiet de gastheercellen herprogrammeren
Theileria annulata leeft binnenin boviene immuuncellen die macrofagen worden genoemd. Daar manipuleert hij sleutelroutes die normaal gesproken celdood, celdeling en beweging reguleren, en duwt de gastheercel in een tumorachtige toestand. Deze gekaapte cellen kunnen vervolgens onbeperkt delen en door weefsels migreren, waarmee ze de parasiet verspreiden. In vroege cultuur zijn zulke geïnfecteerde macrofagen zeer “virulent”, wat betekent dat ze zich gemakkelijk in dieren verspreiden. Na honderden celdelingen neemt hun verspreidingsvermogen echter scherp af; ze worden “geattenteerd” en worden zelfs gebruikt als levende vaccins. Omdat vergelijkbare overgangen van agressieve naar minder agressieve toestanden ook bij menselijke kankers voorkomen, onderzochten de auteurs of veranderingen in het epigenetische landschap—de chemische merktekens die genen aan- of uitzetten zonder de DNA‑sequentie te wijzigen—aan deze omschakeling ten grondslag kunnen liggen.
Focussen op een krachtig gen‑onderdrukkend merkteken
De studie zoomt in op een specifiek chemisch label op histon‑eiwitten, genaamd H3K27me3. Dit label wordt toegevoegd door een eiwitcomplex dat bekendstaat als Polycomb Repressive Complex 2 (PRC2) en is berucht vanwege het afsluiten van genen die celidentiteit en ontwikkeling reguleren. Met chromatine immunoprecipitatie gevolgd door sequencing (ChIP‑seq) brachten de auteurs in kaart waar H3K27me3 in het boviene genoom zit in virulente versus geattendeerde, door de parasiet geïnfecteerde macrofagen. Ze brachten ook H3K4me3 in kaart, een merkteken dat geassocieerd is met actieve genen, ter vergelijking. Ze bevestigden dat hun antilichaam de gastheercelversie van H3K27me3 detecteert maar niet de histonen van de parasiet, zodat de kaarten veranderingen in de rundencel weergeven en niet van de microbe.
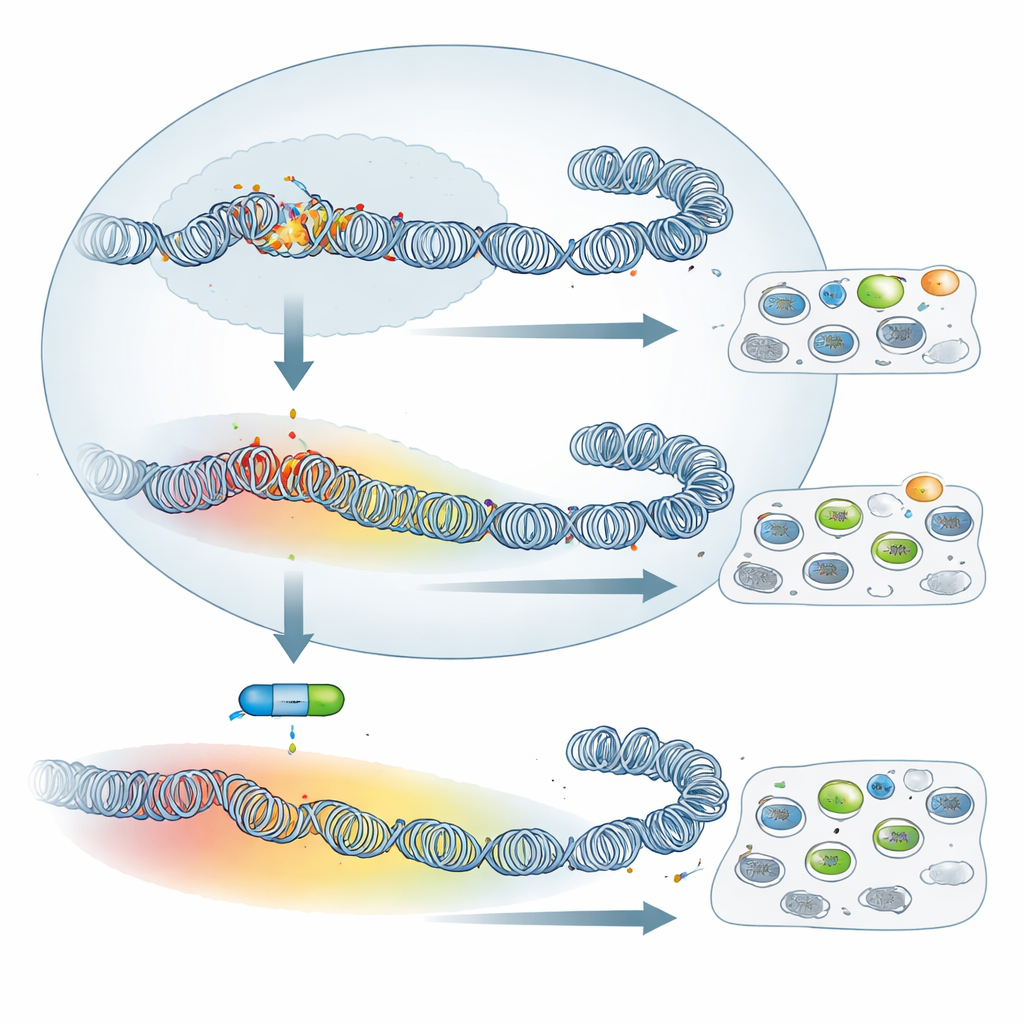
Van scherpe pieken naar brede stille domeinen
De totale hoeveelheid H3K27me3 was hoger in geattendeerde cellen, terwijl het activerende merkteken H3K4me3 lager was. Meer opvallend dan de absolute niveaus was echter de patroonverandering. In virulente macrofagen vormde H3K27me3 smalle pieken gecentreerd nabij genstartplaatsen, een configuratie die vaak gekoppeld is aan precieze, PRC2‑gedreven gencontrole. In geattendeerde cellen verspreidde het merkteken zich en vormde brede domeinen die ver in de omliggende regio’s reikten, soms vele naburige genen omvattend. Een treffend voorbeeld is het SKAP2‑gen, betrokken bij macrophage‑hechting: in virulente cellen draagt het een klein lokaal stukje H3K27me3, maar in geattendeerde cellen ligt het binnen een >500 kilobase domein van dit repressieve merkteken en is het sterk naar beneden gereguleerd. Door het hele genoom heen kwam dergelijke verspreiding veel voor, wat wijst op een ingrijpende herinrichting van de DNA‑verpakking naarmate cellen verschuiven van virulent naar geattendeerd gedrag.
Het blokkeren van het onderdrukkingsmachinerie heeft beperkte gevolgen
Gezien deze ingrijpende herconfiguratie zou je verwachten dat het uitschakelen van PRC2—en dus het wissen van H3K27me3—dramatisch het gedrag van deze cellen verandert. Het team behandelde zowel virulente als geattendeerde macrofagen met UNC1999, een middel dat de enzymatische activiteit van PRC2 remt, en verifieerde dat H3K27me3 grotendeels verdween. Toch veranderden klassieke tumorachtige eigenschappen nauwelijks: het vermogen van de cellen om in een schaaltje aan fibronectine te hechten en hun capaciteit om zich te verspreiden in immuundeficiënte muizen werden door het middel niet significant beïnvloed. Toen de auteurs de genactiviteit bekeken met RNA‑sequencing, vonden ze dat veel meer genen werden heractiveerd in virulente dan in geattendeerde cellen. Met andere woorden: hoewel geattendeerde cellen bredere H3K27me3‑bedekking hebben, hangt hun gendemping minder van PRC2 af. Toch werd een kleine gedeelde groep genen, waaronder bekende of vermoedelijke tumorsuppressoren zoals Granzyme A en Follistatin, door de remmer in beide celtypen weer tot expressie gebracht, wat aantoont dat een kernprogramma van PRC2 intact blijft.
Wat dit betekent voor ziekte en behandeling
Dit werk laat zien dat wanneer door de parasiet getransformeerde macrofagen hun vermogen tot verspreiding verliezen, hun epigenetische landschap ingrijpend wordt herschapen: een belangrijk repressief merkteken breidt zich uit van scherpe pieken tot brede domeinen, maar dit vertaalt zich niet in een eenvoudige, sterkere genonderdrukking. In plaats daarvan is de globale PRC2‑gedreven repressie in geattendeerde cellen afgezwakt, terwijl een subset van cruciale genen nog steeds op dit mechanisme vertrouwt om uitgeschakeld te blijven. Voor de gezondheid van vee suggereren de bevindingen dat het richten op PRC2 alleen waarschijnlijk geen effectieve manier is om door Theileria geïnduceerde tumoren bij dieren te beheersen. Breder gezien illustreert de studie hoe infectie gastheercellen door ziekte‑achtige epigenetische toestanden kan duwen en hoe dramatische veranderingen in chromatinestructuur niet altijd eenduidige functionele gevolgen hebben. Het begrijpen van deze subtiele epigenetische verschuivingen kan helpen toekomstige strategieën te verfijnen die gericht zijn op het bijsturen van genregulatie in zowel infectieziekten als kanker.
Bronvermelding: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
Trefwoorden: epigenetica, Theileria, macrofagen, histonmodificatie, PRC2