Clear Sky Science · ar
المشهد فوق الجيني لعلامة H3K27me3 في البلغميات المتحوِّلة بواسطة Theileria annulata
لماذا يهم طفيلي الأبقار علم الأورام
الثيلية المدارية مرض شديد لدى الأبقار تسببه الطفيلي Theileria annulata وينقله القراد. بعد دخوله الحيوان، يحول الطفيلي خلايا دم بيضاء معينة إلى خلايا متسلسلة الانقسام وقادرة على الحركة تَشبه إلى حد كبير الخلايا السرطانية. تنتشر هذه الخلايا المتحوِّلة في أنحاء الجسم وتسبب المرض. ومن المثير للاهتمام أنه عندما تُزرع هذه الخلايا المصابة في المختبر لفترات طويلة، تفقد تدريجياً قدرتها على الانتشار. تسأل هذه الورقة سؤالاً بسيطاً لكنه ذو آثار بعيدة: ما التغيرات في تغليف الحمض النووي للخلايا المصابة التي ترافق فقدان العدوانية هذا، وماذا تعلمنا عن نموٍ شبيه بالسرطان بصورة أعم؟
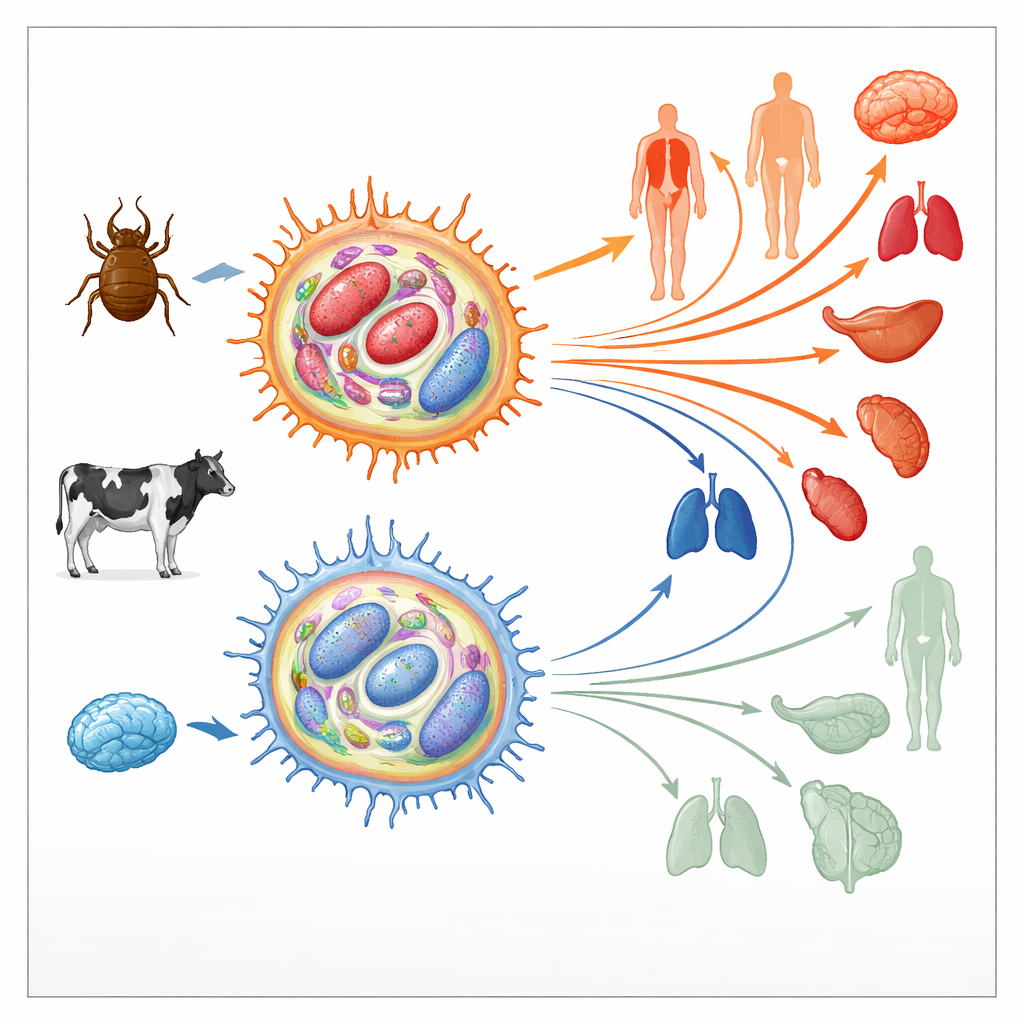
كيف يعيد الطفيلي تهيئة خلايا الجهاز المناعي للمضيف
يعيش Theileria annulata داخل خلايا مناعية بقرية تُسمى البلعميات. هناك يتلاعب بمسارات إشارية أساسية تتحكم عادة في موت الخلية وانقسامها وحركتها، ويدفع الخلية المضيفة إلى حالة شبيهة بالورم. يمكن لهذه الخلايا المغتصَبة أن تنقسم بلا حدود وتهاجر عبر الأنسجة، ناشرة الطفيلي. في المراحل المبكرة من الزراعة، تكون هذه البلعميات المصابة شديدة «الفتك»، أي أنها تنتشر بسهولة في الحيوانات. لكن بعد مئات الانقسامات الخلوية، تنخفض قدرتها على الانتشار بصورة حادة؛ فتُصبح «مخفَّفة» وتُستخدم أحياناً كلقاحات حية. وبما أن انتقالات مماثلة من حالات عدوانية إلى حالات أقل عدوانية تحدث في السرطانات البشرية، فحص المؤلفون ما إذا كانت التغيرات في المشهد فوق الجيني للخلايا — العلامات الكيميائية التي تساعد على تشغيل أو إطفاء الجينات دون تغيير تسلسل الحمض النووي — قد تكون وراء هذا التحول.
التركيز على علامة قوية لكبت الجين
تتعمق الدراسة في وسم كيميائي محدد على بروتينات الهستون تُدعى H3K27me3. تُضاف هذه العلامة بواسطة مركب بروتيني يُعرف بمجمع القمع البوليكوم (PRC2) وهي مشهورة بإخماد الجينات التي تتحكم في هوية الخلايا والتطوّر. باستخدام مناعية الكروماتين متبوعة بالتسلسل (ChIP-seq)، رسم المؤلفون خرائط لمواضع H3K27me3 عبر الجينوم البقري في البلعميات الفتاكة مقابل المخففة المصابة بالطفيلي. كما رسموا أيضاً H3K4me3، علامة مرتبطة بالجينات النشطة، للمقارنة. وأكدوا أن مستضداتهم تكشف نسخة الخلية المضيفة من H3K27me3 وليس هستونات الطفيلي، لذلك تعكس الخرائط تغيّرات في خلية البقرة لا في الميكروب.
من قمم حادة إلى نطاقات صامتة واسعة
كان مقدار H3K27me3 الإجمالي أعلى في الخلايا المخففة، بينما كانت علامة التفعيل H3K4me3 أدنى. وأكثر إثارة للاهتمام من المستويات الكلية كان التغير في النمط. في البلعميات الفتاكة، شكّلت H3K27me3 قممًا ضيقة متمركزة قرب مواقع بدء الجينات، وهو تكوين غالبًا ما يرتبط بتحكم دقيق يقوده PRC2. في الخلايا المخففة، امتدّت العلامة مشكلة نطاقات واسعة تسرّبت إلى المناطق المحيطة، وأحيانًا غطت العديد من الجينات المجاورة. مثال واضح هو جين SKAP2، المتورط في التصاق البلعميات: في الخلايا الفتاكة يحمل رقعة محلية صغيرة من H3K27me3، أما في الخلايا المخففة فيقع داخل نطاق قمعي يزيد على 500 كيلوبايت ويُخمد بشدّة. عبر الجينوم، كان مثل هذا الامتداد شائعًا، مشيرًا إلى إعادة تشكيل شاملة لكيفية تغليف الحمض النووي أثناء تحول الخلايا من سلوك فتّاكي إلى مخفف.
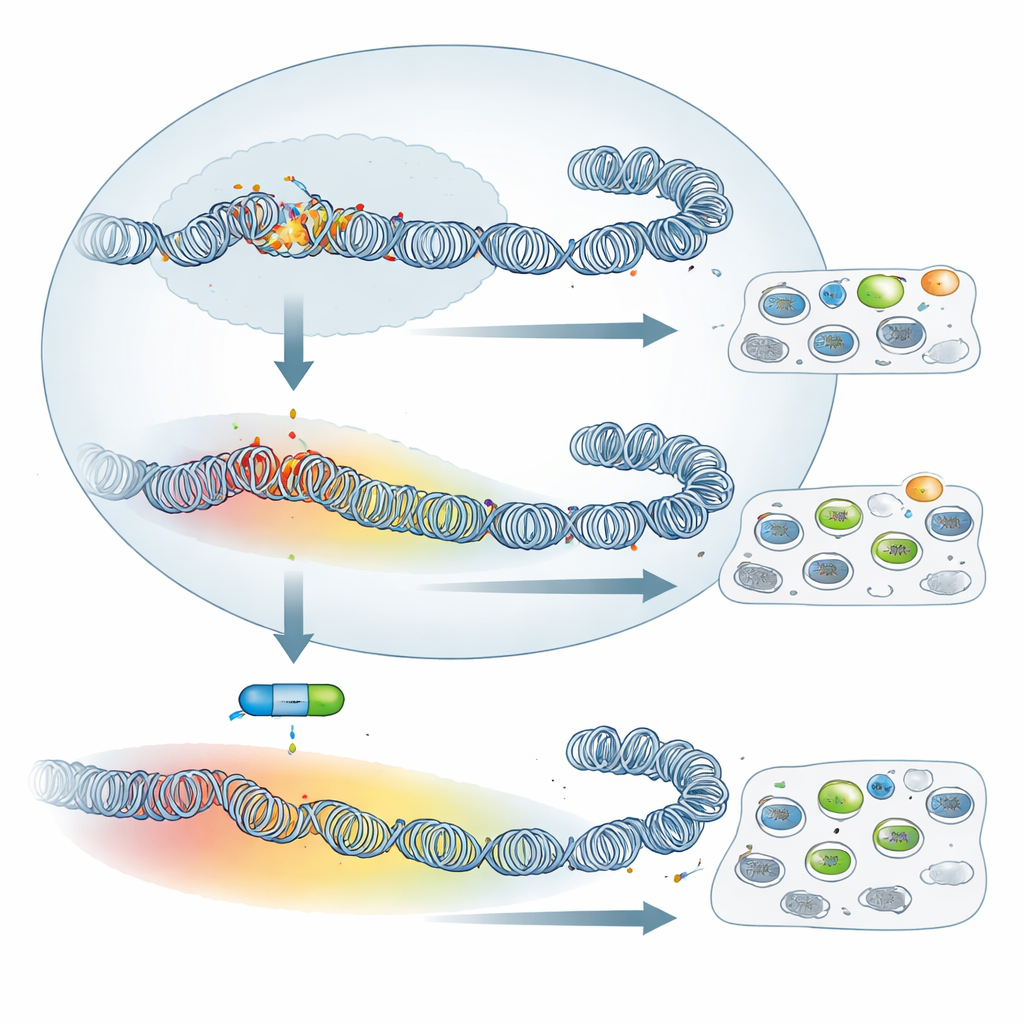
حجب آلية الكبت له تأثير محدود
بالنظر إلى هذا إعادة التشكيل الواسع، قد يتوقع المرء أن إيقاف PRC2 — وبالتالي محو H3K27me3 — سيغير سلوك هذه الخلايا بصورة درامية. عالج الفريق كلًا من البلعميات الفتاكة والمخففة بمثبِّط UNC1999، دواء يثبط نشاط إنزيم PRC2، وتحققوا من أن H3K27me3 فقدت إلى حد كبير. ومع ذلك، لم تتغير الصفات الورمية الكلاسيكية تقريبًا: قدرة الخلايا على الالتصاق بالفبرونيكتين في الصحن، وقدرتها على الانتشار في الفئران ذات المناعة الضعيفة، لم تتأثر بشكل كبير بالدواء. وعندما فحص المؤلفون نشاط الجينات بواسطة تسلسل الرنا، وجدوا أن عدداً أكبر من الجينات أعيد تنشيطه في الخلايا الفتاكة مقارنة بالمخففة. بعبارة أخرى، رغم أن الخلايا المخففة تملك تغطية أوسع لـ H3K27me3، فإن كبتها للجينات يعتمد بشكل أقل على PRC2. ومع ذلك، أعيد تنشيط مجموعة صغيرة مشتركة من الجينات، بما في ذلك مثبطات أورام معروفة أو مشتبه بها مثل الغرانزيم A والفوليستاتين، بواسطة المثبط في كلا نوعي الخلايا، مما يبيّن أن برنامج PRC2 الأساسي لا يزال قائمًا.
ماذا يعني هذا للمرض والعلاج
تكشف هذه الدراسة أنه عندما تفقد البلعميات المتحوِّلة بالطفيلي قدرتها على الانتشار، يُعاد تشكيل مشهدها فوق الجيني بعمق: تنتشر علامة كبت رئيسية من قمم حادة إلى نطاقات واسعة، ومع ذلك لا يترجم ذلك إلى إغلاق أبسط أو أقوى للجينات. بدلًا من ذلك، يُضعف الكبت العام المدفوع بـ PRC2 في الخلايا المخففة، بينما تظل مجموعة فرعية من الجينات الحيوية معتمدة على هذه الآلية للبقاء مطفأة. بالنسبة لصحة الماشية، تشير النتائج إلى أن استهداف PRC2 وحده من غير المرجح أن يكون وسيلة فعالة للسيطرة على الأورام الناتجة عن Theileria في الحيوانات. وعلى نطاق أوسع، تبيّن الدراسة كيف يمكن أن يدفع العدوى خلايا المضيف إلى حالات فوق جينية شبيهة بالسرطان، وكيف أن التغيرات الدراماتيكية في بنية الكروماتين لا تقود دائمًا إلى نتائج وظيفية بسيطة ومباشرة. قد يساعد فهم هذه التحولات الفوق جينية الدقيقة في صقل استراتيجيات مستقبلية تهدف إلى تعديل تنظيم الجينات في كلٍّ من الأمراض المعدية والسرطان.
الاستشهاد: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
الكلمات المفتاحية: فوق جينية, ثيليريا, البلعميات, تعديل هستوني, PRC2