Clear Sky Science · sv
Epigenetiskt landskap för H3K27me3-marken i makrofager omvandlade av Theileria annulata
Varför en parasit hos nötkreatur är viktig för cancerforskning
Tropisk theilerios är en svår sjukdom hos nötkreatur som orsakas av parasiten Theileria annulata, som sprids via fästingar. När parasiten väl tagit sig in i djuret förvandlar den vissa vita blodkroppar till oändligt delande, mobiliserade celler som beter sig mycket likt cancer. Dessa omvandlade celler sprider sig i hela kroppen och driver sjukdomen. Intressant nog förlorar sådana infekterade celler gradvis sin spridningsförmåga när de odlas länge i labb. Denna artikel ställer en enkel men långtgående fråga: vilka förändringar i de infekterade cellernas DNA-packning följer denna minskning i aggressivitet, och vad lär det oss mer allmänt om cancerliknande tillväxt?
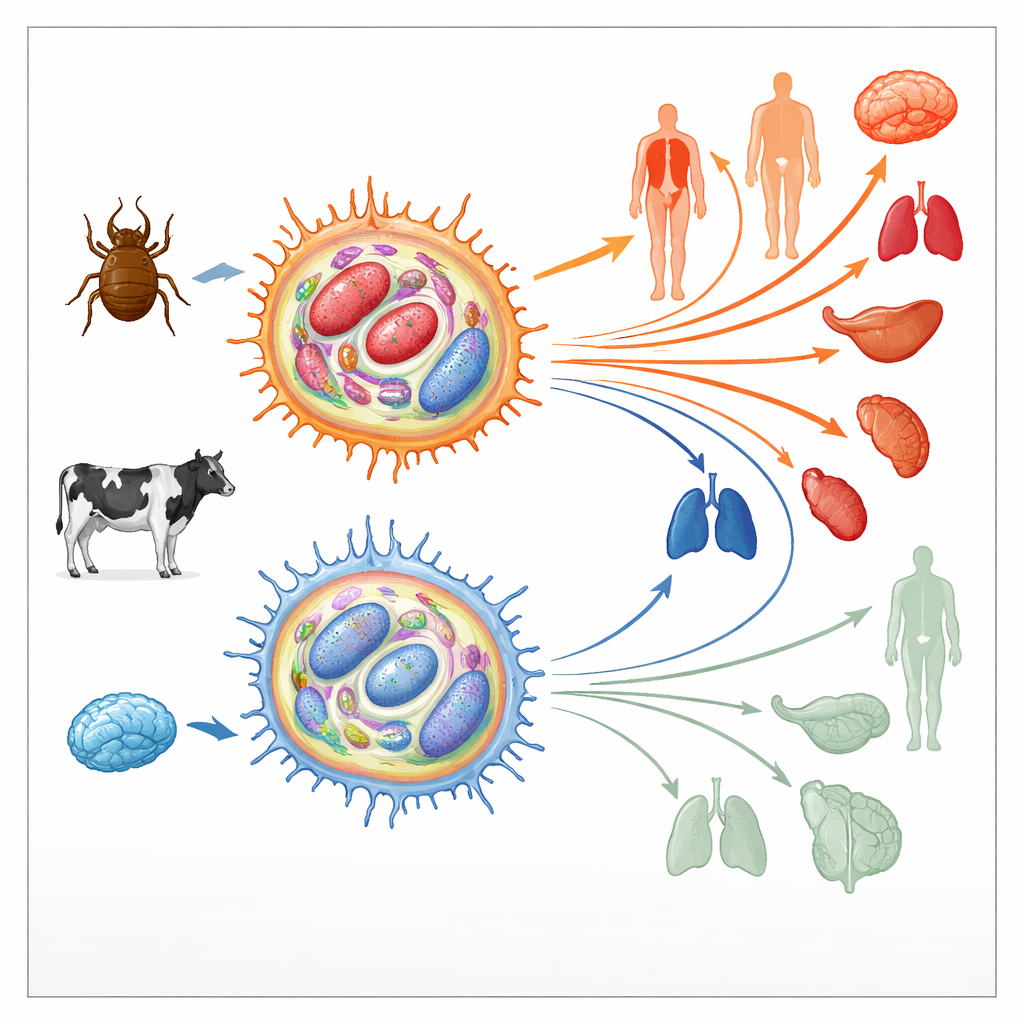
Hur parasiten ombygger värdcellernas immunsvar
Theileria annulata lever inuti bovina immunceller som kallas makrofager. Där manipulerar den centrala signalvägar som normalt styr celldöd, celldelning och rörelse, och pressar värdcellen in i ett tumörliknande tillstånd. Dessa kapade celler kan därefter dela sig obegränsat och migrera genom vävnader och sprida parasiten. Tidigt i odling är sådana infekterade makrofager mycket “virulenta”, det vill säga de sprider sig lätt i djur. Efter hundratals celldelningar sjunker dock deras spridningsförmåga kraftigt; de blir ”attenuerade” och används till och med som levande vaccin. Eftersom liknande övergångar från aggressiva till mindre aggressiva tillstånd förekommer i människocancer, undersökte författarna om förändringar i cellernas epigenetiska landskap — de kemiska märken som hjälper till att slå på eller av gener utan att ändra DNA-sekvensen — kan ligga bakom denna växling.
Fokus på en kraftfull genstängande markör
Studien zoomar in på en specifik kemisk etikett på histonproteiner, kallad H3K27me3. Denna etikett sätts dit av ett proteinkomplex känt som Polycomb Repressive Complex 2 (PRC2) och är känt för att stänga av gener som kontrollerar cellidentitet och utveckling. Med kromatinimmunoprecipitering följt av sekvensering (ChIP-seq) kartlade författarna var H3K27me3 finns över det bovina genomet i virulenta respektive attenuerade, parasitinfekterade makrofager. De kartlade också H3K4me3, en markör kopplad till aktiva gener, för jämförelse. De bekräftade att deras antikropp detekterar värdcellens version av H3K27me3 men inte parasitens egna histoner, så kartorna speglar förändringar i nötkreaturscellen snarare än mikroben.
Från skarpa toppar till breda tysta domäner
Den totala mängden H3K27me3 var högre i attenuerade celler, medan den aktiverande marken H3K4me3 var lägre. Mer slående än totalnivåerna var dock förändringen i mönster. I virulenta makrofager bildade H3K27me3 smala toppar centrerade nära genstartsplatser, en konfiguration som ofta kopplas till precis, PRC2-driven genreglering. I attenuerade celler spred sig märket och bildade breda domäner som sträckte sig långt ut i omgivande områden och ibland täckte många närliggande gener. Ett tydligt exempel är SKAP2-genen, involverad i makrofagadhesion: i virulenta celler bär den en liten lokal fläck av H3K27me3, men i attenuerade celler ligger den inom en >500 kilobas stor domän av denna repressiva mark och är starkt nedreglerad. Över genomet var sådan utbredning vanlig, vilket tyder på en genomgripande ommodellering av hur DNA packas när celler skiftar från virulent till attenuerat beteende.
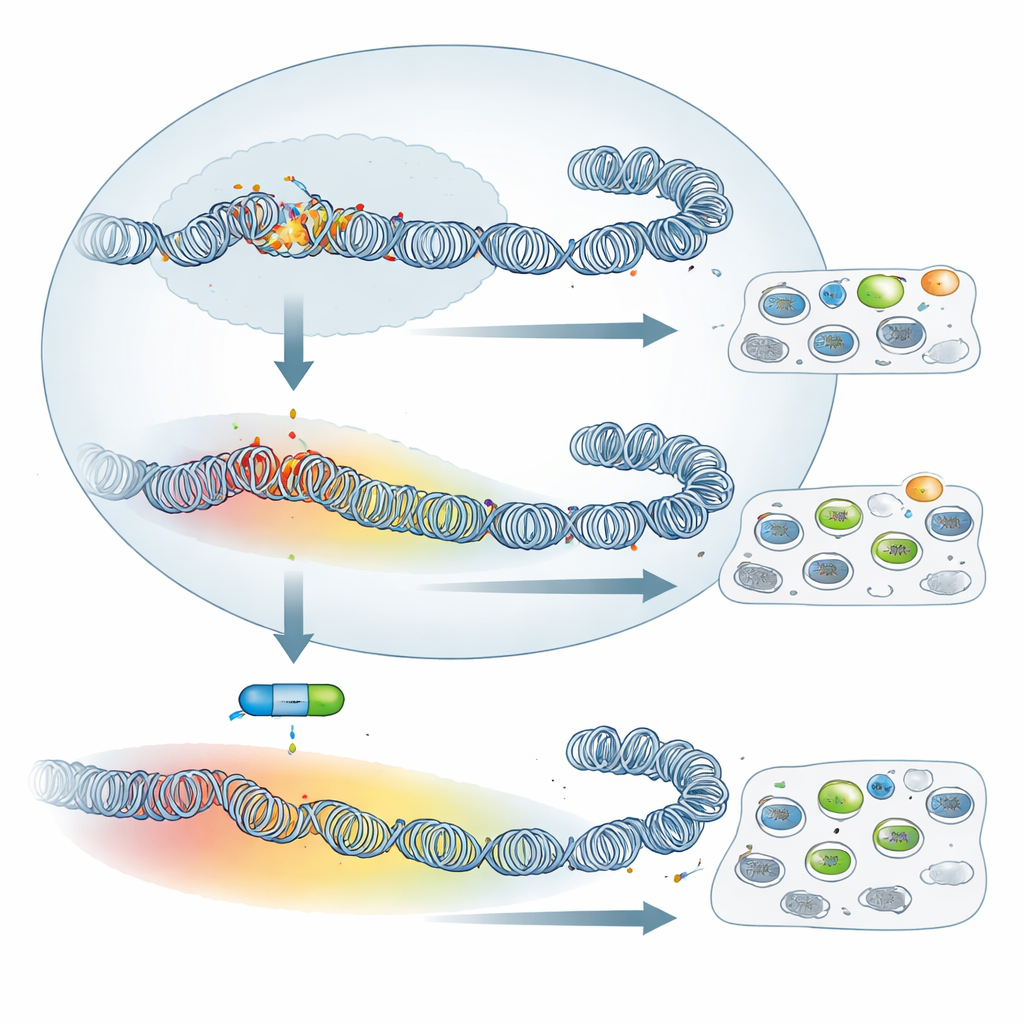
Blockering av det stängande maskineriet har begränsad effekt
Givet denna omfattande omkonfiguration skulle man kunna förvänta sig att stänga av PRC2 — och därmed radera H3K27me3 — skulle förändra cellernas beteende dramatiskt. Forskargruppen behandlade både virulenta och attenuerade makrofager med UNC1999, ett läkemedel som hämmar PRC2:s enzymatiska aktivitet, och verifierade att H3K27me3 i stor utsträckning försvann. Ändå förändrades de klassiska tumörlika egenskaperna knappt: cellernas förmåga att fästa vid fibronectin på en odlingsplatta och deras kapacitet att spridas i immunsupprimerade möss påverkades inte signifikant av läkemedlet. När författarna granskade genaktivitet med RNA-sekvensering fann de att många fler gener återaktiverades i virulenta än i attenuerade celler. Med andra ord, även om attenuerade celler har bredare H3K27me3-täckning, beror deras genstängning i mindre utsträckning på PRC2. Fortfarande återaktiverades en liten gemensam grupp gener, inklusive kända eller misstänkta tumörsuppressorer såsom Granzyme A och Follistatin, av hämmaren i båda celltyperna, vilket visar att ett kärn-PRC2-program är bevarat.
Vad detta betyder för sjukdom och behandling
Detta arbete visar att när parasitomvandlade makrofager förlorar sin spridningsförmåga omformas deras epigenetiska landskap djupt: en viktig stängande mark sprider sig från skarpa toppar till breda domäner, men detta översätts inte till en enkel, starkare genavstängning. Istället är den globala PRC2-drivna repressionen dämpad i attenuerade celler, medan en undergrupp av avgörande gener fortfarande är beroende av detta maskineri för att förbli avstängda. För djurhälsa antyder resultaten att riktade insatser mot PRC2 ensam sannolikt inte blir ett effektivt sätt att kontrollera Theileria-inducerade tumörer hos djur. Mer allmänt illustrerar studien hur infektion kan driva värdceller genom cancerlika epigenetiska tillstånd, och hur dramatiska förändringar i kromatinstruktur inte alltid får enkla funktionella följder. Att förstå dessa subtila epigenetiska skiften kan hjälpa till att förfina framtida strategier som syftar till att justera genreglering vid både infektionssjukdomar och cancer.
Citering: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
Nyckelord: epigenetik, Theileria, makrofager, histonmodifiering, PRC2