Clear Sky Science · ja
Theileria annulataによって形質転換されたマクロファージにおけるH3K27me3標識のエピジェネティックなランドスケープ
なぜ牛の寄生虫ががん生物学に重要なのか
熱帯性シェイレリア症はダニによって媒介される寄生虫Theileria annulataによって引き起こされる牛の重篤な疾患です。動物体内に入ると、この寄生虫は特定の白血球を無制限に分裂し移動する細胞へと変化させ、がんに似た振る舞いを示します。こうして形質転換された細胞は全身に広がり、病気を進行させます。興味深いことに、こうした感染細胞を長期間培養すると、徐々に拡散能力を失います。本論文は単純だが広範な問いを立てます:攻撃性の喪失に伴って感染細胞のDNAの梱包(クロマチン)にどのような変化が起きるか、そしてそれはより一般的ながん様増殖について何を教えてくれるか、ということです。
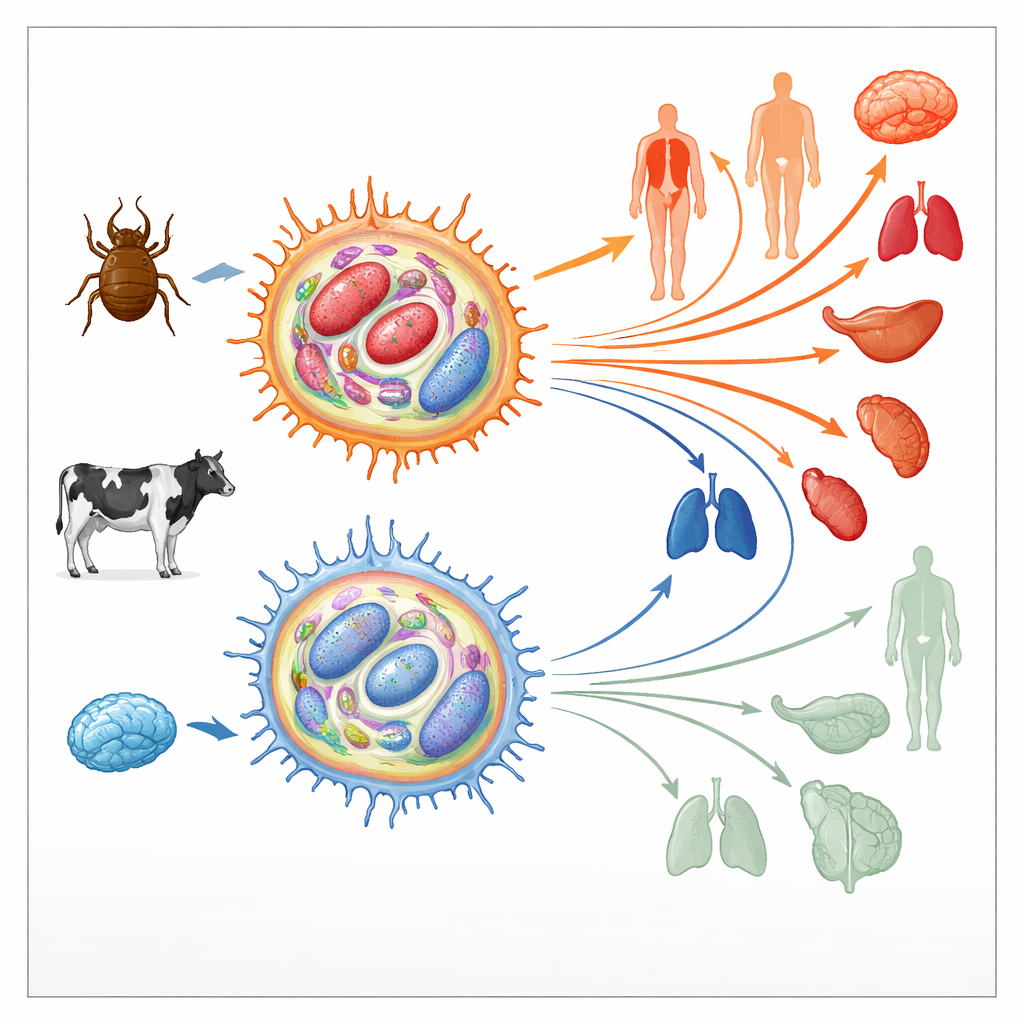
寄生虫が宿主の免疫細胞をどう作り替えるか
Theileria annulataはマクロファージと呼ばれる牛の免疫細胞内部に潜みます。そこで細胞死・増殖・運動を通常制御する主要なシグナル経路を操り、宿主細胞を腫瘍様の状態に押し込みます。こうして乗っ取られた細胞は無制限に分裂し、組織を移動して寄生虫を拡散させます。培養初期の感染マクロファージは高い「病原性(virulent)」を示し、動物内で容易に広がります。しかし何百回もの分裂を経ると、拡散能力は急激に低下し、「減弱(attenuated)」と呼ばれる状態になり、実際に生ワクチンとして利用されることもあります。攻撃的から非攻撃的への類似した変化はヒトのがんでも見られるため、著者らは配列を変えずに遺伝子のオン/オフを助ける化学的標識――すなわちエピジェネティックなランドスケープ――の変化がこのスイッチの基盤になっているかを調べました。
強力な遺伝子サイレンシング標識に着目する
本研究はヒストンタンパク質上の特定の化学タグ、H3K27me3に焦点を当てます。これはPolycomb Repressive Complex 2(PRC2)として知られるタンパク複合体によって付加され、細胞の同一性や発生を制御する遺伝子を抑えることで著名です。クロマチン免疫沈降に続くシークエンシング(ChIP-seq)を用いて、著者らは病原性マクロファージと減弱マクロファージにおけるボウ牛ゲノム全体のH3K27me3の配置をマッピングしました。比較のために活性化に関連するマークであるH3K4me3もマッピングしました。抗体が寄生虫自身のヒストンではなく宿主細胞のH3K27me3を検出していることを確認しており、したがってこれらのマップは微生物ではなく牛細胞側の変化を反映しています。
鋭いピークから広いサイレントドメインへ
全体的なH3K27me3の量は減弱細胞で高く、一方で活性化マークであるH3K4me3は低くなっていました。しかし総量よりもむしろ印象的だったのはパターンの変化です。病原性のマクロファージではH3K27me3は遺伝子開始部付近に集中した狭いピークを形成しており、これはしばしば精密なPRC2駆動の遺伝子制御に関連します。減弱細胞ではその標識が広がり、周囲領域へ大きく伸びる広域ドメインを形成し、時に多くの隣接遺伝子を覆います。鮮烈な例がマクロファージの接着に関与するSKAP2遺伝子で、病原性細胞では小さな局所的パッチしか持たないのに対し、減弱細胞ではこの抑制マークが500キロベース以上にわたるドメイン内に入り、強く抑え込まれています。ゲノム全体でこのような広がりが一般的に見られ、細胞が病原性から減弱へと転じる際にDNAの梱包様式が大規模に再編成されていることを示唆します。
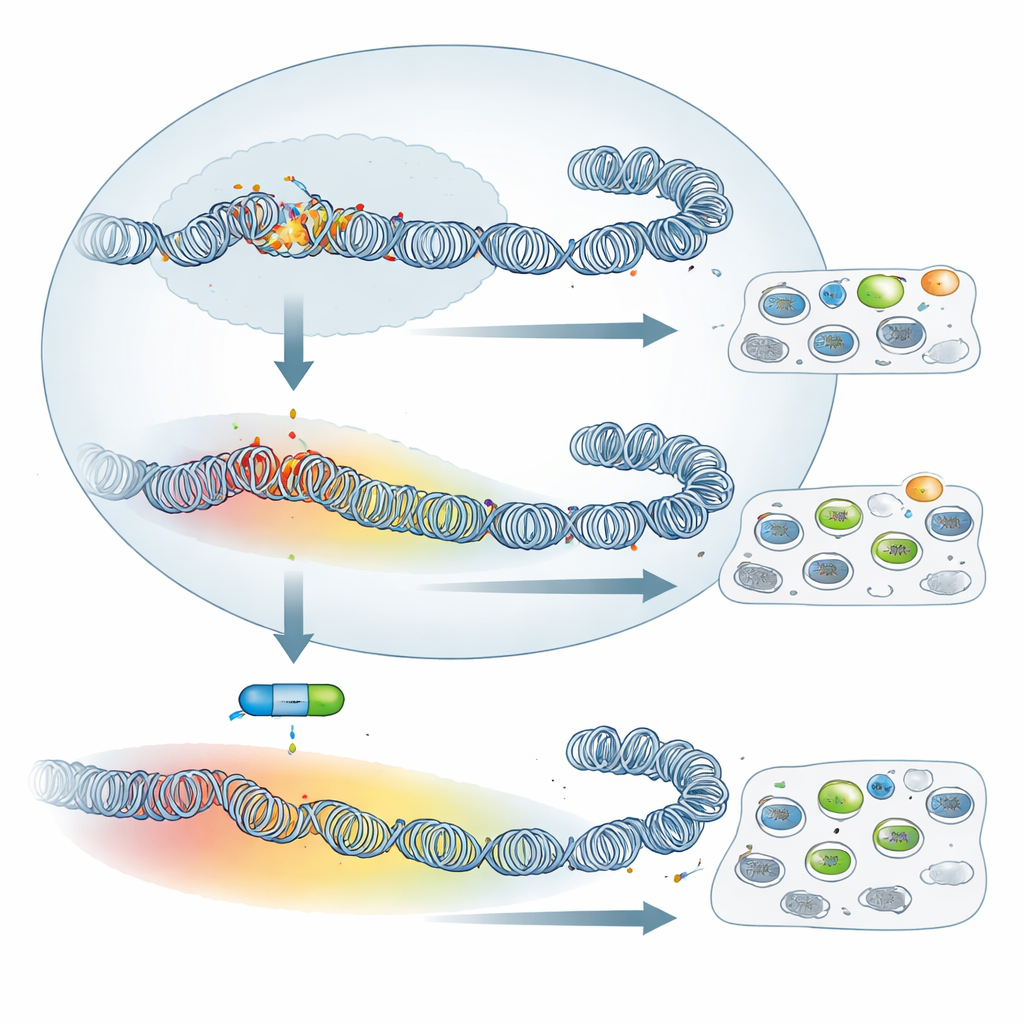
サイレンシング機構の阻害は限定的な影響しか与えない
このような広範な再構成を踏まえると、PRC2をオフにしてH3K27me3を消去すればこれらの細胞の振る舞いが劇的に変わると予想されます。研究チームは病原性および減弱マクロファージの両方をPRC2の酵素活性を阻害する薬剤UNC1999で処理し、H3K27me3が大幅に失われることを確認しました。しかし古典的な腫瘍様表現型はほとんど変化しませんでした:細胞のディッシュ上でのフィブロネクチンへの接着能や、免疫不全マウスにおける拡散能力は薬剤で有意に変わりませんでした。RNAシーケンシングで遺伝子発現を調べると、病原性細胞ではより多くの遺伝子が再活性化されたのに対し、減弱細胞ではそれほど再活性化が起こりませんでした。言い換えれば、減弱細胞はH3K27me3のカバレッジが広いにもかかわらず、遺伝子サイレンシングはPRC2に依存しにくくなっているのです。それでも、Granzyme AやFollistatinのような既知または疑われる腫瘍抑制因子を含む小さな共通の遺伝子群は、両細胞型で阻害剤により再び活性化され、コアとなるPRC2プログラムが残っていることを示しました。
疾患と治療にとっての意義
この研究は、寄生虫に形質転換されたマクロファージが拡散能力を失うにつれて、そのエピジェネティックなランドスケープが深く再形成されることを明らかにしました:重要なサイレンシング標識が鋭いピークから広いドメインへと広がる一方で、必ずしも単純に遺伝子の強い抑制につながるわけではありません。むしろ、減弱細胞では全般的なPRC2駆動の抑制は弱まりつつも、いくつかの重要な遺伝子はなおこの機構に依存して抑えられています。家畜の健康という観点では、PRC2単独を標的にすることはTheileria誘導腫瘍を制御する有効な手段とはなりにくいことを示唆します。より広い視点では、この研究は感染が宿主細胞をがん様のエピジェネティック状態へと押し進め得ること、そしてクロマチン構造の劇的な変化が必ずしも直線的な機能的結果をもたらすわけではないことを示しています。これらの微妙なエピジェネティックな変化を理解することは、感染症とがんの両方で遺伝子制御を調整する将来の戦略を洗練する助けになるかもしれません。
引用: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
キーワード: エピジェネティクス, Theileria, マクロファージ, ヒストン修飾, PRC2