Clear Sky Science · pl
Epigenetyczny krajobraz markera H3K27me3 w makrofagach przekształconych przez Theileria annulata
Dlaczego pasożyt bydła ma znaczenie dla biologii nowotworów
Tropikalna theilerioza to ciężka choroba bydła wywoływana przez pasożyta Theileria annulata, przenoszonego przez kleszcze. Po wejściu do organizmu pasożyt przekształca niektóre białe krwinki w komórki dzielące się bez końca, ruchome i zachowujące się podobnie do nowotworu. Takie przekształcone komórki rozprzestrzeniają się po organizmie i powodują chorobę. Co ciekawsze, gdy te zakażone komórki są długo hodowane w laboratorium, stopniowo tracą zdolność do szerzenia się. Artykuł zadaje proste, lecz dalekosiężne pytanie: jakie zmiany w upakowaniu DNA w tych komórkach towarzyszą utracie agresywności i czego to uczy nas o nowotworopodobnym wzroście w szerszym kontekście?
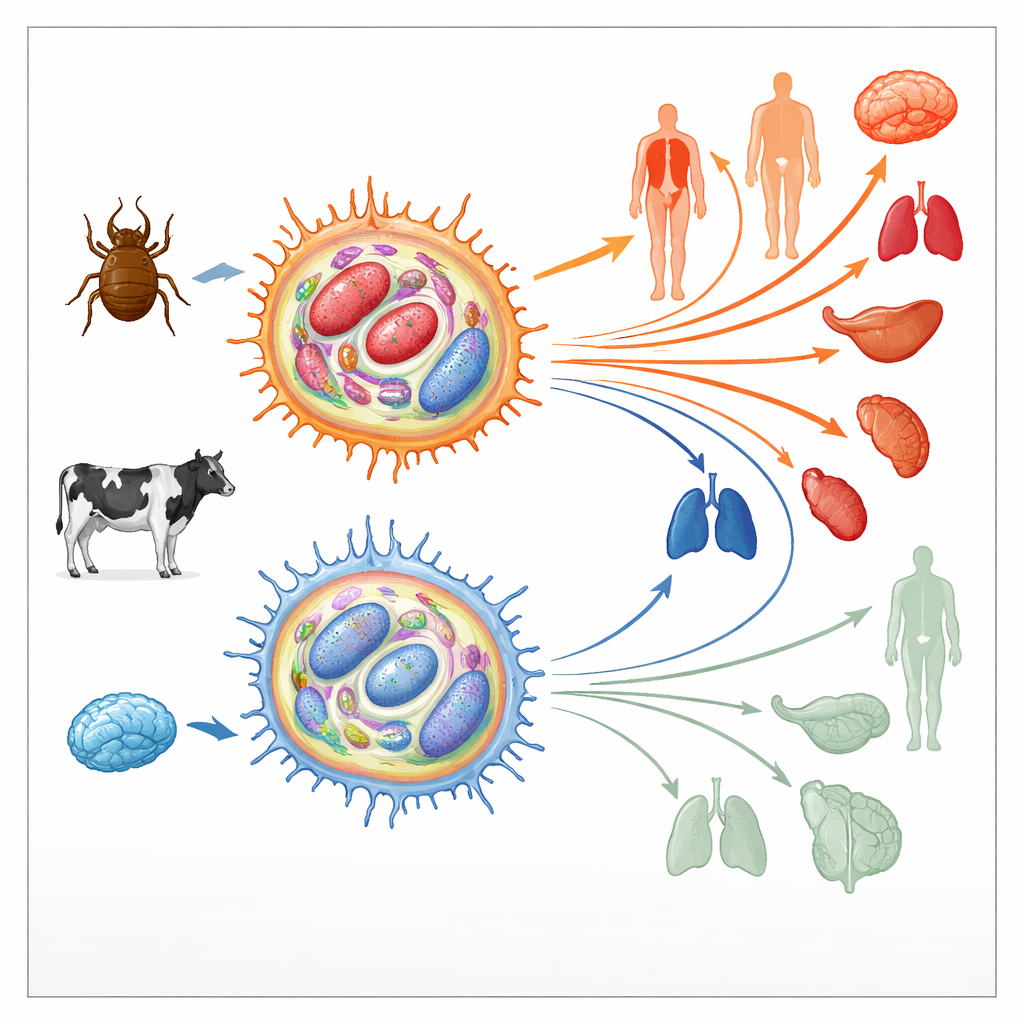
Jak pasożyt przeprogramowuje komórki układu odpornościowego gospodarza
Theileria annulata żyje wewnątrz bydlęcych komórek odpornościowych zwanych makrofagami. Manipuluje tam kluczowymi szlakami sygnalizacyjnymi, które normalnie kontrolują śmierć komórkową, podział i ruch, popychając komórkę gospodarza w stan przypominający guz. Przejęte komórki mogą wtedy dzielić się bez ograniczeń i migrować przez tkanki, rozprzestrzeniając pasożyta. We wczesnym etapie hodowli takie zakażone makrofagi są wysoce „wirusogenne” (virulent), czyli łatwo się rozprzestrzeniają in vivo. Po kilkuset podziałach ich zdolność do rozprzestrzeniania się jednak gwałtownie spada; stają się „osłabione” (attenuated) i są nawet wykorzystywane jako szczepionki żywe. Ponieważ podobne przejścia z stanów agresywnych do mniej agresywnych występują w ludzkich nowotworach, autorzy zbadali, czy zmiany w epigenetycznym krajobrazie komórek — chemicznych znakach pomagających włączać lub wyłączać geny bez zmiany sekwencji DNA — mogą leżeć u podstaw tej zmiany.
Skupienie na silnym znaku wyciszającym geny
Badanie koncentruje się na konkretnej modyfikacji histonów, nazwanej H3K27me3. Znacznik ten jest dodawany przez kompleks białkowy znany jako Polycomb Repressive Complex 2 (PRC2) i jest powszechnie kojarzony z wyłączaniem genów kontrolujących tożsamość komórkową i rozwój. Przy użyciu immunoprecypitacji chromatyny z następczym sekwencjonowaniem (ChIP-seq) autorzy zmapowali rozmieszczenie H3K27me3 w genomie bydła w makrofagach zakażonych pasożytem, porównując komórki wirulentne i osłabione. Dla porównania zmapowali także H3K4me3, znacznik związany z aktywnymi genami. Potwierdzili, że ich przeciwciało wykrywa wersję H3K27me3 komórki gospodarza, a nie histony pasożyta, zatem mapy odzwierciedlają zmiany w komórce bydła, a nie w mikroorganizmie.
Od ostrych szczytów po szerokie domeny ciszy
Ogólna ilość H3K27me3 była wyższa w komórkach osłabionych, podczas gdy aktywujący znacznik H3K4me3 był niższy. Jeszcze bardziej uderzająca niż całkowite poziomy była zmiana wzorca. W makrofagach wirulentnych H3K27me3 tworzył wąskie szczyty skupione blisko miejsc startu genów, konfigurację często związaną z precyzyjną regulacją przez PRC2. W komórkach osłabionych znacznik rozprzestrzeniał się, tworząc szerokie domeny rozciągające się daleko w sąsiednie obszary, czasami obejmujące wiele pobliskich genów. Żywym przykładem jest gen SKAP2, zaangażowany w adhezję makrofagów: w komórkach wirulentnych nosi małą lokalną łatkę H3K27me3, lecz w komórkach osłabionych leży w obrębie domeny tej represyjnej modyfikacji większej niż 500 kilobaz i jest silnie wyciszony. W całym genomie takie rozprzestrzenianie było powszechne, sugerując gruntowną przebudowę upakowania DNA, gdy komórki przechodzą od zachowania wirulentnego do osłabionego.
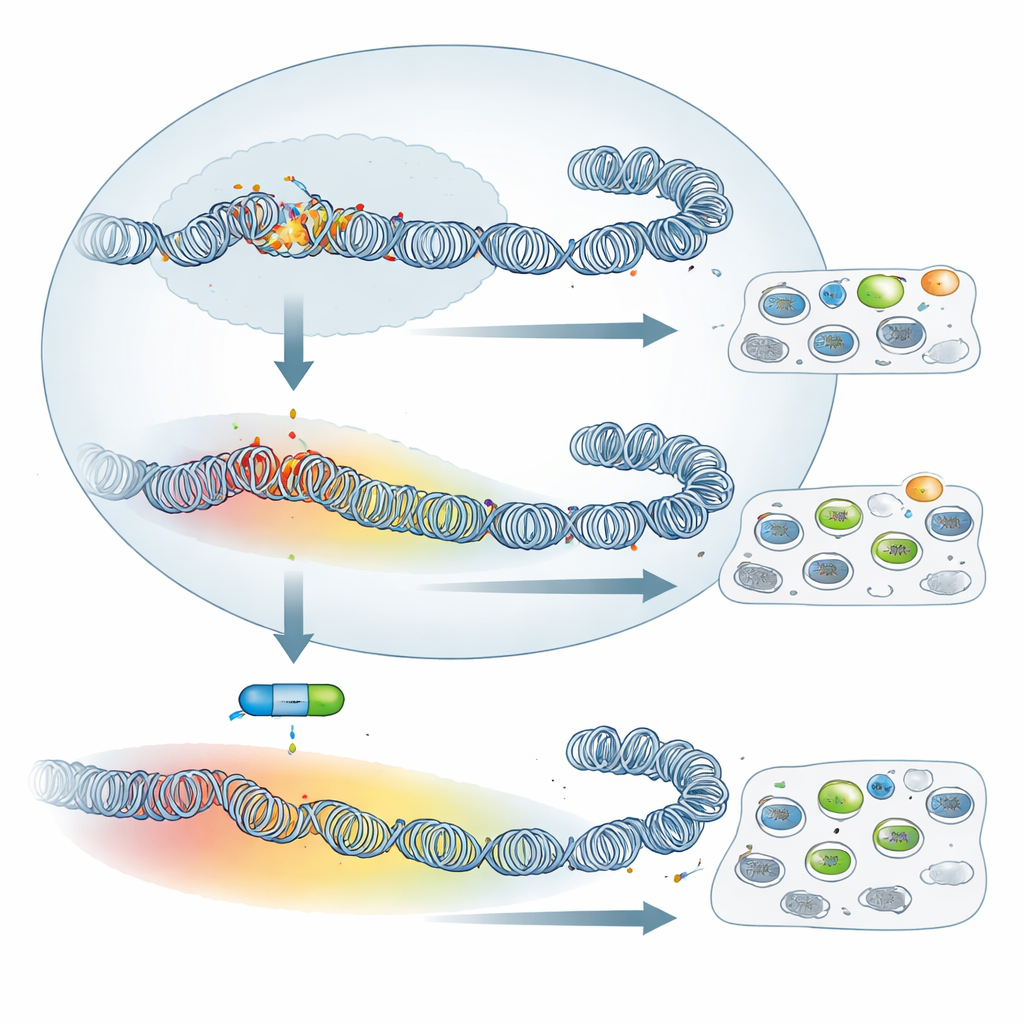
Blokowanie machiny wyciszającej daje ograniczony efekt
Biorąc pod uwagę tę szeroką rearanżację, można by się spodziewać, że wyłączenie PRC2 — a więc usunięcie H3K27me3 — dramatycznie zmieni zachowanie tych komórek. Zespół potraktował zarówno makrofagi wirulentne, jak i osłabione związkiem UNC1999, inhibitorem aktywności enzymatycznej PRC2, i potwierdził, że H3K27me3 zostało w dużej mierze utracone. Mimo to klasyczne cechy nowotworopodobne zmieniły się nieznacznie: zdolność komórek do przyczepiania się do fibryonektyny na płytce oraz ich zdolność do rozsiewu w mysich modelach z niedoborem odporności nie uległy istotnym zmianom po zastosowaniu leku. Analiza aktywności genów przez sekwencjonowanie RNA wykazała, że znacznie więcej genów zostało reaktywowanych w komórkach wirulentnych niż w osłabionych. Innymi słowy, mimo że komórki osłabione mają szersze pokrycie H3K27me3, ich wyciszanie genów jest mniej zależne od PRC2. Nadal jednak niewielka wspólna grupa genów, w tym znane lub podejrzewane supresory nowotworów, takie jak Granzyme A i Follistatin, została ponownie uaktywniona przez inhibitor w obu typach komórek, co pokazuje, że rdzeniowy program PRC2 pozostaje funkcjonalny.
Co to oznacza dla choroby i leczenia
Praca ta ujawnia, że gdy makrofagi przekształcone przez pasożyta tracą zdolność do szerzenia się, ich epigenetyczny krajobraz ulega głębokiej przebudowie: kluczowy znak wyciszający rozprzestrzenia się ze wąskich szczytów w szerokie domeny, jednak nie przekłada się to na prostsze czy silniejsze wyłączenie genów. Zamiast tego globalne represyjne działanie PRC2 jest osłabione w komórkach osłabionych, podczas gdy podzbiór istotnych genów nadal polega na tym mechanizmie, aby pozostać wyłączonymi. Dla zdrowia zwierząt wyniki sugerują, że samo ukierunkowanie PRC2 prawdopodobnie nie będzie skutecznym sposobem kontrolowania guzów wywołanych przez Theileria. W szerszym kontekście badanie pokazuje, jak zakażenie może popchnąć komórki gospodarza przez epigenetyczne stany podobne do nowotworów oraz że dramatyczne zmiany w strukturze chromatyny nie zawsze mają prosty efekt funkcjonalny. Zrozumienie tych subtelnych przesunięć epigenetycznych może pomóc w udoskonaleniu przyszłych strategii modulowania regulacji genów zarówno w chorobach zakaźnych, jak i w nowotworach.
Cytowanie: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
Słowa kluczowe: epigenetyka, Theileria, makrofagi, modyfikacja histonów, PRC2