Clear Sky Science · pt
Paisagem epigenética da marca H3K27me3 em macrófagos transformados por Theileria annulata
Por que um parasita bovino importa para a biologia do câncer
A theileriose tropical é uma doença grave do gado causada pelo parasita Theileria annulata, transmitido por carrapatos. Uma vez no animal, o parasita transforma certos glóbulos brancos em células móveis e de divisão contínua que se comportam de maneira semelhante ao câncer. Essas células transformadas se espalham pelo corpo e promovem a doença. Intrigantemente, quando essas células infectadas são cultivadas em laboratório por muito tempo, elas gradualmente perdem a capacidade de se disseminar. Este artigo faz uma pergunta simples, porém de grande alcance: que mudanças na embalagem do DNA das células infectadas acompanham essa perda de agressividade, e o que isso nos ensina sobre o crescimento semelhante ao câncer de forma mais ampla?
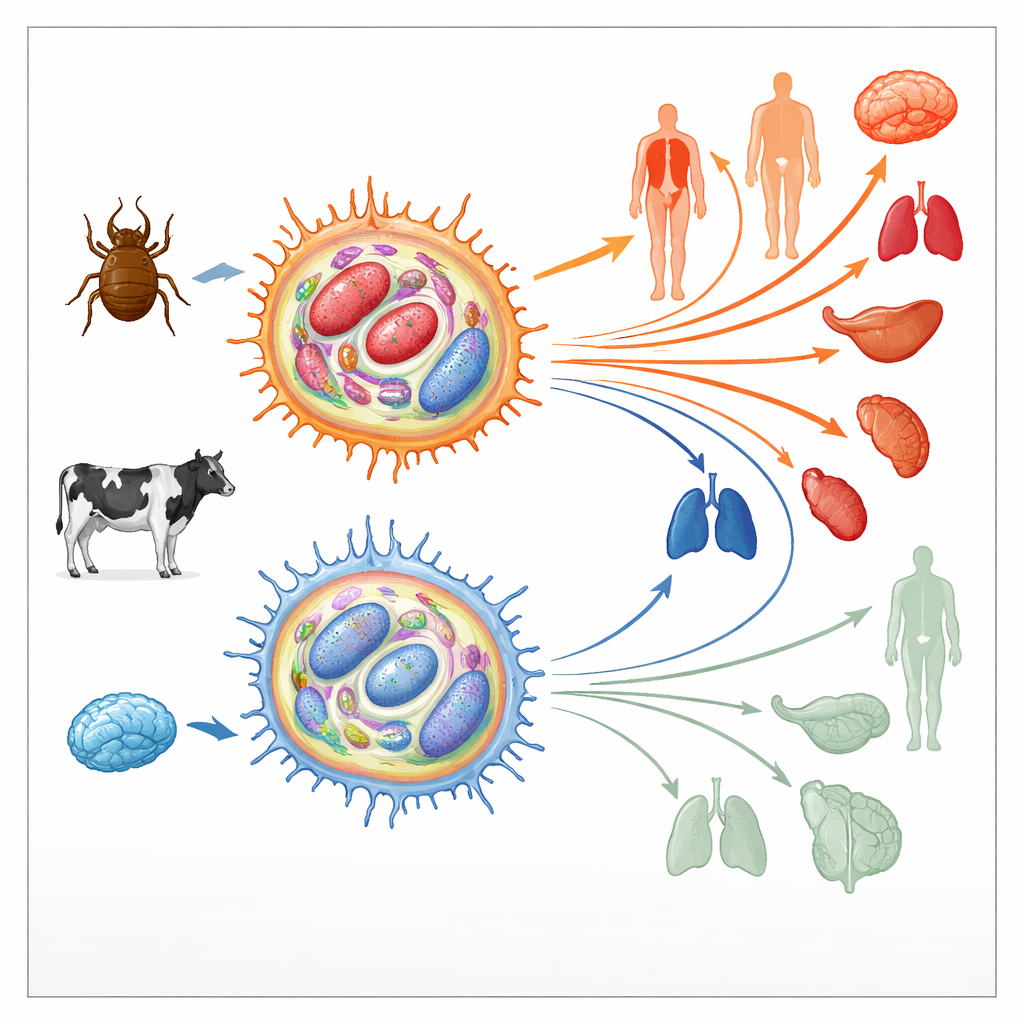
Como o parasita reprograma células imunes do hospedeiro
Theileria annulata vive dentro de células imunes bovinas chamadas macrófagos. Ali, ele manipula vias de sinalização-chave que normalmente controlam morte celular, divisão e movimento, empurrando a célula hospedeira para um estado semelhante a tumor. Essas células sequestradas podem então dividir-se sem limite e migrar pelos tecidos, espalhando o parasita. No início do cultivo, tais macrófagos infectados são altamente “virulentos”, ou seja, disseminam-se facilmente em animais. Após centenas de divisões celulares, contudo, sua capacidade de disseminação cai abruptamente; tornam-se “atenuados” e são até usados como vacinas vivas. Como transições similares de estados agressivos para menos agressivos ocorrem em cânceres humanos, os autores investigaram se mudanças na paisagem epigenética das células — as marcas químicas que ajudam a ligar ou desligar genes sem alterar a sequência de DNA — poderiam explicar essa mudança.
Foco em uma marca poderosa de silenciamento gênico
O estudo concentra-se em uma etiqueta química específica nas histonas, chamada H3K27me3. Essa marca é adicionada por um complexo proteico conhecido como Complexo Repressor de Policombinação 2 (PRC2) e é famoso por silenciar genes que controlam identidade celular e desenvolvimento. Usando imunoprecipitação de cromatina seguida de sequenciamento (ChIP-seq), os autores mapearam onde a H3K27me3 se encontra no genoma bovino em macrófagos infectados virulentos versus atenuados. Também mapearam H3K4me3, uma marca associada a genes ativos, para comparação. Eles confirmaram que seu anticorpo detecta a versão da H3K27me3 da célula hospedeira, mas não as próprias histonas do parasita, de modo que os mapas refletem mudanças na célula bovina e não no micro-organismo.
De picos estreitos a amplos domínios silenciosos
A quantidade total de H3K27me3 foi maior em células atenuadas, enquanto a marca ativadora H3K4me3 foi menor. Mais impressionante do que os níveis totais, porém, foi a mudança no padrão. Em macrófagos virulentos, a H3K27me3 formava picos estreitos centrados perto dos sítios de início de genes, uma configuração frequentemente ligada ao controle gênico preciso dirigido pelo PRC2. Em células atenuadas, a marca espalhou-se, formando domínios amplos que se estendiam para regiões circundantes, às vezes cobrindo muitos genes vizinhos. Um exemplo vívido é o gene SKAP2, envolvido na adesão de macrófagos: em células virulentas ele apresenta um pequeno trecho local de H3K27me3, mas em células atenuadas fica dentro de um domínio de repressão com mais de 500 kilobases e é fortemente silenciado. Ao longo do genoma, esse espalhamento foi comum, sugerindo uma remodelação abrangente de como o DNA é empacotado à medida que as células mudam de comportamento virulento para atenuado.
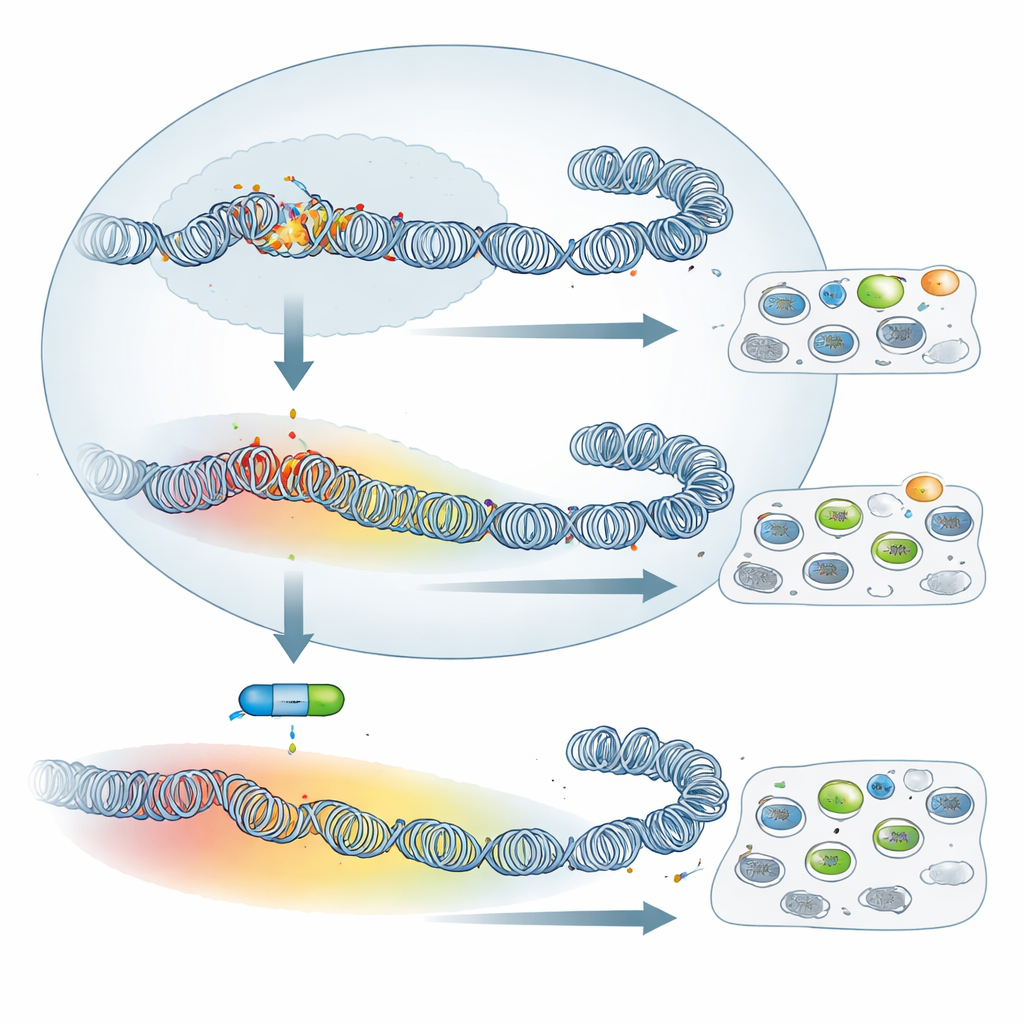
Bloquear a maquinaria de silenciamento tem impacto limitado
Dada essa reconfiguração ampla, poderia-se esperar que desativar o PRC2 — e assim apagar a H3K27me3 — mudasse dramaticamente o comportamento dessas células. A equipe tratou macrófagos virulentos e atenuados com UNC1999, uma droga que inibe a atividade enzimática do PRC2, e verificou que a H3K27me3 foi amplamente perdida. Ainda assim, traços clássicos de comportamento semelhante a tumor mudaram pouco: a capacidade das células de aderir à fibronectina em placa e sua capacidade de disseminação em camundongos imunodeprimidos não foram alteradas de forma significativa pelo fármaco. Quando os autores analisaram a atividade gênica por sequenciamento de RNA, descobriram que muito mais genes foram reativados em células virulentas do que em atenuadas. Em outras palavras, embora as células atenuadas apresentem cobertura mais ampla de H3K27me3, seu silenciamento gênico depende menos do PRC2. Ainda assim, um pequeno conjunto compartilhado de genes, incluindo supressores tumorais conhecidos ou suspeitos como Granzyme A e Follistatina, foi reativado pelo inibidor em ambos os tipos celulares, mostrando que um núcleo do programa PRC2 permanece ativo.
O que isso significa para doença e tratamento
Este trabalho revela que, à medida que macrófagos transformados pelo parasita perdem a capacidade de se espalhar, sua paisagem epigenética é profundamente remodelada: uma marca-chave de silenciamento se espalha de picos estreitos para amplos domínios, contudo isso não se traduz em um simples e mais forte desligamento gênico. Em vez disso, a repressão global dirigida pelo PRC2 é atenuada em células atenuadas, enquanto um subconjunto de genes cruciais ainda depende dessa maquinaria para permanecer desligado. Para a saúde do gado, os achados sugerem que mirar apenas o PRC2 provavelmente não será uma forma eficaz de controlar tumores induzidos por Theileria em animais. Mais amplamente, o estudo ilustra como a infecção pode empurrar células hospedeiras por estados epigenéticos semelhantes aos do câncer, e como mudanças dramáticas na estrutura da cromatina nem sempre têm resultados funcionais diretos. Compreender essas sutis alterações epigenéticas pode ajudar a refinar estratégias futuras destinadas a ajustar a regulação gênica tanto em doenças infecciosas quanto no câncer.
Citação: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
Palavras-chave: epigenética, Theileria, macrófagos, modificação de histonas, PRC2