Clear Sky Science · fr
Paysage épigénétique de la marque H3K27me3 dans des macrophages transformés par Theileria annulata
Pourquoi un parasite bovin intéresse la biologie du cancer
La théilériose tropicale est une maladie grave des bovins causée par le parasite Theileria annulata, transmis par les tiques. Une fois dans l’animal, le parasite transforme certains globules blancs en cellules mobiles et indéfiniment proliférantes qui se comportent de manière très proche du cancer. Ces cellules transformées se disséminent dans tout l’organisme et sont responsables de la maladie. Fait intrigant, lorsque ces cellules infectées sont maintenues en culture pendant longtemps, elles perdent progressivement leur capacité à se propager. Cet article pose une question simple mais de grande portée : quels changements dans l’organisation de l’ADN des cellules infectées accompagnent cette perte d’agressivité, et qu’apprenons-nous de cela sur la croissance de type cancéreux en général ?
Comment le parasite reprogramme les cellules immunitaires de l’hôte
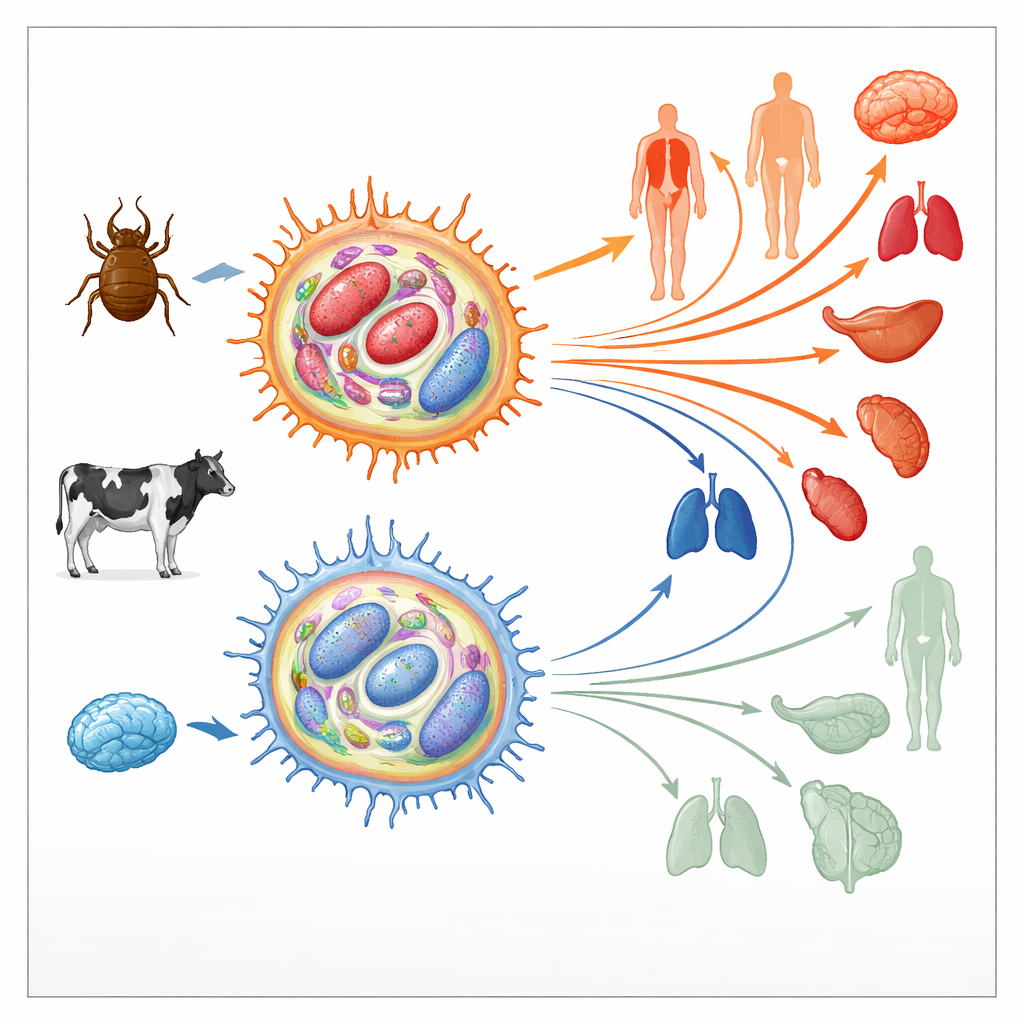
Theileria annulata vit à l’intérieur de cellules immunitaires bovines appelées macrophages. Là, il manipule des voies de signalisation clés qui contrôlent normalement la mort cellulaire, la division et le mouvement, poussant la cellule hôte vers un état de type tumoral. Ces cellules détournées peuvent alors se diviser sans limite et migrer à travers les tissus, propageant le parasite. En culture, ces macrophages infectés sont au début très « virulents », c’est‑à‑dire qu’ils se disséminent facilement chez l’animal. Après des centaines de divisions cellulaires, toutefois, leur capacité de dissémination chute fortement ; ils deviennent « atténués » et sont même utilisés comme vaccins vivants. Comme des transitions similaires d’un état agressif à un état moins agressif surviennent dans les cancers humains, les auteurs ont examiné si des changements dans le paysage épigénétique — les marques chimiques qui activent ou répriment les gènes sans modifier la séquence d’ADN — pouvaient sous‑tendre ce basculement.
Se concentrer sur une marque puissante de répression génique
L’étude s’intéresse à une marque chimique spécifique sur les histones, appelée H3K27me3. Cette marque est ajoutée par un complexe protéique connu sous le nom de Polycomb Repressive Complex 2 (PRC2) et est célèbre pour l’arrêt des gènes qui contrôlent l’identité cellulaire et le développement. À l’aide d’une immunoprécipitation de la chromatine suivie de séquençage (ChIP‑seq), les auteurs ont cartographié l’emplacement de H3K27me3 dans le génome bovin des macrophages infectés virulents versus atténués. Ils ont également cartographié H3K4me3, une marque associée aux gènes actifs, pour comparaison. Ils ont confirmé que leur anticorps détecte la version H3K27me3 de la cellule hôte mais pas les histones du parasite, de sorte que les cartes reflètent des changements dans la cellule bovine plutôt que dans le microbe.
De pics étroits à de larges domaines silencieux
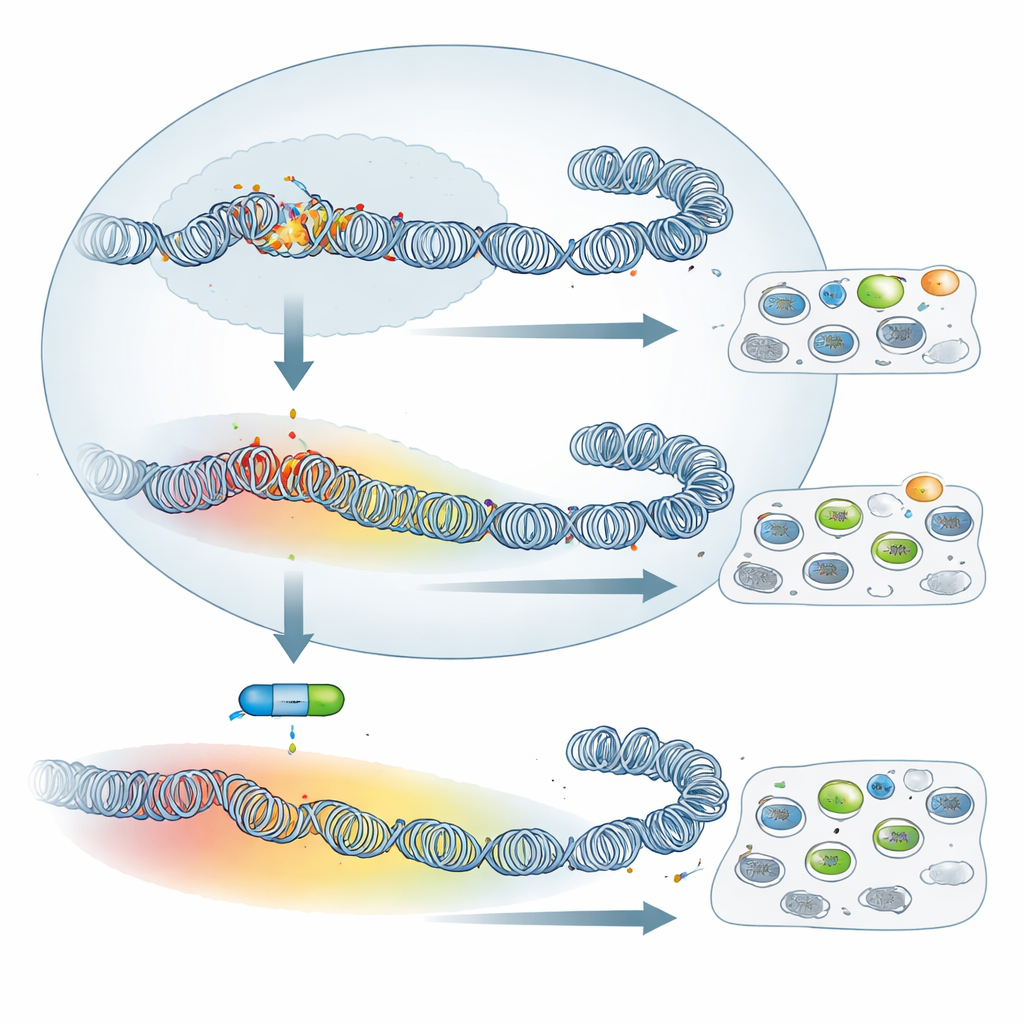
La quantité globale de H3K27me3 était plus élevée dans les cellules atténuées, tandis que la marque d’activation H3K4me3 était plus faible. Plus frappant que les niveaux totaux fut toutefois le changement de configuration. Dans les macrophages virulents, H3K27me3 formait des pics étroits centrés près des sites de démarrage des gènes, une configuration souvent liée à un contrôle précis piloté par PRC2. Dans les cellules atténuées, la marque s’est étendue, formant de larges domaines qui s’étendaient loin dans les régions avoisinantes, couvrant parfois de nombreux gènes voisins. Un exemple saisissant est le gène SKAP2, impliqué dans l’adhésion des macrophages : dans les cellules virulentes il porte une petite zone locale de H3K27me3, mais dans les cellules atténuées il se trouve à l’intérieur d’un domaine répressif de plus de 500 kilobases et est fortement réprimé. À l’échelle du génome, une telle expansion était courante, suggérant une refonte globale de l’empaquetage de l’ADN lorsque les cellules passent d’un comportement virulent à atténué.
Bloquer la machinerie de répression a un impact limité
Face à cette reconfiguration massive, on pourrait s’attendre à ce que l’inhibition de PRC2 — et donc l’effacement de H3K27me3 — modifie radicalement le comportement de ces cellules. L’équipe a traité des macrophages virulents et atténués avec UNC1999, un médicament qui inhibe l’activité enzymatique de PRC2, et a vérifié que H3K27me3 était largement perdu. Pourtant, les traits classiques de type tumoral ont à peine bougé : la capacité des cellules à adhérer à la fibronectine en culture et leur aptitude à se disséminer chez des souris immunodéficientes n’ont pas été significativement modifiées par le traitement. En examinant l’activité génique par séquençage d’ARN, les auteurs ont constaté que beaucoup plus de gènes étaient réactivés dans les cellules virulentes que dans les cellules atténuées. Autrement dit, bien que les cellules atténuées présentent une couverture plus large de H3K27me3, leur répression génique dépend moins de PRC2. Néanmoins, un petit groupe commun de gènes, incluant des suppresseurs de tumeur connus ou suspectés tels que la Granzyme A et la Follistatine, a été ranimé par l’inhibiteur dans les deux types cellulaires, montrant qu’un programme central piloté par PRC2 demeure actif.
Ce que cela signifie pour la maladie et le traitement
Ce travail révèle qu’à mesure que les macrophages transformés par le parasite perdent leur capacité de dissémination, leur paysage épigénétique est profondément remanié : une marque clé de répression s’étend de pics étroits à de larges domaines, mais cela ne se traduit pas par une simple et plus forte extinction des gènes. Au contraire, la répression globale menée par PRC2 est atténuée dans les cellules atténuées, tandis qu’un sous‑ensemble de gènes cruciaux dépend encore de cette machinerie pour rester éteint. Pour la santé du bétail, ces résultats suggèrent que cibler uniquement PRC2 est peu susceptible de constituer une stratégie efficace pour contrôler les tumeurs induites par Theileria chez les animaux. Plus largement, l’étude illustre comment une infection peut pousser les cellules hôtes dans des états épigénétiques apparentés au cancer, et comment des changements spectaculaires de la structure de la chromatine n’entraînent pas toujours des conséquences fonctionnelles simples. Comprendre ces déplacements épigénétiques subtils pourrait aider à affiner des stratégies futures visant à moduler la régulation des gènes, tant en maladies infectieuses qu’en oncologie.
Citation: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
Mots-clés: épigénétique, Theileria, macrophages, modification des histones, PRC2