Clear Sky Science · it
Paesaggio epigenetico della marcatura H3K27me3 nei macrofagi trasformati da Theileria annulata
Perché un parassita del bestiame interessa la biologia del cancro
La theileriosi tropicale è una malattia grave del bestiame causata dal parassita Theileria annulata, trasmesso dalle zecche. Una volta entrato nell’animale, il parassita trasforma alcuni globuli bianchi in cellule mobili che si dividono all’infinito e si comportano in modo molto simile al cancro. Queste cellule trasformate si diffondono nell’organismo e guidano la malattia. È interessante che, quando tali cellule infette vengono coltivate in laboratorio per lungo tempo, perdano gradualmente la capacità di diffondersi. Questo lavoro pone una domanda semplice ma di ampia portata: quali cambiamenti nel confezionamento del DNA delle cellule infette accompagnano questa perdita di aggressività, e cosa ci insegnano in generale sulla crescita simile al cancro?
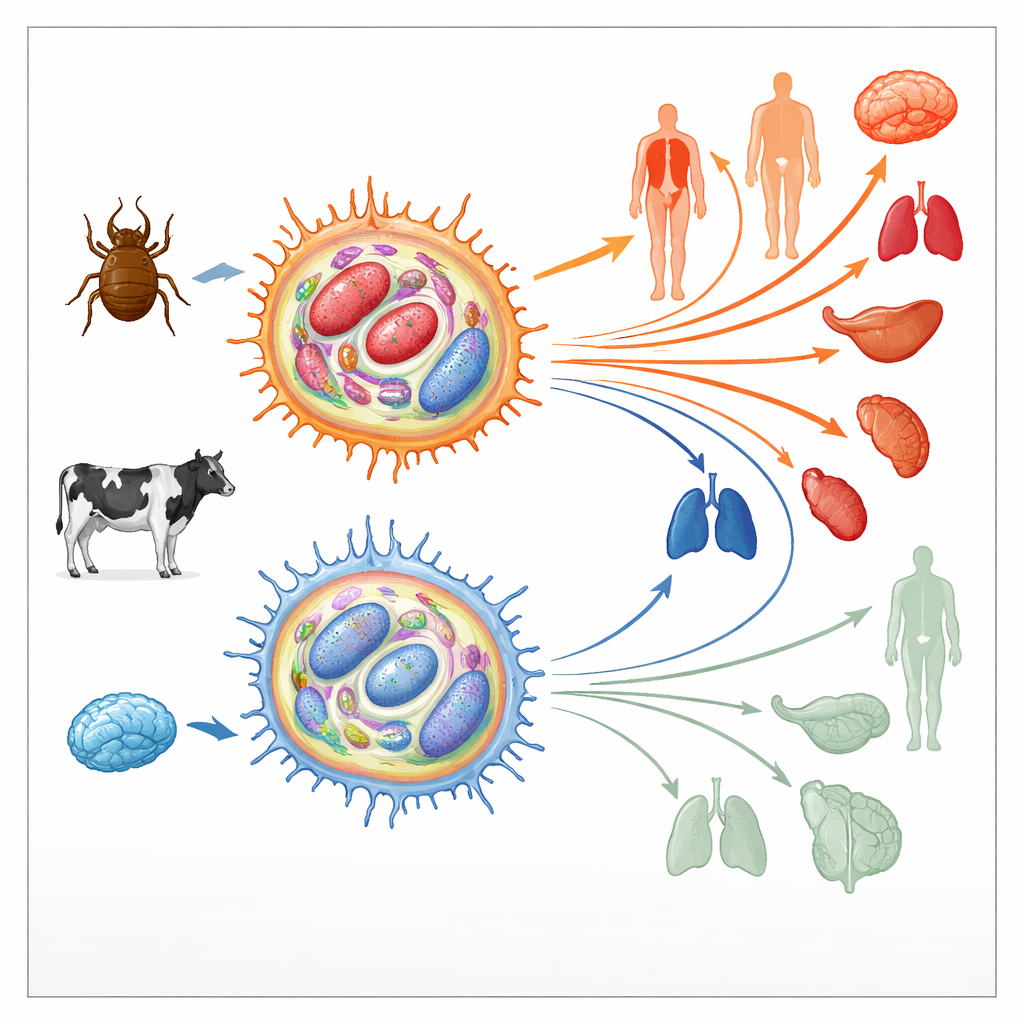
Come il parassita rimodella le cellule immunitarie dell’ospite
Theileria annulata vive all’interno di cellule immunitarie bovine chiamate macrofagi. Lì manipola vie di segnalazione chiave che normalmente controllano morte cellulare, divisione e movimento, spingendo la cellula ospite in uno stato simile a un tumore. Queste cellule dirottate possono quindi dividersi senza limite e migrare nei tessuti, favorendo la diffusione del parassita. All’inizio della coltura, tali macrofagi infetti sono altamente “virulenti”, cioè si disseminano facilmente negli animali. Dopo centinaia di divisioni cellulari, tuttavia, la loro capacità di diffondersi cala bruscamente; diventano “attenuati” e vengono persino usati come vaccini vivi. Poiché transizioni simili da stati aggressivi a meno aggressivi si osservano anche nei tumori umani, gli autori hanno esaminato se cambiamenti nel paesaggio epigenetico delle cellule—i segni chimici che aiutano ad accendere o spegnere i geni senza alterare la sequenza del DNA—possano essere alla base di questo passaggio.
Concentrare l’attenzione su un potente segno di silenziamento genico
Lo studio si focalizza su un particolare marcatore chimico sugli istoni, chiamato H3K27me3. Questo segno è aggiunto da un complesso proteico noto come Polycomb Repressive Complex 2 (PRC2) ed è famoso per spegnere geni che controllano l’identità cellulare e lo sviluppo. Tramite immunoprecipitazione della cromatina seguita da sequenziamento (ChIP-seq), gli autori hanno mappato la distribuzione di H3K27me3 nel genoma bovino in macrofagi infetti virulenti rispetto a quelli attenuati. Hanno anche mappato H3K4me3, un marcatore associato a geni attivi, per confronto. Hanno confermato che il loro anticorpo rileva la versione di H3K27me3 della cellula ospite ma non gli istoni del parassita, quindi le mappe riflettono cambiamenti nella cellula bovina piuttosto che nel microbo.
Da picchi netti a ampi domini silenti
La quantità complessiva di H3K27me3 era maggiore nelle cellule attenuate, mentre il marcatore attivante H3K4me3 risultava ridotto. Più significativo dei soli livelli totali è stato però il cambiamento nel modello di distribuzione. Nei macrofagi virulenti, H3K27me3 formava picchi stretti centrati vicino ai siti di inizio dei geni, una configurazione spesso legata a un controllo genico preciso guidato da PRC2. Nelle cellule attenuate, il marcatore si è diffuso, formando domini ampi che si estendevano nelle regioni circostanti, talvolta coprendo molti geni vicini. Un esempio vivido è il gene SKAP2, coinvolto nell’adesione dei macrofagi: nelle cellule virulenti porta una piccola patch locale di H3K27me3, ma nelle cellule attenuate si trova all’interno di un dominio repressivo di oltre 500 kilobasi ed è fortemente inattivato. Nel genoma questa diffusione era comune, suggerendo una rimodulazione su vasta scala del modo in cui il DNA è impacchettato quando le cellule passano da un comportamento virulento a uno attenuato.
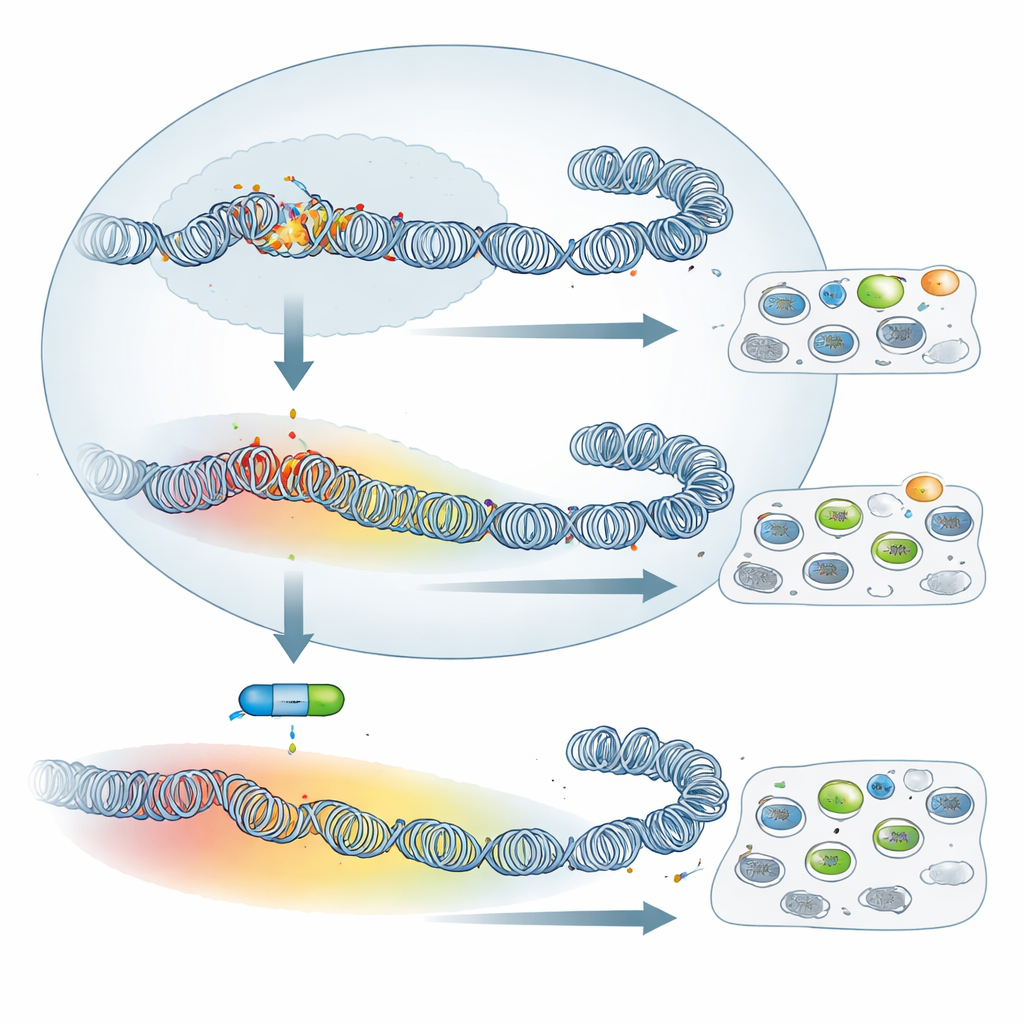
Bloccare la macchina del silenziamento ha un impatto limitato
Dato questo ripensamento esteso, ci si potrebbe aspettare che spegnere PRC2—e quindi cancellare H3K27me3—modifichi drasticamente il comportamento di queste cellule. Il gruppo ha trattato sia macrofagi virulenti sia attenuati con UNC1999, un farmaco che inibisce l’attività enzimatica di PRC2, e ha verificato che H3K27me3 è stata in gran parte persa. Eppure i classici tratti tumorali hanno subito pochi cambiamenti: la capacità delle cellule di aderire alla fibronectina in coltura e la loro capacità di disseminarsi in topi immunodeficienti non sono risultate significativamente alterate dal farmaco. Analizzando l’attività genica tramite RNA-seq, gli autori hanno trovato che molti più geni sono stati riattivati nelle cellule virulenti rispetto a quelle attenuate. In altre parole, anche se le cellule attenuate presentano una copertura più ampia di H3K27me3, il loro silenziamento genico dipende meno da PRC2. Tuttavia, un piccolo gruppo di geni condivisi, inclusi noti o sospetti oncosoppressori come Granzyme A e Follistatina, è stato riattivato dall’inibitore in entrambi i tipi cellulari, mostrando che esiste ancora un programma centrale dipendente da PRC2.
Cosa significa per malattia e trattamento
Questo lavoro rivela che, quando i macrofagi trasformati dal parassita perdono la capacità di diffondersi, il loro paesaggio epigenetico viene profondamente rimodellato: un marcatore chiave di silenziamento si espande da picchi netti a domini ampi, eppure ciò non si traduce in un semplice ed uniforme rafforzamento dello spegnimento genico. Al contrario, la repressione globale guidata da PRC2 è attenuata nelle cellule attenuate, mentre un sottoinsieme di geni cruciali continua a dipendere da questa macchina per restare spento. Per la salute del bestiame, i risultati suggeriscono che mirare solo a PRC2 è improbabile che sia una strategia efficace per controllare i tumori indotti da Theileria negli animali. Più in generale, lo studio illustra come l’infezione possa spingere le cellule ospiti attraverso stati epigenetici simili al cancro, e come cambiamenti drastici nella struttura della cromatina non si traducano sempre in risultati funzionali semplici. Comprendere questi sottili spostamenti epigenetici può aiutare a raffinare strategie future volte a modulare la regolazione genica sia nelle malattie infettive sia nel cancro.
Citazione: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
Parole chiave: epigenetica, Theileria, macrofagi, modificazione degli istoni, PRC2