Clear Sky Science · es
Panorama epigenético de la marca H3K27me3 en macrófagos transformados por Theileria annulata
Por qué un parásito bovino importa para la biología del cáncer
La theileriosis tropical es una enfermedad grave del ganado causada por el parásito Theileria annulata, transmitido por garrapatas. Una vez dentro del animal, el parásito transforma ciertos leucocitos en células móviles y de división indefinida que se comportan de forma muy parecida al cáncer. Estas células transformadas se diseminan por el organismo y causan la enfermedad. De forma intrigante, cuando dichas células infectadas se cultivan en laboratorio durante mucho tiempo, pierden gradualmente su capacidad de diseminación. Este trabajo plantea una pregunta simple pero de amplio alcance: ¿qué cambios en el empaquetamiento del ADN de las células infectadas acompañan a esta pérdida de agresividad, y qué nos enseña eso sobre el crecimiento tipo cáncer en general?
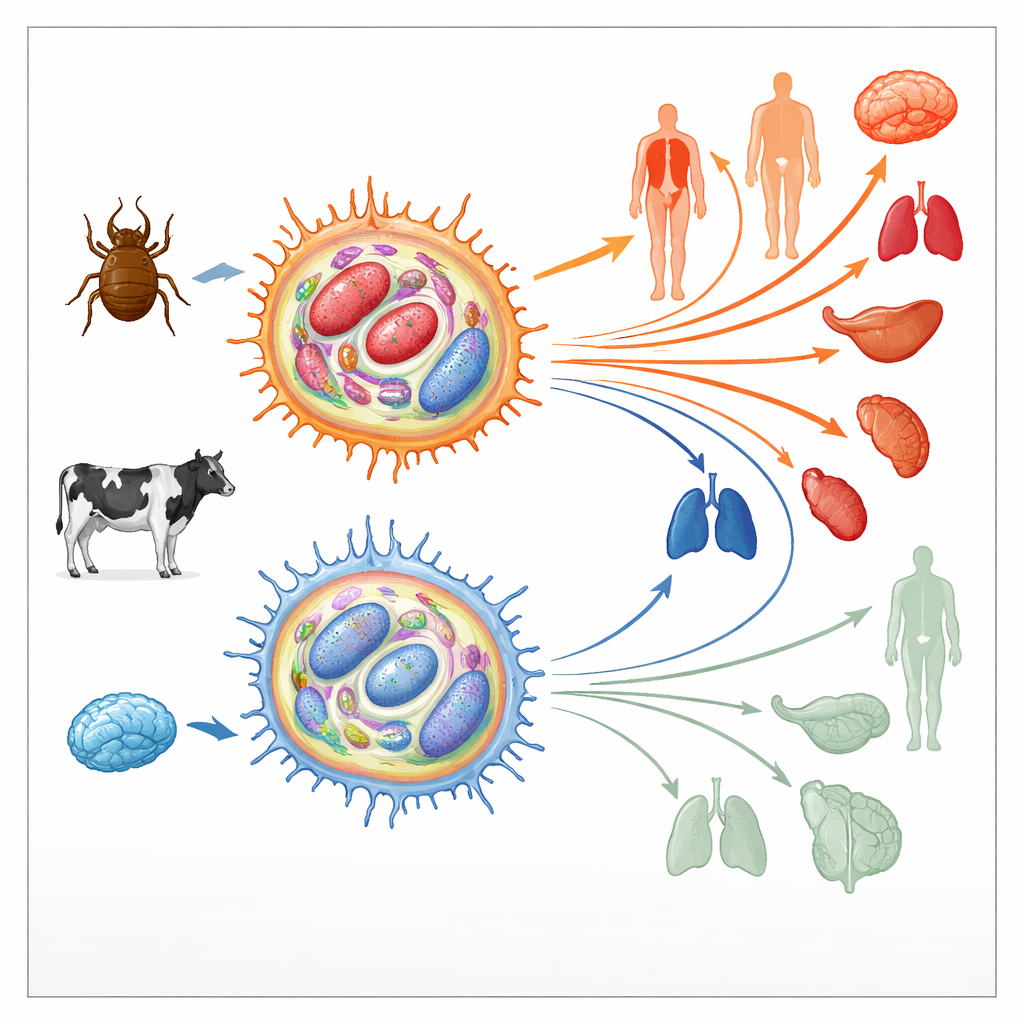
Cómo el parásito rehace las células inmunitarias del huésped
Theileria annulata vive dentro de células inmunitarias bovinas llamadas macrófagos. Allí manipula vías de señalización clave que normalmente controlan la muerte celular, la división y el movimiento, empujando a la célula huésped hacia un estado similar a un tumor. Estas células secuestradas pueden entonces dividirse sin límite y migrar por los tejidos, diseminando el parásito. Al inicio del cultivo, tales macrófagos infectados son muy “virulentos”, es decir, se diseminan con facilidad en los animales. Sin embargo, tras cientos de divisiones celulares su capacidad de diseminación cae bruscamente; se vuelven “atenuados” y se usan incluso como vacunas vivas. Dado que transiciones similares de estados agresivos a menos agresivos ocurren en cánceres humanos, los autores examinaron si cambios en el paisaje epigenético de las células —las marcas químicas que ayudan a activar o silenciar genes sin alterar la secuencia del ADN— podrían subyacer a este cambio.
Enfoque en una potente marca de silenciamiento génico
El estudio se centra en una etiqueta química específica en las histonas, llamada H3K27me3. Esta marca la añade un complejo proteico conocido como Complejo Represor de Polycomb 2 (PRC2) y es famosa por apagar genes que controlan la identidad celular y el desarrollo. Mediante inmunoprecipitación de la cromatina seguida de secuenciación (ChIP-seq), los autores cartografiaron dónde se localiza H3K27me3 en el genoma bovino comparando macrófagos infectados virulentos y atenuados. También mapearon H3K4me3, una marca asociada a genes activos, para comparación. Confirmaron que su anticuerpo detecta la versión de H3K27me3 de la célula huésped pero no las histonas del parásito, por lo que los mapas reflejan cambios en la célula bovina y no en el microbio.
De picos estrechos a dominios amplios y silenciados
La cantidad total de H3K27me3 fue mayor en las células atenuadas, mientras que la marca activadora H3K4me3 fue menor. Más llamativo que los niveles totales fue el cambio en el patrón. En macrófagos virulentos, H3K27me3 formaba picos estrechos centrados cerca de los sitios de inicio génico, una configuración a menudo vinculada al control preciso dirigido por PRC2. En células atenuadas, la marca se expandió, formando dominios amplios que se extendían hacia regiones circundantes, a veces abarcando muchos genes vecinos. Un ejemplo claro es el gen SKAP2, implicado en la adhesión de macrófagos: en células virulentas presenta un parche local pequeño de H3K27me3, pero en las atenuadas se encuentra dentro de un dominio repressivo de>500 kilobases y está fuertemente reprimido. A lo largo del genoma, este tipo de propagación fue común, lo que sugiere una remodelación masiva del empaquetamiento del ADN cuando las células cambian de comportamiento virulento a atenuado.
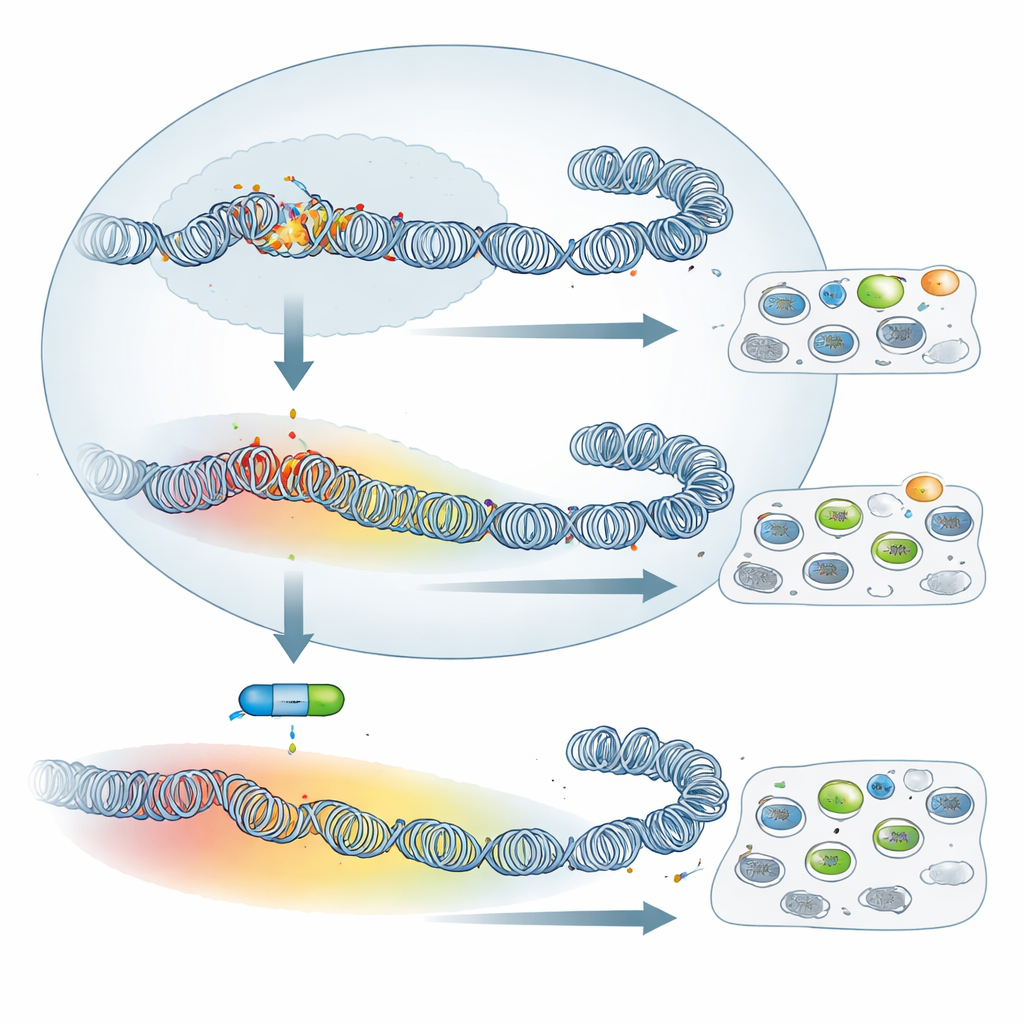
Bloquear la maquinaria de silenciamiento tiene un impacto limitado
Dada esta reconfiguración extensa, uno podría esperar que desactivar PRC2 —y por tanto borrar H3K27me3— cambiara drásticamente el comportamiento de estas células. El equipo trató tanto macrófagos virulentos como atenuados con UNC1999, un fármaco que inhibe la actividad enzimática de PRC2, y verificó que H3K27me3 se perdió en gran medida. Aun así, los rasgos clásicos tipo tumor poco cambiaron: la capacidad de las células para adherirse a fibronectina en placa y su potencial para diseminarse en ratones inmunodeficientes no se vieron alterados de forma significativa por el fármaco. Al examinar la actividad génica por secuenciación de ARN, encontraron que muchos más genes se reactivaron en las células virulentas que en las atenuadas. En otras palabras, aunque las células atenuadas contienen una cobertura más amplia de H3K27me3, su silenciamiento génico depende menos de PRC2. Aun así, un pequeño grupo compartido de genes, incluidos supresores tumorales conocidos o sospechosos como la Granzyme A y la Follistatina, se reactivaron con el inhibidor en ambos tipos celulares, mostrando que un núcleo del programa PRC2 permanece activo.
Qué significa esto para la enfermedad y el tratamiento
Este trabajo revela que, cuando los macrófagos transformados por el parásito pierden su capacidad de diseminarse, su paisaje epigenético se reconfigura profundamente: una marca clave de silenciamiento se expande de picos estrechos a dominios amplios, sin que ello se traduzca en un apagado génico más simple o más fuerte. En cambio, la represión global mediada por PRC2 está atenuada en las células atenuadas, mientras que un subconjunto de genes cruciales sigue dependiendo de esta maquinaria para mantenerse silenciado. Para la salud ganadera, los hallazgos sugieren que dirigir PRC2 por sí solo probablemente no sea una estrategia eficaz para controlar los tumores inducidos por Theileria en animales. En un sentido más amplio, el estudio ilustra cómo la infección puede empujar a las células del huésped a estados epigenéticos con aire de cáncer, y cómo cambios dramáticos en la estructura de la cromatina no siempre tienen resultados funcionales sencillos. Comprender estos sutiles desplazamientos epigenéticos puede ayudar a afinar futuras estrategias destinadas a ajustar la regulación génica tanto en enfermedades infecciosas como en cáncer.
Cita: Sakura, T., Tajeri, S., Rchiad, Z. et al. Epigenetic landscape of the H3K27me3 mark in macrophages transformed by Theileria annulata. Commun Biol 9, 478 (2026). https://doi.org/10.1038/s42003-026-09735-3
Palabras clave: epigenética, Theileria, macrófagos, modificación de histonas, PRC2