Clear Sky Science · zh
SH3 域通过非常规的三级接触选择性激活 PI3 激酶
细胞如何控制生长信号
我们的细胞不断在“生长、分裂或保持静止”之间做出决策。参与这一过程的关键决策者之一是称为 PI3 激酶(PI3K)的酶,它帮助调控细胞代谢与存活,并在许多癌症中异常活跃。本研究提出了一个微妙但重要的问题:当大量相似的分子“插头与插座”零件充斥细胞时,PI3K 如何区分那些无害的偶遇与少数能够将其从“关闭”切换到“开启”的相互作用?答案揭示了一层隐藏的选择性,这一发现可能有助于设计更精确的癌症疗法。
众多相似的插头,只有少数真正的开关
细胞充满了可重复使用的构件,称为蛋白质结构域——紧凑的模块,可与其他蛋白的短肽段结合。一个广泛存在的家族是 SH3 域,它识别富脯氨酸的简单基序,这类基序在人类蛋白质组中非常常见。由于这些基序如此普遍,而 SH3 域对它们的结合既弱又在一定程度上不加选择,人们一直困惑:含 SH3 的蛋白如何在高度特异的信号通路中发挥作用而不导致混乱?这一问题对 PI3K 尤为重要,因为其误激活会驱动癌症和其他疾病。早期工作表明,PI3K 的调控亚基 p85 可以被某些 Src 家族激酶的 SH3 域激活,但并非所有 SH3 都能做到这一点,尽管许多这些 SH3 识别相似的富脯氨酸标签。
PI3K 开关上的隐性辅助接触
作者们关注不同蛋白的 SH3 域如何与 p85 相互作用以及这如何影响 PI3K 活性。通过精确的结合测量和结构学方法,他们比较了 Fyn 的 SH3 域与来自 p85 的短富脯氨酸肽段以及几乎全长的 p85 片段之间的相互作用。短肽以常规方式与 Fyn 结合,而完整 p85 片段结合得更紧且具有不同的能量学特征,这提示额外的表面参与了相互作用。通过将 p85 解构为片段并重组为嵌合体,研究组证明其 C 端区——两个 SH2 结构域和通常夹住催化亚基 p110 的 iSH2 共螺旋段——也参与了与 SH3 的这种扩展的“三级”接触。
决定结合与激活的两个微小位点
核磁共振实验绘制出 Fyn SH3 域在与完整 p85 结合时受扰动最严重的部位。两个位点尤为突出:一个靠近常见的富脯氨酸结合槽(称为 PR 近端位点),另一个位于结构域的相对面(称为 PR 远端位点)。突变这些位点几乎不改变 SH3 与简单富脯氨酸肽段的结合强度,但显著改变了它与全长 p85 的结合方式以及关键的 PI3K 激活程度。在基于细胞的脂激酶测定中,一些亲和力仅有小幅变化的突变体实际上比野生型更强烈地激活了 PI3K,而其他亲和力相近的突变体则失去了大部分激活能力。这表明激活并不单纯依赖“握得有多紧”,而取决于 SH3 能否与 p85 的两个抑制性 SH2 区域形成合适的三级接触并将其从 p110 上重新定位开来。
把普通接触与真正的启动开关区分开
研究人员随后测试了来自其他若干蛋白的 SH3 域,包括 Hck、Grb2、p85 本身和 Ubs3A,特别关注 PR 远端位点的结构邻域。所有这些 SH3 域在总体上都能以类似的强度结合 p85,但只有那些在关键远端位点具有兼容疏水补丁的——如 Hck 和 Grb2 的 C 端 SH3——才能在生化测定中激活 PI3K。未激活的 SH3 域,包括 p85 自身的 SH3,仍能挂靠在 p85 的富脯氨酸区,但未能产生将抑制性 SH2 结构域拉开的额外三级接触模式。交联质谱支持这一观点:能激活的 SH3 域与 SH2 区域形成聚焦的接触,而不能激活的则取样更广泛的位置,符合一种更松散、非产生活性的结合方式。
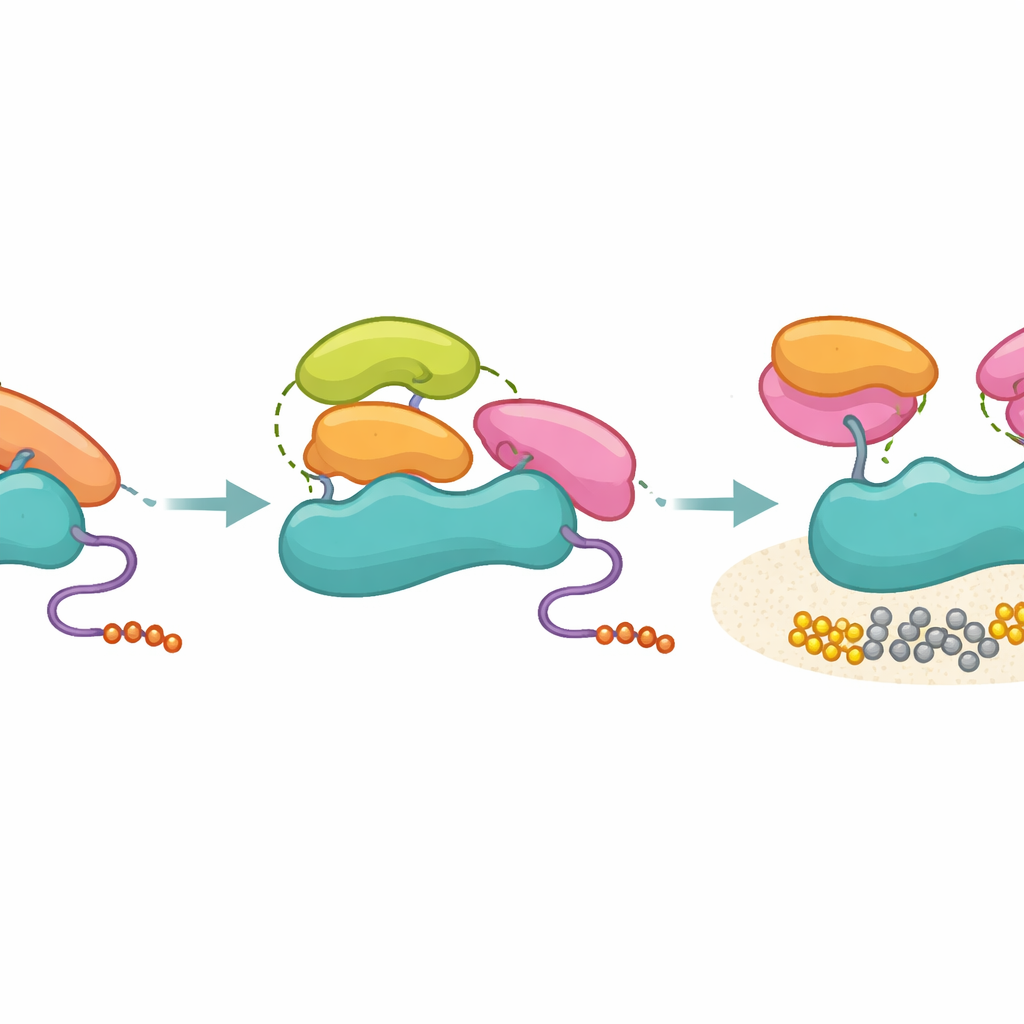
这对疾病与药物设计的意义
综上所述,该工作提出了一个模型:p85 充当分子过滤器——它并不阻止大量 SH3 域结合,但只允许那些能够形成正确三维接触的 SH3 真正解锁 PI3K。通俗地说,许多钥匙可以插入钥匙孔,但只有少数能使内部的销子对齐从而转动锁芯。结合与激活的分离有助于在细胞拥挤的环境中维持信号的准确性,并解释了为何看似“泛化结合”的 SH3 模块也能产生特异的功能结果。理解这些三级接触规则可能为设计模拟或阻断激活性 SH3 表面的药物指明方向,从而为调节癌症及其他由 PI3K 驱动的疾病中的 PI3K 信号提供新策略。
引用: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
关键词: PI3 激酶, 蛋白质信号传导, SH3 域, 癌症生物学, 分子相互作用