Clear Sky Science · pl
Domeny SH3 selektywnie aktywują kinazę PI3 poprzez niekonwencjonalne kontakty trzeciorzędowe
Jak komórki utrzymują sygnały wzrostu pod kontrolą
Nasze komórki nieustannie decydują, czy rosnąć, dzielić się, czy pozostawać w stanie spoczynku. Kluczowym rozstrzygającym ogniwem w tym procesie jest enzym zwany kinazą PI3 (PI3K), który kontroluje metabolizm komórkowy i przeżycie i często jest nadaktywowany w nowotworach. W tym badaniu zadano subtelne, ale istotne pytanie: gdy w komórce tłoczy się tyle podobnych molekularnych „wtyczek i gniazd”, jak PI3K rozróżnia niegroźne styczności od tych kilku, które rzeczywiście przełączają go z pozycji „wyłączony” na „włączony”? Odpowiedź ujawnia ukrytą warstwę selektywności, która może pomóc w projektowaniu precyzyjniejszych terapii przeciwnowotworowych.
Wiele podobnych wtyczek, tylko kilka prawdziwych przełączników
Komórki są wypełnione wielokrotnego użytku elementami budulcowymi zwanymi domenami białkowymi — zwartymi modułami, które wiążą krótkie fragmenty innych białek. Jedna szeroko rozpowszechniona rodzina, domeny SH3, rozpoznaje proste motywy bogate w prolinę, które są bardzo powszechne w ludzkim proteomie. Ponieważ te motywy są tak liczne, a domeny SH3 wiążą je słabo i do pewnego stopnia niedyskretnie, zastanawiające było, jak białka zawierające SH3 uczestniczą w wysoce specyficznych szlakach sygnalizacyjnych, nie powodując chaosu. To zagadnienie jest szczególnie istotne dla PI3K, którego nieprawidłowa aktywacja napędza nowotwory i inne choroby. Wcześniejsze prace wykazały, że podjednostka regulacyjna PI3K, nazwana p85, może zostać włączona przez domeny SH3 niektórych kinaz z rodziny Src, ale nie przez inne, mimo że wiele z tych domen SH3 rozpoznaje podobne prolinowe znaczniki.
Ukryte pomocnicze kontakty na przełączniku PI3K
Autorzy skupili się na tym, jak domeny SH3 z różnych białek wchodzą w interakcję z p85 i jak to wpływa na aktywność PI3K. Korzystając z precyzyjnych pomiarów wiązania i metod strukturalnych, porównali interakcję domeny SH3 Fyn z krótkim peptydem bogatym w prolinę pochodzącym z p85 oraz z niemal pełnej długości fragmentem p85. Podczas gdy krótki peptyd wiązał się z Fyn w standardowy sposób, pełny fragment p85 wiązał się silniej i z innym podpisem energetycznym, co sugerowało zaangażowanie dodatkowych powierzchni. Poprzez rozczłonkowanie p85 i odtworzenie go jako chimery, zespół wykazał, że jego regiony C‑terminalne — dwie domeny SH2 oraz skrętowy segment iSH2, które normalnie zaciskają się na katalitycznym partnerze p110 — także uczestniczą w tym rozszerzonym, czyli „trzeciorzędowym”, kontakcie z SH3.
Dwa maleńkie miejsca decydujące między przyłączeniem a aktywacją
Eksperymenty z rezonansiem magnetycznym jądrowym zmapowały, które części domeny SH3 Fyn są najbardziej zaburzone przy wiązaniu pełnego p85. Wyłoniły się dwa położenia: jedno w pobliżu zwykłego rowka wiążącego prolina (nazwane miejsce PR-proksymalne) i drugie na przeciwnej stronie domeny (miejsce PR-dystalne). Mutacje w tych pozycjach zaledwie nieznacznie zmieniały, jak mocno SH3 chwytają prosty peptyd bogaty w prolinę, lecz dramatycznie zmieniały, jak ten SH3 wiązał się z pełnej długości p85 i, co kluczowe, jak bardzo aktywował PI3K. W komórkowych testach kinazy lipidowej niektóre mutacje o umiarkowanym powinowactwie faktycznie aktywowały PI3K silniej niż dziki typ, podczas gdy inne o podobnym powinowactwie utraciły większość zdolności aktywacyjnej. Pokazało to, że aktywacja nie podąża po prostu za „siłą uścisku”, lecz zależy od tego, czy domena SH3 może utworzyć właściwe kontakty trzeciorzędowe z obiema inhibitującymi domenami SH2 p85 i przesunąć je z dala od p110.
Oddzielenie zwykłego kontaktu od prawdziwego włącznika
Naukowcy przetestowali następnie domeny SH3 z kilku innych białek, w tym Hck, Grb2, samego p85 i Ubs3A, zwracając szczególną uwagę na strukturalne otoczenie miejsca PR-dystalnego. Wszystkie te domeny SH3 mogły wiązać p85 z ogólnie podobną siłą, jednak tylko te z kompatycyjną hydrofobową łatką w kluczowej pozycji dystalnej — jak Hck i C‑końcowa domena SH3 Grb2 — były w stanie włączyć PI3K w testach biochemicznych. Domeny SH3 nieaktywujące, w tym własna domena SH3 p85, nadal przyczepiały się do regionu bogatego w prolinę p85, lecz nie generowały dodatkowego wzoru kontaktów trzeciorzędowych potrzebnego do odsunięcia inhibitorychnych domen SH2. Spektrometria mas po utworzeniu crosslinków wspierała tę koncepcję: domeny SH3 aktywujące tworzyły skoncentrowane kontakty z regionami SH2, podczas gdy te nieaktywujące próbowały szerszego zestawu pozycji, co odpowiadało luźniejszemu, nieproduktywnemu przyłączeniu.
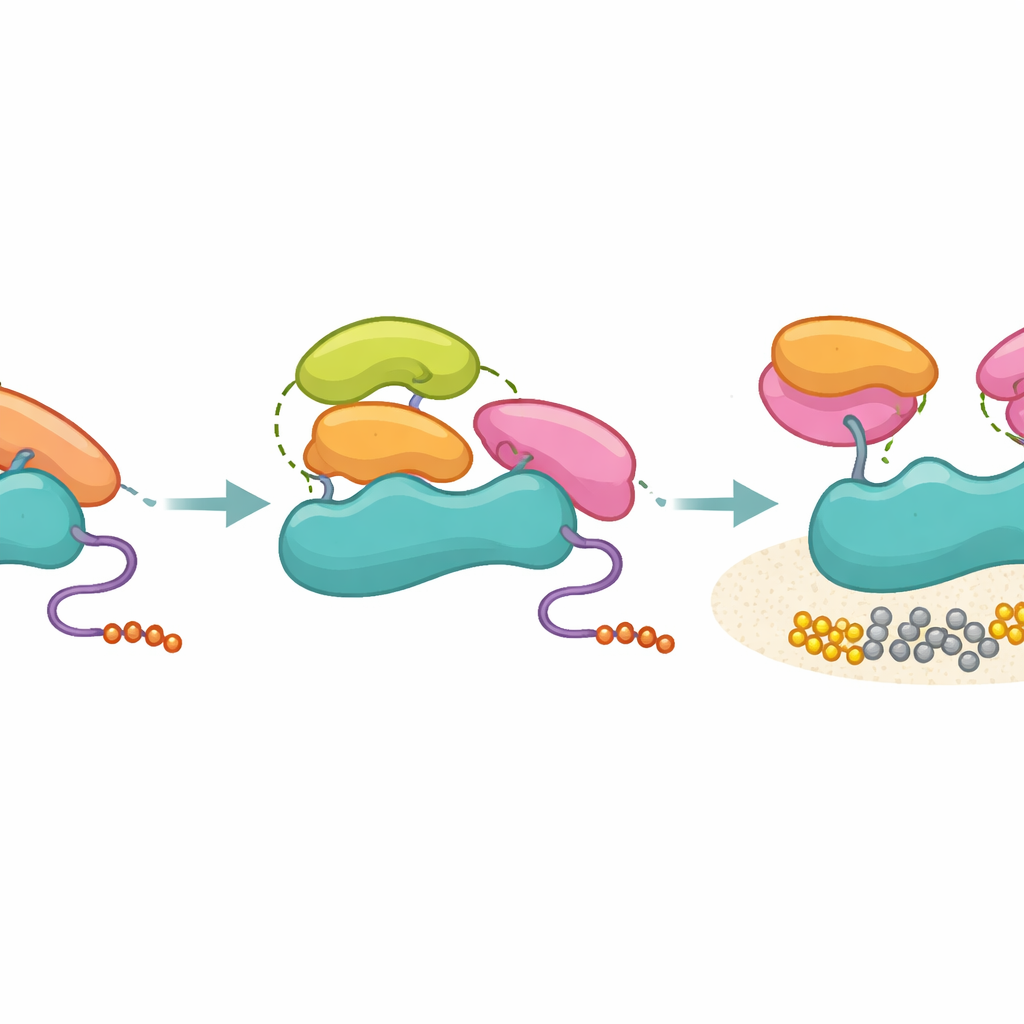
Co to znaczy dla chorób i projektowania leków
Podsumowując, praca proponuje model, w którym p85 działa jak filtr molekularny: nie zapobiega wielu domenom SH3 w przyłączaniu się, ale przepuszcza tylko te, które potrafią nawiązać właściwe trójwymiarowe kontakty, aby faktycznie odblokować PI3K. Mówiąc obrazowo: wiele kluczy pasuje do zamka, ale tylko kilka wyrównuje wewnętrzne palce wystarczająco dobrze, by przekręcić zamek. To rozdzielenie wiązania od aktywacji pomaga utrzymać precyzję sygnalizacji w zatłoczonym środowisku komórki i wyjaśnia, jak pozornie „promiskuitywne” moduły SH3 mogą wywoływać specyficzne efekty funkcjonalne. Zrozumienie tych zasad kontaktów trzeciorzędowych może wskazać drogę do leków, które naśladują lub blokują aktywujące powierzchnie SH3, oferując nowe strategie do modulowania sygnalizacji PI3K w nowotworach i innych chorobach napędzanych przez PI3K.
Cytowanie: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
Słowa kluczowe: kinaza PI3, sygnalizacja białkowa, domena SH3, biologia nowotworów, interakcje molekularne