Clear Sky Science · pt
Domínios SH3 ativam seletivamente a PI3 quinase por contatos terciários não convencionais
Como as Células Mantêm os Sinais de Crescimento Sob Controle
Nossas células decidem continuamente se crescem, se dividem ou permanecem inertes. Um componente-chave nesse processo é uma enzima chamada PI3 quinase (PI3K), que ajuda a controlar o metabolismo e a sobrevivência celular e frequentemente está hiperativa em cânceres. Este estudo faz uma pergunta sutil, porém importante: quando tantas peças moleculares semelhantes — tipo "pinos e tomadas" — se amontoam na célula, como a PI3K distingue encontros inofensivos daqueles poucos que a viram de "desligada" para "ligada"? A resposta revela uma camada oculta de seletividade que pode ajudar a projetar terapias contra o câncer mais precisas.
Muitos Pinos Parecidos, Apenas Alguns Verdadeiros Interruptores
As células estão cheias de blocos reutilizáveis chamados domínios proteicos — módulos compactos que se ligam a pequenos trechos de outras proteínas. Uma família ampla, os domínios SH3, reconhece motivos ricos em prolina que são muito comuns no proteoma humano. Como esses motivos são tão abundantes e os SH3 os reconhecem apenas fracamente e de forma relativamente indiscriminada, tem sido intrigante entender como proteínas com SH3 participam de vias de sinalização altamente específicas sem causar confusão. Esse enigma é especialmente relevante para a PI3K, cuja ativação indevida impulsiona câncer e outras doenças. Trabalhos anteriores já mostraram que a subunidade regulatória da PI3K, chamada p85, pode ser ativada por domínios SH3 de certas quinases da família Src, mas não por outras, apesar de muitos desses SH3 reconhecerem sequências prolinas parecidas.
Os Contatos Auxiliares Ocultos no Interruptor da PI3K
Os autores concentraram-se em como domínios SH3 de proteínas diferentes interagem com p85 e como isso afeta a atividade da PI3K. Usando medições precisas de ligação e métodos estruturais, compararam a interação do domínio SH3 de Fyn com um peptídeo curto rico em prolina derivado de p85 versus com p85 quase em comprimento total. Enquanto o peptídeo curto envolvia Fyn de maneira padrão, o fragmento maior de p85 ligou-se com maior afinidade e apresentou uma assinatura energética diferente, sugerindo que superfícies adicionais entravam em cena. Ao dissecar p85 em partes e reconstruí-lo como quimeras, a equipe demonstrou que suas regiões C‑terminais — os dois domínios SH2 e o segmento iSH2 em hélice que normalmente prende a parceira catalítica p110 — também participam desse contato ampliado, ou "terciário", com o SH3.
Dois Pontos Minúsculos que Decidem Entre Ligação e Ativação
Experimentos de ressonância magnética nuclear mapearam quais partes do domínio SH3 de Fyn são mais perturbadas quando ele se liga ao p85 completo. Dois pontos se destacaram: um próximo ao sulco usual de ligação à prolina (chamado sítio PR-proximal) e outro na face oposta do domínio (um sítio PR-distal). Mutar essas posições quase não mudou o quanto o SH3 prendia o peptídeo simples rico em prolina, mas alterou dramaticamente como ele interagia com o p85 de comprimento total e, crucialmente, quanto a PI3K era ativada. Em ensaios celulares de quinase lipídica, alguns mutantes com afinidade modesta ativaram a PI3K mais fortemente que o tipo selvagem, enquanto outros com afinidade semelhante perderam a maior parte de seu poder ativador. Isso mostrou que a ativação não segue simplesmente “o quão forte é a ligação”, mas depende de o domínio SH3 conseguir formar os contatos terciários corretos com ambas as regiões SH2 inibitórias de p85 e reposicioná-las em relação a p110.
Separando o Contato Simples do Verdadeiro Interruptor
Os pesquisadores então testaram domínios SH3 de várias outras proteínas, incluindo Hck, Grb2, o próprio p85 e Ubs3A, prestando atenção especial ao entorno estrutural do sítio PR-distal. Todos esses domínios SH3 puderam ligar-se a p85 com força amplamente semelhante, mas apenas aqueles com uma mancha hidrofóbica compatível na posição distal-chave — como Hck e o SH3 C-terminal de Grb2 — foram capazes de ativar a PI3K em ensaios bioquímicos. Domínios SH3 não ativadores, incluindo o próprio SH3 de p85, ainda se ligavam à região rica em prolina de p85, mas falhavam em gerar o padrão extra de contatos terciários necessário para afastar os domínios SH2 inibitórios. A espectrometria de massa com ligação cruzada apoiou essa visão: domínios SH3 ativadores formaram contatos focados com as regiões SH2, enquanto os não ativadores amostram um conjunto mais amplo de posições, consistente com uma fixação mais frouxa e não produtiva.
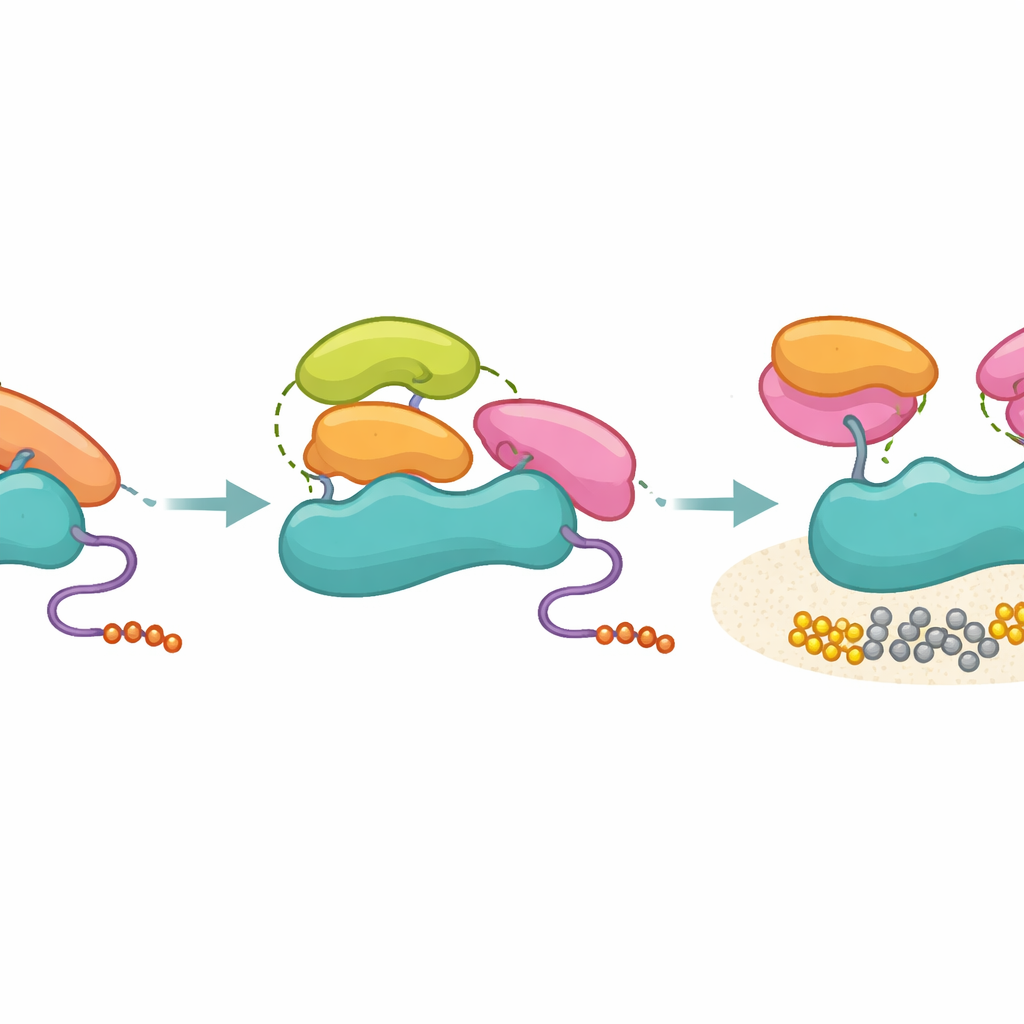
O Que Isso Significa para Doenças e Desenvolvimento de Fármacos
Em conjunto, o trabalho propõe um modelo em que p85 atua como um filtro molecular: ele não impede muitos domínios SH3 de se ligarem, mas só permite que aqueles que conseguem estabelecer os contatos tridimensionais corretos realmente desbloqueiem a PI3K. Em termos cotidianos, muitas chaves entram na fechadura, mas apenas algumas alinham os pinos internos bem o suficiente para girar a chave. Essa separação entre ligação e ativação ajuda a manter a precisão da sinalização no ambiente congestionado da célula e explica como módulos SH3 aparentemente “promíscuos” podem ter resultados funcionais específicos. Compreender essas regras de contato terciário pode apontar caminhos para fármacos que imitem ou bloqueiem superfícies SH3 ativadoras, oferecendo novas estratégias para ajustar a sinalização da PI3K em cânceres e outras doenças dirigidas pela PI3K.
Citação: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
Palavras-chave: PI3 quinase, sinalização proteica, domínio SH3, biologia do câncer, interações moleculares