Clear Sky Science · ar
مجالات SH3 تُفَعِّل بصورة انتقائية كيناز PI3 عبر تلامسات ثلاثية غير تقليدية
كيف تُسيطر الخلايا على إشارات النمو
تقرر خلاياِنا باستمرار ما إذا كانت ستنمو أو تنقسم أو تبقى في حالة سكون. أحد صانعي القرارات الرئيسيين في هذه العملية هو إنزيم يدعى كيناز PI3 (PI3K)، الذي يساعد في تنظيم أيض الخلية وبقائها وغالبًا ما يكون مفعّلاً بشكل مفرط في السرطانات. يطرح هذا البحث سؤالًا دقيقًا لكنه مهمًا: عندما تتكدس داخل الخلية العديد من القطع الجزيئية المتشابهة التي تعمل كـ «قابس ومقبس»، كيف يفرّق PI3K بين اللقاءات البريئة وتلك القليلة التي تحوّله فعلاً من حالة "مطفأ" إلى "مشتغل"؟ يكشف الجواب عن طبقة خفية من الانتقائية قد تساعد في تصميم علاجات سرطانية أكثر دقة.
منافذ متشابهة كثيرة، ومفاتيح تشغيل قليلة فقط
تمتلئ الخلايا بوحدات بناء قابلة لإعادة الاستخدام تُسمى مجالات البروتين — وحدات مدمجة ترتبط بمقاطع قصيرة من بروتينات أخرى. إحدى العائلات الشائعة، مجالات SH3، تتعرف على أنماط غنية بالبرولين بسيطة وتنتشر بكثرة في البروتيوم البشري. وبما أن هذه النماذج وافية الانتشار وارتباط مجالات SH3 بها عادة ضعيف وغير انتقائي إلى حد ما، كان من المحير كيف تشارك البروتينات الحاملة لمجال SH3 في مسارات إشارية محددة للغاية من دون أن تُحدث فوضى. تبرز هذه المعضلة بصورة خاصة بالنسبة لـ PI3K، إذ يؤدي نشاطه غير المنضبط إلى السرطان وأمراض أخرى. أظهرت أعمال سابقة أن الوحدة المنظمة لـ PI3K المسماة p85 يمكن أن تُفَعَّل بواسطة مجالات SH3 من بعض كينازات عائلة Src، ولكن ليس من الأخرى، رغم أن العديد من هذه المجالات يتعرف على لاصقات غنية بالبرولين متشابهة.
التلامسات المساعدة الخفية على مفتاح PI3K
ركز المؤلفون على كيفية تفاعل مجالات SH3 من بروتينات مختلفة مع p85 وكيف يؤثر ذلك على نشاط PI3K. باستخدام قياسات ارتباط دقيقة وطرق هيكلية، قارنوا تفاعل مجال SH3 من Fyn مع پبتيد قصير غني بالبرولين مأخوذ من p85 مقابل تفاعله مع p85 شبه كامل الطول. بينما تفاعل الببتيد القصير مع Fyn بالطريقة القياسية، ارتبط الجزء الكامل من p85 بشدة أكبر وببصمة طاقية مختلفة، مما دلّ على تدخل أسطح إضافية. عبر تفكيك p85 إلى أجزاء وإعادة بنائه كخلائط هجينة، أظهر الفريق أن مناطقه الطرفية الخلفية — نطاقي SH2 المزدوجين والمقطع اللولبي iSH2 الذي يقبض عادة على الشريك الحفاز p110 — تشارك أيضًا في هذا التلامس الممتد أو «الثلاثي» مع SH3.
نقطتان صغيرتان تقرران بين الارتباط والتفعيل
حددت تجارب الرنين المغناطيسي النووي أي أجزاء من مجال SH3 في Fyn تتأثر أكثر عند ارتباطه بـ p85 الكامل. برز موقعان: أحدهما قرب الأخدود المعتاد لالتقاط البرولين (الموقع القريب من PR) وآخر في الوجه المقابل للمجال (موقع بعيد عن PR). لم تغير طفرات في هذين الموقعين كثيرًا مدى ارتباط SH3 بالپبتيد البسيط الغني بالبرولين، لكنها غيّرت بشكل درامي طريقة ارتباطه بـ p85 الكامل ومقدار النشاط الذي حفّز به PI3K. في اختبارات الكيناز الدهنية الخلوية، دفع بعض المتحورات ذات الألفة المتواضعة PI3K إلى تفعيل أقوى من النوع البري، بينما فقدت متحورات أخرى ذات ألفة متشابهة معظم قدرتها على التفعيل. بينت هذه النتائج أن التفعيل لا يتبع ببساطة "مدى قوة القبضة"، بل يعتمد على ما إذا كان مجال SH3 قادرًا على تكوين التلامسات الثلاثية الصحيحة مع منطقتي SH2 المثبطتين في p85 وإبعادهما عن p110.
فصل اللمسة البسيطة عن مفتاح التشغيل الحقيقي
اختبر الباحثون بعد ذلك مجالات SH3 من عدة بروتينات أخرى، بما في ذلك Hck وGrb2 وp85 نفسه وUbs3A، مع إيلاء اهتمام خاص للمجاورة التركيبية للموقع البعيد عن PR. كانت كل هذه المجالات قادرة على الارتباط بـ p85 بقوة متقاربة إلى حد كبير، ومع ذلك لم تستطع سوى تلك التي تمتلك رقعة هيدروفوبية متوافقة في الموضع البعيد الرئيسي — مثل Hck وSH3 الطرفي لـ Grb2 — تشغيل PI3K في الاختبارات الحيوية الكيميائية. المجالات غير المنشّطة لـ SH3، بما في ذلك SH3 الخاص بـ p85، لا تزال تلتصق بمنطقة p85 الغنية بالبرولين لكنها تفشل في توليد نمط التلامس الثلاثي الإضافي المطلوب لسحب نطاقي SH2 المثبطين بعيدًا. دعمت تحليلات الطيف الكتلي بعد التشبيك هذه الصورة: شكلت مجالات SH3 المنشّطة تلامسات مركزة مع مناطق SH2، في حين جربت المجالات غير المنشّطة مجموعة أوسع من المواضع، متسقة مع ارتباط أوسع وأقل إنتاجية.
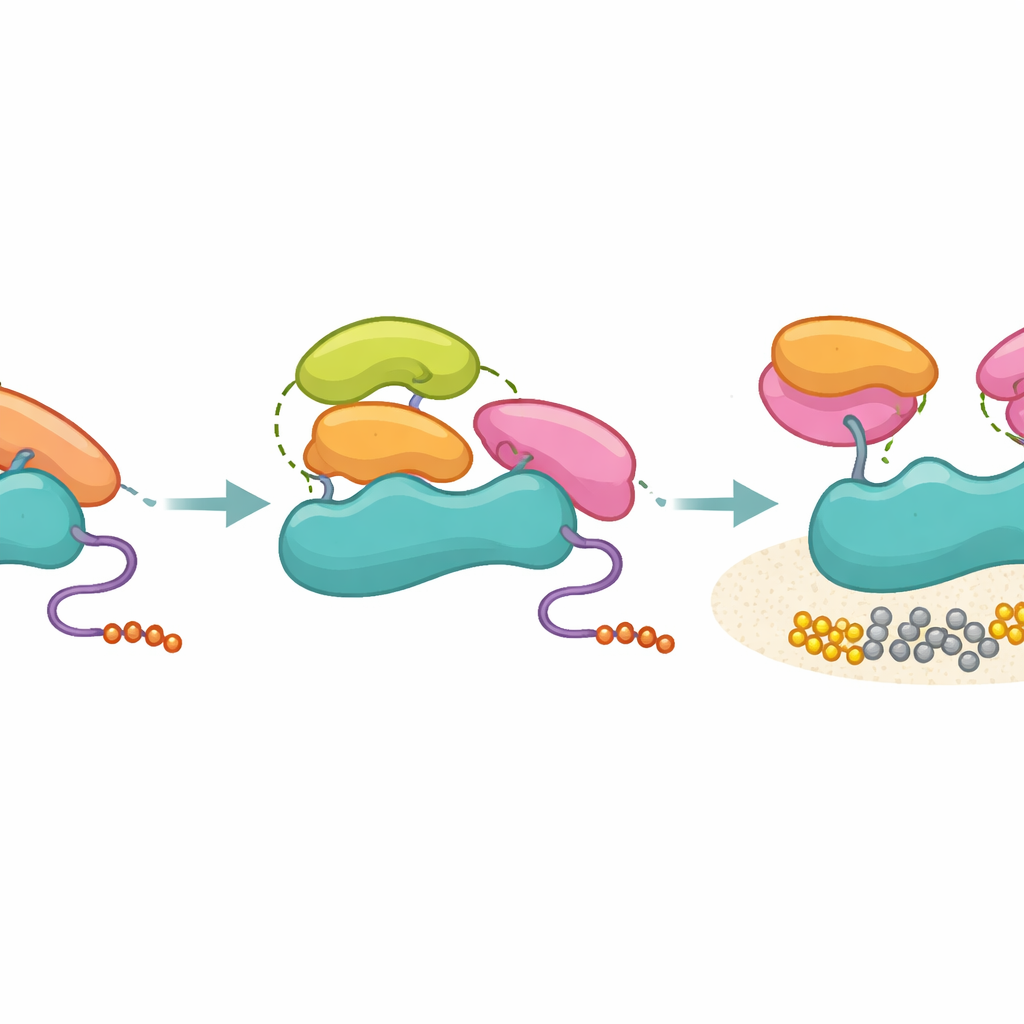
ما معنى هذا للمرض وتصميم الأدوية
تقترح هذه الدراسة نموذجًا يكون فيه p85 بمثابة مرشح جزيئي: فهو لا يمنع ارتباط العديد من مجالات SH3، لكنه يسمح فقط لأولئك القادرين على إحداث التلامسات الثلاثية ثلاثية الأبعاد الصحيحة بأن يفتحوا PI3K فعليًا. بمصطلحات يومية، كثير من المفاتيح تدخل في ثقب القفل، لكن القليل فقط يصطف داخليًا بحيث يدير الدبابيس الداخلية بما يكفي لتدوير القفل. يساعد هذا الفصل بين الارتباط والتفعيل في الحفاظ على دقة الإشارة في بيئة الخلية المزدحمة ويشرح كيف يمكن لوحدات SH3 "المنفتحة" أن تفضي إلى نتائج وظيفية محددة. قد توجهنا فهم قواعد التلامس الثلاثي هذه نحو أدوية تحاكي أو تحجب سطوح SH3 المنشّطة، ما يفتح استراتيجيات جديدة لضبط إشارات PI3K في السرطانات وغيرها من الأمراض المدفوعة بـ PI3K.
الاستشهاد: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
الكلمات المفتاحية: كيناز PI3, إشارة البروتين, مجال SH3, بيولوجيا السرطان, التفاعلات الجزيئية