Clear Sky Science · sv
SH3-domäner aktiverar selektivt PI3-kinas genom okonventionella tertiära kontakter
Hur celler håller tillväxtsignaler under kontroll
Våra celler beslutar ständigt om de ska växa, dela sig eller förbli inaktiva. En nyckelaktör i denna process är ett enzym som kallas PI3-kinas (PI3K), som hjälper till att styra cellmetabolism och överlevnad och ofta är överaktivt vid cancer. Denna studie ställer en subtil men viktig fråga: när så många lika molekylära ”kontaktstycken” trängs i cellen, hur skiljer PI3K mellan harmlösa möten och de få som faktiskt slår om den från "av" till "på"? Svaret blottlägger ett dolt lager av selektivitet som kan hjälpa till att utforma mer precisa cancerterapier.
Många lika pluggar, bara några verkliga strömbrytare
Celler är fulla av återanvändbara byggstenar kallade proteindomäner—kompakta moduler som binder korta sträckor av andra proteiner. En utbredd familj, SH3-domänerna, känner igen enkla prolinrika motiv som är mycket vanliga i det humana proteomet. Eftersom dessa motiv är så talrika och SH3-domäner binder dem svagt och något indiscriminant, har det varit gåtfullt hur SH3-innehållande proteiner deltar i högspecifika signalvägar utan att skapa kaos. Denna gåta är särskilt akut för PI3K, vars felaktiga aktivering driver cancer och andra sjukdomar. Tidigare arbete visade att den regulatoriska subenheten av PI3K, kallad p85, kan aktiveras av SH3-domäner från vissa Src-familjekinaser, men inte andra, trots att många av dessa SH3-domäner känner igen liknande prolinrika taggar.
De dolda hjälpkontakterna på PI3K-strömbrytaren
Författarna fokuserade på hur SH3-domäner från olika proteiner interagerar med p85 och hur detta påverkar PI3K-aktivitet. Med precisa bindningsmätningar och strukturella metoder jämförde de interaktionen mellan Fyns SH3-domän och en kort prolinrik peptid från p85 med interaktionen mot nästan fullängds p85. Medan den korta peptiden engagerade Fyn på ett standardiserat sätt, band den fullständiga p85-fragmentet tätare och med en annan energisignatur, vilket antydde att extra ytor kom i spel. Genom att dissekera p85 i delar och återbygga den som chimärer visade teamet att dess C-terminala regioner—de två SH2-domänerna och den ihopvridna iSH2-segmentet som normalt klämmer runt den katalytiska p110-partnern—också deltar i denna utvidgade, eller "tertiära", kontakt med SH3.
Två små platser som avgör mellan bindning och aktivering
Nukleär magnetisk resonanskartläggning visade vilka delar av Fyns SH3-domän som påverkas mest när den binder fullängds p85. Två positioner framträdde: en nära den vanliga prolinbindande fåran (kallad PR-proximal plats) och en annan på motsatt sida av domänen (en PR-distal plats). Muteringar på dessa positioner förändrade knappt hur väl SH3 grep tag i den enkla prolinrika peptiden, men ändrade dramatiskt hur den engagerade fullängds p85 och, avgörande, hur mycket PI3K-aktivitet den utlöste. I cellbaserade lipidkinasassayer aktiverade vissa mutanter med måttlig affinitet faktiskt PI3K starkare än vildtypen, medan andra med liknande affinitet förlorade största delen av sin aktiverande förmåga. Detta visade att aktivering inte helt enkelt följer "hur hårt greppet är", utan beror på om SH3-domänen kan bilda rätt tertiära kontakter med båda p85:s inhibitoriska SH2-regioner och omplacera dem bort från p110.
Att skilja blott kontakt från en riktig på-knapp
Forskarna testade sedan SH3-domäner från flera andra proteiner, inklusive Hck, Grb2, p85 själv och Ubs3A, med särskild uppmärksamhet på det strukturella grannskapet kring PR-distal platsen. Alla dessa SH3-domäner kunde binda p85 med i stort sett liknande styrka, men bara de med en kompatibel hydrofob yta vid den viktiga distala positionen—som Hck och C-terminala SH3 hos Grb2—kunde slå på PI3K i biokemiska assay. Icke-aktiverande SH3-domäner, inklusive p85:s egen SH3, fäste fortfarande vid p85:s prolinrika region men lyckades inte generera det extra tertiära kontaktmönstret som krävdes för att dra de inhibitoriska SH2-domänerna åt sidan. Tvärbindnings-masspektrometri stödde denna bild: aktiverande SH3-domäner bildade fokuserade kontakter med SH2-regionerna, medan icke-aktiverande provade ett bredare spektrum av positioner, förenligt med en lösare, icke-produktiv bindning.
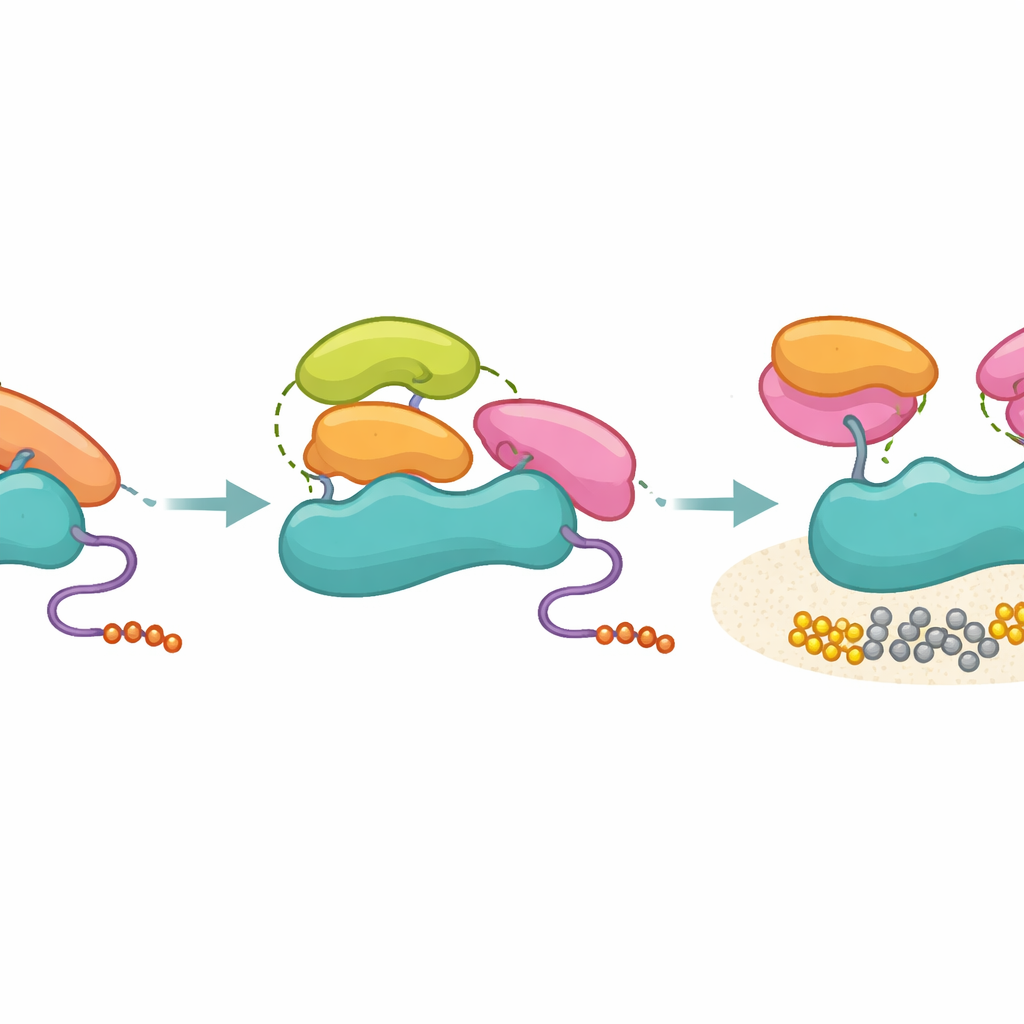
Vad detta betyder för sjukdom och läkemedelsdesign
Tillsammans föreslår arbetet en modell där p85 fungerar som ett molekylärt filter: det hindrar inte många SH3-domäner från att binda, men tillåter endast dem som kan skapa rätt tredimensionella kontakter att faktiskt låsa upp PI3K. I vardagliga termer passar många nycklar i nyckelhålet, men bara några få alignerar de inre pinnarna tillräckligt bra för att vrida låset. Denna åtskillnad mellan bindning och aktivering hjälper till att bibehålla signalnoggrannhet i cellens trånga miljö och förklarar hur annars "promiskuösa" SH3-moduler kan få specifika funktionella utfall. Att förstå dessa tertiära kontaktregler kan peka ut vägar till läkemedel som antingen imiterar eller blockerar aktiverande SH3-ytor, vilket erbjuder nya strategier för att finjustera PI3K-signalering vid cancer och andra PI3K-drivna sjukdomar.
Citering: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
Nyckelord: PI3-kinas, proteinsignalering, SH3-domän, cancerbiologi, molekylära interaktioner