Clear Sky Science · de
SH3-Domänen aktivieren selektiv die PI3-Kinase durch unkonventionelle tertiäre Kontakte
Wie Zellen Wachstumssignale unter Kontrolle halten
Unsere Zellen entscheiden fortlaufend, ob sie wachsen, sich teilen oder ruhig bleiben. Ein wichtiger Entscheider in diesem Prozess ist ein Enzym namens PI3-Kinase (PI3K), das Stoffwechsel und Überleben der Zelle steuert und bei Krebs häufig überaktiv ist. Diese Studie stellt eine feine, aber wichtige Frage: Wenn so viele ähnliche molekulare „Stecker und Buchsen“-Teile die Zelle bevölkern, wie unterscheidet PI3K harmlose Begegnungen von den wenigen, die es tatsächlich von „aus“ auf „an“ schalten? Die Antwort offenbart eine versteckte Selektivitätsebene, die helfen könnte, präzisere Krebstherapien zu entwickeln.
Viele ähnliche Stecker, nur wenige echte Schalter
Zellen sind voller wiederverwendbarer Bausteine, so genannter Protein-Domänen—kompakter Module, die an kurze Abschnitte anderer Proteine binden. Eine weit verbreitete Familie, die SH3-Domänen, erkennt einfache prolinreiche Motive, die im menschlichen Proteom sehr häufig vorkommen. Da diese Motive so zahlreich sind und SH3-Domänen sie nur schwach und relativ unspezifisch binden, war lange unklar, wie SH3-haltige Proteine in hochspezifischen Signalwegen mitwirken können, ohne Chaos zu verursachen. Dieses Rätsel ist besonders relevant für PI3K, deren falsche Aktivierung Krebs und andere Krankheiten antreibt. Frühere Arbeiten zeigten, dass die regulatorische Untereinheit von PI3K, genannt p85, von SH3-Domänen bestimmter Src-Familien-Kinasen eingeschaltet werden kann, aber nicht von anderen—obwohl viele dieser SH3-Domänen ähnliche prolinreiche Tags erkennen.
Die verborgenen Helfer-Kontakte am PI3K-Schalter
Die Autoren konzentrierten sich darauf, wie SH3-Domänen verschiedener Proteine mit p85 interagieren und wie dies die PI3K-Aktivität beeinflusst. Mit präzisen Bindungsmessungen und Strukturmethoden verglichen sie die Wechselwirkung der Fyn-SH3-Domäne mit einem kurzen prolinreichen Peptid aus p85 gegenüber nahezu volllänglichem p85. Während das kurze Peptid Fyn auf die übliche Weise ansprach, band das vollständige p85-Fragment stärker und mit einem anderen energetischen Profil, was darauf hindeutete, dass zusätzliche Oberflächen ins Spiel kamen. Durch Zerlegung von p85 in Teile und Wiederaufbau als Chimären zeigte das Team, dass seine C-terminalen Regionen—die beiden SH2-Domänen und das coil‑förmige iSH2-Segment, das normalerweise das katalytische p110-Partner einklemmt—ebenfalls an diesem erweiterten bzw. „tertären“ Kontakt mit SH3 beteiligt sind.
Zwei winzige Stellen, die zwischen Bindung und Aktivierung entscheiden
NMR-Experimente (Kernspinresonanz) kartierten, welche Teile der Fyn-SH3-Domäne am stärksten gestört werden, wenn sie vollen p85 bindet. Zwei Positionen stachen hervor: eine nahe der üblichen Prolin-Bindungstasche (genannt PR‑nahe Stelle) und eine auf der gegenüberliegenden Fläche der Domäne (eine PR‑ferne Stelle). Mutationen an diesen Positionen veränderten kaum, wie gut SH3 das einfache prolinreiche Peptid ergriff, beeinflussten aber dramatisch, wie es vollwertiges p85 ansprach und entscheidend, wie stark PI3K dadurch aktiviert wurde. In zellbasierten Lipidkinase-Assays aktivierten einige Mutanten mit mäßiger Affinität PI3K sogar stärker als der Wildtyp, während andere mit ähnlicher Affinität den Großteil ihrer Aktivierungskraft verloren. Das zeigte, dass Aktivierung nicht einfach der Frage folgt „wie fest der Griff ist“, sondern davon abhängt, ob die SH3-Domäne die richtigen tertiären Kontakte zu beiden inhibitorischen SH2-Regionen von p85 herstellen und diese vom p110 wegpositionieren kann.
Kontakt von echtem Ein‑Schalter unterscheiden
Die Forscher testeten dann SH3-Domänen aus mehreren anderen Proteinen, darunter Hck, Grb2, p85 selbst und Ubs3A, und achteten besonders auf die strukturelle Umgebung der PR‑fernen Stelle. Alle diese SH3-Domänen konnten p85 mit ähnlich großer Stärke binden, doch nur diejenigen mit einem kompatiblen hydrophoben Fleck an der kritischen distalen Position—wie Hck und die C-terminale SH3 von Grb2—konnten PI3K in biochemischen Assays aktivieren. Nicht-aktivierende SH3-Domänen, einschließlich der eigenen SH3 von p85, hefteten sich zwar an die prolinreiche Region von p85, erzeugten aber nicht das zusätzliche tertiäre Kontaktmuster, das nötig ist, um die inhibitorischen SH2-Domänen wegzuziehen. Crosslinking-Massenspektrometrie stützte dieses Bild: aktivierende SH3-Domänen bildeten fokussierte Kontakte mit den SH2-Regionen, während nicht-aktivierende eine breitere Palette von Positionen ausloteten, was mit einer lockereren, nicht-produktiven Anheftung übereinstimmt.
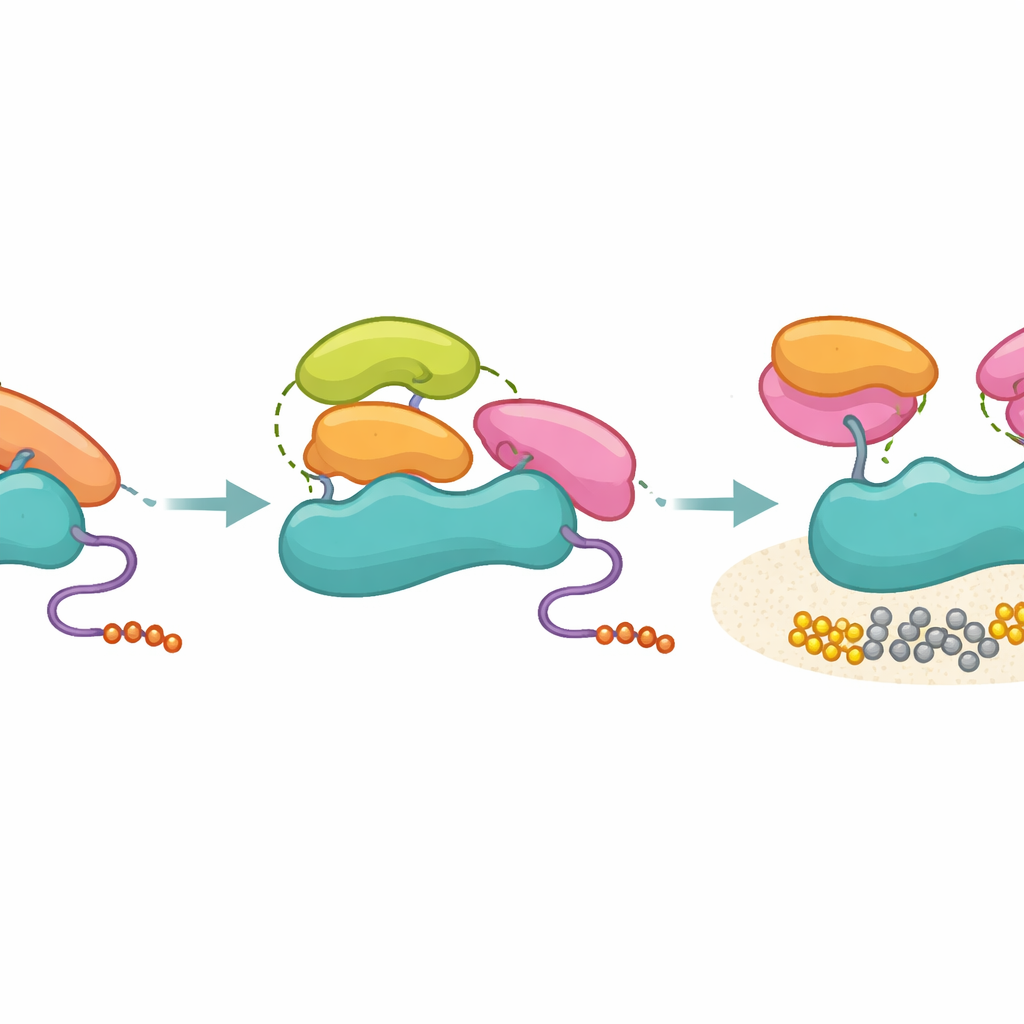
Was das für Krankheit und Wirkstoffdesign bedeutet
Zusammengefasst schlagen die Autoren ein Modell vor, in dem p85 als molekularer Filter wirkt: Es verhindert nicht, dass viele SH3-Domänen binden, lässt aber nur diejenigen zu, die die richtigen dreidimensionalen Kontakte herstellen, tatsächlich die PI3K zu entriegeln. Alltäglich ausgedrückt: Viele Schlüssel passen ins Schlüsselloch, aber nur einige richten die inneren Stifte so aus, dass das Schloss sich dreht. Diese Trennung von bloßem Kontakt und Aktivierung hilft, Signalfähigkeit in der überfüllten Zellumgebung zu bewahren und erklärt, wie sonst „promiskuitive“ SH3-Module spezifische funktionelle Ergebnisse liefern können. Das Verständnis dieser Regeln tertiärer Kontakte könnte den Weg zu Medikamenten weisen, die entweder aktivierende SH3‑Oberflächen nachahmen oder blockieren und so neue Strategien bieten, PI3K-Signale bei Krebs und anderen PI3K‑getriebenen Erkrankungen zu modulieren.
Zitation: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
Schlüsselwörter: PI3-Kinase, Proteinsignalgebung, SH3-Domäne, Krebsbiologie, molekulare Interaktionen