Clear Sky Science · he
דומיינים SH3 מפעילים בצורה סלקטיבית את ה‑PI3 קינאז דרך מגעים שלישוניים לא‑קונבנציונליים
איך תאים שומרים על אותות הגדילה תחת שליטה
התאים שלנו כל הזמן מקבלים החלטות האם לגדול, להתחלק או להישאר שקטים. מקבל החלטות מרכזי בתהליך הזה הוא האנזים PI3 קינאז (PI3K), שמווסת מטבוליזם ובטיחות התא ותדיר פעילותו מוגברת בסרטן. המחקר בחן שאלה עדינה אך חשובה: כאשר כל כך הרבה חלקים מולקולריים דמויים־פלאג־ושקע צופפים בתא, איך PI3K מבחין בין מפגש תמים לבין אותו מפגש שבאמת מפעיל אותו מ״כבוי״ ל״פועל״? התשובה מגלה שכבת סלקטיביות נסתרת שיכולה לסייע בעיצוב טיפולים מדויקים יותר לסרטן.
המון תקעים דומים, רק כמה מהם מממשים את המתג
תאים מלאים בלבנים חוזרות הנקראות דומייני חלבון — מודולים קומפקטיים שקושרים רצפים קצרים של חלבונים אחרים. משפחה רחבה אחת, דומייני ה‑SH3, מזהה מוטיבים עשירים בפרולין הנפוצים מאוד בפרוטאום האנושי. מכיוון שמוטיבים אלה שופעים ודומייני SH3 נקשרים אליהם בחולשה ובאופן יחסית לא־דיסקרמינטיבי, זה היה דבר מבלבל איך חלבונים הכוללים SH3 משתתפים במסלולי איתות ספציפיים מבלי לייצר כאוס. לפאזל הזה יש חשיבות מיוחדת עבור PI3K, שכן הפעלה לא מבוקרת שלו מניעה סרטן ומחלות נוספות. עבודות קודמות הראו שהתת־יחידה הרגולטורית של PI3K, p85, יכולה להיות מוּפְעֶלֶת על‑ידי דומייני SH3 מחלק מבני משפחת Src, אך לא על‑ידי אחרים, אף על פי שרבים מה‑SH3 הללו מזהים תגי פרולין דומים.
המגעים העוזרים הנסתרים במתג של PI3K
המחברים התמקדו באופן שבו דומייני SH3 מחלבונים שונים מתקשרים עם p85 וכיצד זה משפיע על פעילות PI3K. באמצעות מדידות קשירה מדויקות ושיטות מבניות השוו בין אינטראקציה של דומיין ה‑Fyn SH3 עם פפטיד קצר עשיר בפרולין מ‑p85 לבין אינטראקציה עם מקטע של p85 כמעט בשלמותו. בעוד שהפפטיד הקצר התקשר ל‑Fyn בצורה סטנדרטית, מקטע p85 המלא התקשר בחוזקה רבה יותר ובחתימת אנרגיה שונה, מה שעורר חשד שמשטחים נוספים נדרשים. על ידי פירוק p85 לחתיכות והרכבתם כחיאמרות, הראו החוקרים שאזורי C‑טרמינל שלו — שני דומייני ה‑SH2 ומקטע ה‑iSH2 המקופל שמצמיד בדרך כלל את השותף הקטליטי p110 — גם הם משתתפים במגע המשולש המורחב עם ה‑SH3.
שתי נקודות זעירות שמחליטות בין קשירה להדלקה
ניסויי תהודה מגנטית גרעינית מיפו אילו חלקים בדומיין ה‑Fyn SH3 מופרעים ביותר כאשר הוא נקשר ל‑p85 המלא. שתי עמדות בלטו: אחת סמוך לשקע הקשור בפרולין הרגיל (הנקודה הקרובה ל‑PR) ואחרת על פניו הנגדית של הדומיין (נקודת PR‑מרוחקת). מוטציות בעמדות אלה כמעט ולא שינו את חוזק הקשירה של ה‑SH3 לפפטיד הפרוליני הפשוט, אך שינו באופן דרמטי כיצד הוא מתקשר ל‑p85 בשלמותו ובמיוחד כמה פעילות PI3K נגרמת. בבדיקות קינאזת ליפידים בתאים, חלק מהמוטנטים עם אפיניות צנועה הפעלו בפועל את PI3K חזק יותר מסוג הבר ורבים אחרים עם אפיניות דומה איבדו את יכולת ההפעלה שלהם. ממצא זה הראה שההפעלה אינה פשוטה פונקציה של "כמה חזק החיבור", אלא תלויה ביכולת דומיין ה‑SH3 ליצור את המגעים השלישוניים המתאימים עם שני אזורי ה‑SH2 המעכבים של p85 ולהזיזם משם הרחק מ‑p110.
להבחין בין מגע בלבד לבין מתג אמיתי
בהמשך בחנו החוקרים דומייני SH3 ממספר חלבונים נוספים, כולל Hck, Grb2, p85 עצמו ו‑Ubs3A, ותשומת הלב הופנתה במיוחד לשכנות המבנית של נקודת ה‑PR‑מרוחקת. כל דומייני ה‑SH3 הללו יכלו לקשור את p85 בעוצמת קשירה בדויה דומה, אך רק אלה עם מדור היגרופי תואם בעמדה המרוחקת — כמו Hck וה‑SH3 הטרמינלי של Grb2 — הצליחו להדליק את PI3K בבדיקות ביוכימיות. דומייני SH3 שלא הפעלו, כולל ה‑SH3 של p85 עצמו, עדיין התחברו לאזור העשיר בפרולין של p85 אך נכשלו ביצירת דפוס המגע השלישוני הנוסף שנחוץ להזזת דומייני ה‑SH2 המעכבים. מיסוי־מסה עם קרוס‑לינקינג תמך בפרשנות זו: דומייני SH3 מעוררי היו יוצרים מגעים ממוקדים עם אזורי ה‑SH2, בעוד שהלא־מעוררים דגמו מגוון רחב יותר של עמדות, בהתאמה לקשירה רופפת ולא־מועילה.
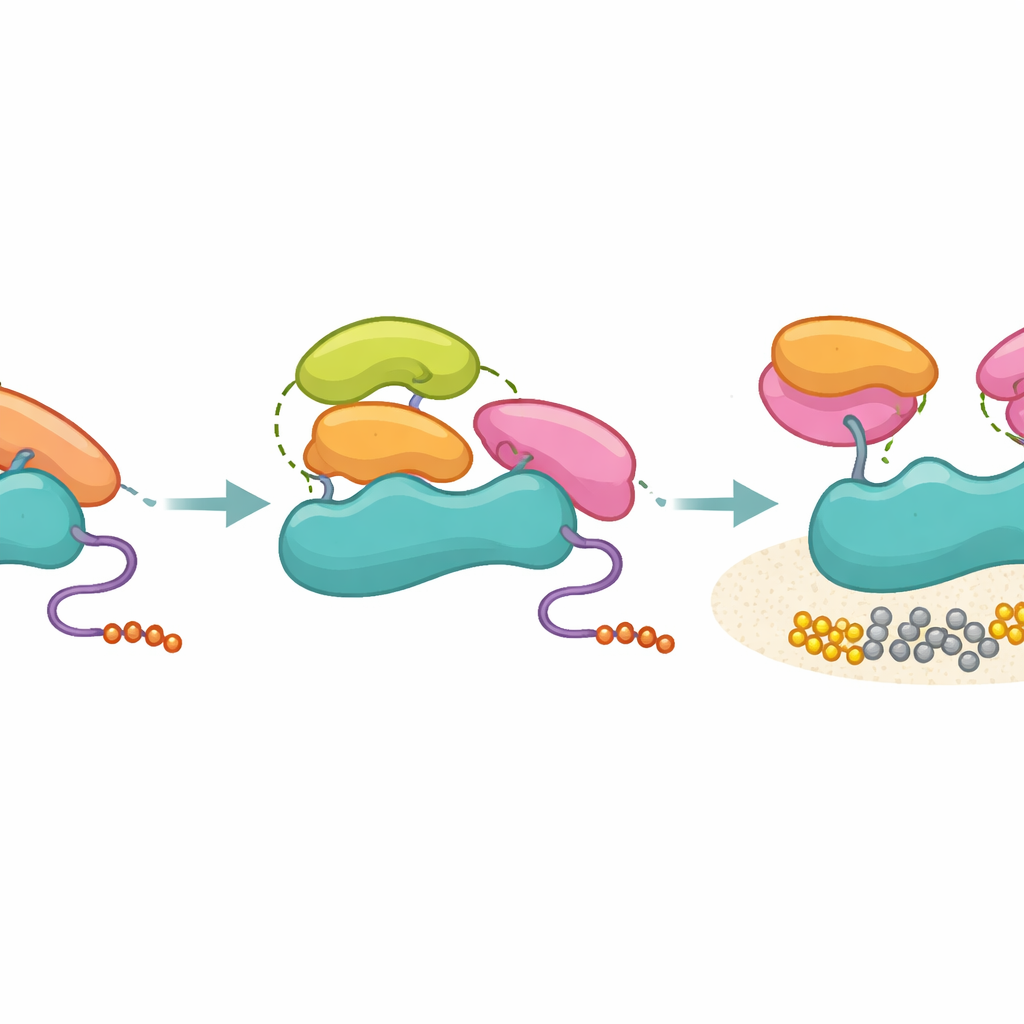
מה משמעות הדבר למחלה ולעיצוב תרופות
כולל, העבודה מציעה מודל שבו p85 פועל כמסננת מולקולרית: הוא אינו מונע ממספר רב של דומייני SH3 להיקשר, אך מאפשר רק לאלה שיכולים לבצע את המגעים התלת־ממדיים הנכונים לשחרר בפועל את PI3K. במילים פשוטות, הרבה מפתחות נכנסות לחלון המנעול, אך רק מעטים מיישרים מספיק את הסיכות הפנימיות כדי לסובב את המנעול. ההבחנה בין קשירה להדלקה עוזרת לשמור על דיוק האיתות בסביבה הצפופה של התא ומסבירה כיצד מודולי SH3 שנראים "פרומיסקואיים" יכולים עדיין להניב תוצאות פונקציונליות ספציפיות. הבנת כללי המגעים השלישוניים האלה עשויה להצביע על דרכים לפתח תרופות החולמות או חוסמות משטחים של SH3 מעוררי, ובכך להציע אסטרטגיות חדשות לכוונון איתות ה‑PI3K בסרטנים ומחלות נוספות מונעות‑PI3K.
ציטוט: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
מילות מפתח: PI3 קינאז, אותות חלבונים, דומיין SH3, ביולוגיה של הסרטן, אינטראקציות מולקולריות