Clear Sky Science · ru
Домены SH3 избирательно активируют PI3-киназу через нетрадиционные третичные контакты
Как клетки держат сигналы роста под контролем
Наши клетки постоянно принимают решения: расти, делиться или сохранять покой. Ключевым регулятором в этом процессе является фермент PI3-киназа (PI3K), который помогает контролировать метаболизм и выживание клетки и часто гиперактивен при раке. В этом исследовании рассматривается тонкий, но важный вопрос: когда в клетке полно похожих молекулярных «штекеров» и «розеток», как PI3K отличает безвредные контакты от тех немногих, которые действительно переключают его с «выключено» на «включено»? Ответ открывает скрытый уровень селективности, который может помочь в разработке более точных противораковых терапий.
Много похожих штекеров, лишь несколько настоящих переключателей
Клетки заполнены многоразовыми строительными блоками — белковыми доменами: компактными модулями, связывающими короткие участки других белков. Одна широко распространённая семья, домены SH3, распознаёт простые пролин-богатые мотивы, которые очень распространены в человеческом протеоме. Поскольку эти мотивы повсюду, а SH3-домены связываются с ними слабо и относительно недифференцировано, оставалось непонятным, как белки с SH3 принимают участие в строго специфичных сигнальных путях, не создавая хаоса. Эта проблема особенно важна для PI3K: его неправильная активация вызывает рак и другие болезни. Ранее показывали, что регуляторная субъединица PI3K, называемая p85, может активироваться SH3-доменами некоторых киноз семейства Src, но не других, хотя многие из этих SH3 распознают схожие пролин-богатые метки.
Скрытые вспомогательные контакты на переключателе PI3K
Авторы сосредоточились на том, как SH3-домены из разных белков взаимодействуют с p85 и как это влияет на активность PI3K. С помощью точных измерений связывания и структурных методов они сравнили взаимодействие SH3-домена Fyn с коротким пролин-богатым пептидом из p85 и с почти полноразмерным фрагментом p85. Если короткий пептид взаимодействовал с Fyn привычным образом, то более полный фрагмент p85 связывался прочнее и с отличающейся энергетической подписью, что указывает на участие дополнительных поверхностей. Разрезая p85 на части и собирая его в химерные конструкции, команда показала, что его карбоновая (C-концевая) область — две SH2-домены и спиральный участок iSH2, который обычно зажимает каталитическую субединицу p110 — также участвуют в этом расширенном, или «третичном», контакте с SH3.
Две крошечные точки, решающие между связыванием и активацией
Эксперименты с ядерно-магнитным резонансом показали, какие участки SH3-домена Fyn наиболее нарушаются при связывании с полноценным p85. Выделились две позиции: одна рядом с обычной бороздой для связывания пролина (обозначенная как PR-близкая), и другая на противоположной грани домена (PR-дистальная). Мутации в этих позициях почти не меняли, насколько сильно SH3 удерживал простой пролин-богатый пептид, но существенно меняли его взаимодействие с полноразмерным p85 и, что важно, насколько сильно это вызывало активность PI3K. В клеточных тестах липидкиназ некоторые мутанты с умеренным сродством активировали PI3K сильнее, чем дикий тип, тогда как другие с похожим сродством теряли большую часть своей активационной способности. Это показало, что активация не следует простому правилу «чем сильнее захват, тем сильнее активация», а зависит от того, может ли SH3 сформировать правильные третичные контакты с обеими ингибирующими SH2-областями p85 и отдалить их от p110.
Отделение простого контакта от настоящего включения
Затем исследователи протестировали SH3-домены нескольких других белков, включая Hck, Grb2, сам p85 и Ubs3A, уделяя особое внимание структурному окружению PR-дистальной позиции. Все эти SH3-домены могли связываться с p85 с примерно схожей силой, но только те, у которых в ключевой дистальной позиции был совместимый гидрофобный участок — как у Hck и C-концевого SH3 домена Grb2 — могли включать PI3K в биохимических тестах. Неактивирующие SH3-домены, включая собственный SH3 p85, всё же прикреплялись к пролин-богатому участку p85, но не образовывали дополнительных третичных контактов, необходимых, чтобы оттянуть ингибирующие SH2-домены. Кросслинкинг с последующим масс-спектрометрическим анализом подтвердил эту картину: активирующие SH3 формировали сфокусированные контакты с SH2-регионами, тогда как неактивирующие охватывали более широкий набор позиций, что согласуется с более рыхлым, непродуктивным присоединением.
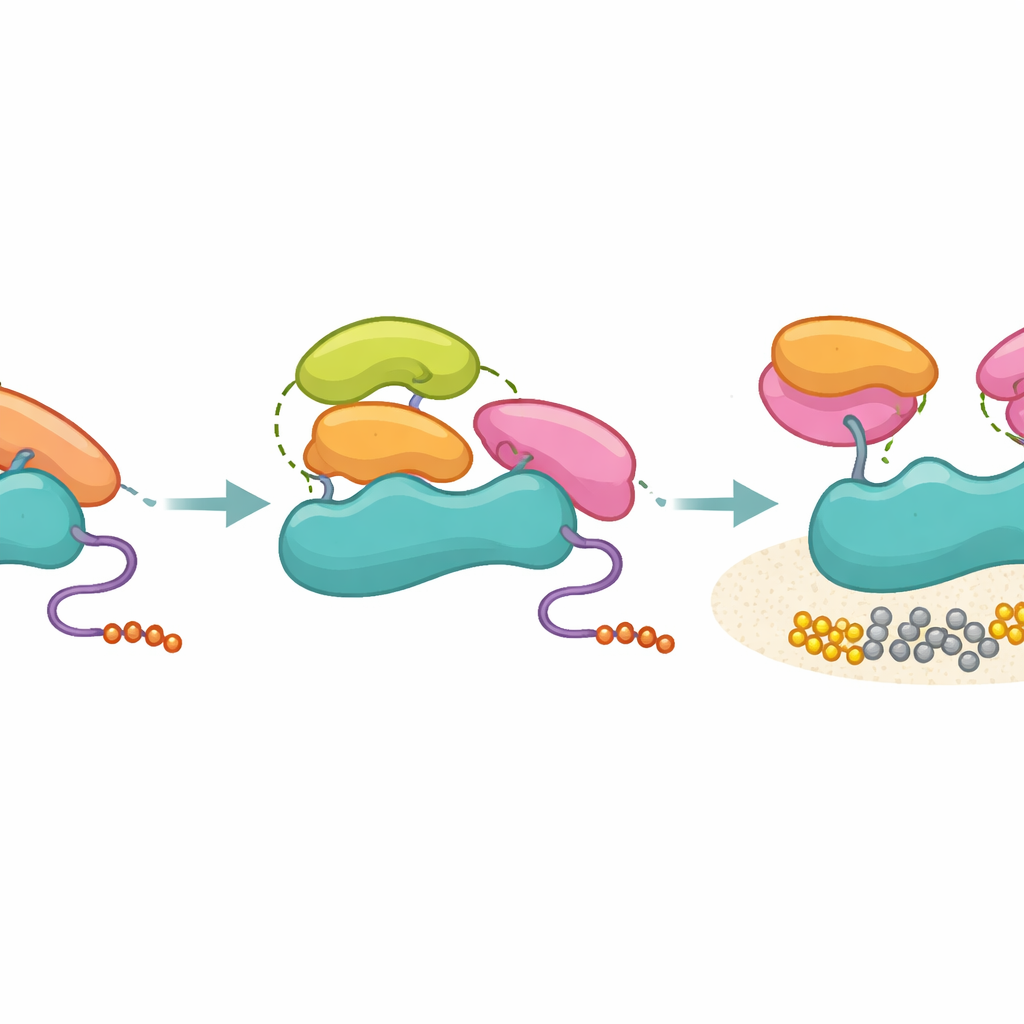
Что это значит для болезней и дизайна лекарств
Вместе взятые результаты предлагают модель, в которой p85 действует как молекулярный фильтр: он не препятствует многим SH3-доменам связываться, но пропускает дальше только те, которые способны установить нужные трёхмерные контакты, чтобы действительно разблокировать PI3K. В обиходной аналогии: множество ключей входят в замочную скважину, но лишь немногие выравнивают внутренние штифты достаточно точно, чтобы повернуть замок. Такое разделение связывания и активации помогает поддерживать точность сигналов в переполненной молекулами среде клетки и объясняет, как в противном случае «промискуитетные» модули SH3 могут давать специфические функциональные результаты. Понимание правил этих третичных контактов может указать путь к разработке препаратов, которые либо имитируют, либо блокируют активирующие поверхности SH3, предлагая новые стратегии настройки сигнального пути PI3K при раке и других заболеваниях, зависимых от PI3K.
Цитирование: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
Ключевые слова: PI3-киназа, белковая сигнализация, домен SH3, онкобиология, молекулярные взаимодействия