Clear Sky Science · nl
SH3‑domeinen activeren selectief de PI3‑kinase via niet‑conventionele tertiaire contacten
Hoe cellen groeisignalen onder controle houden
Onze cellen beslissen voortdurend of ze moeten groeien, delen of inactief blijven. Een belangrijke beslisser in dit proces is een enzym dat PI3‑kinase (PI3K) heet; het reguleert celmetabolisme en overleving en is vaak overactief bij kanker. Deze studie stelt een subtiele maar belangrijke vraag: wanneer zoveel vergelijkbare moleculaire ‘stekkers en stopcontacten’ de cel bevolken, hoe kan PI3K onschuldige ontmoetingen onderscheiden van de enkele interacties die het daadwerkelijk van “uit” naar “aan” schakelen? Het antwoord onthult een verborgen selectiviteitslaag die kan helpen bij het ontwerpen van preciezere kankertherapieën.
Veel vergelijkbare stekkers, slechts een paar echte schakelaars
Cellen zitten vol herbruikbare bouwstenen genaamd proteïnedomeinen — compacte modules die binden aan korte sequenties van andere eiwitten. Een wijdverspreide familie, de SH3‑domeinen, herkent eenvoudige proline‑rijke motieven die zeer veel voorkomen in het humane proteoom. Omdat deze motieven zo talrijk zijn en SH3‑domeinen er slechts zwak en enigszins onselectief aan binden, is het een raadsel hoe SH3‑bevatte eiwitten toch deelnemen aan zeer specifieke signaalroutes zonder wanorde te veroorzaken. Dit probleem is vooral urgent voor PI3K, waarvan verkeerde activatie kanker en andere ziekten aandrijft. Eerder werk liet zien dat de regulerende subeenheid van PI3K, p85 genoemd, geactiveerd kan worden door SH3‑domeinen van bepaalde Src‑familie kinases, maar niet door andere, ook al herkennen veel van die SH3‑domeinen vergelijkbare proline‑rijke tags.
De verborgen hulpcontacten op de PI3K‑schakelaar
De auteurs richtten zich op hoe SH3‑domeinen van verschillende eiwitten met p85 interageren en hoe dit PI3K‑activiteit beïnvloedt. Met precieze bindingsmetingen en structurele methoden vergeleken ze de interactie van het Fyn SH3‑domein met een kort proline‑rijk peptide uit p85 tegenover bijna het volledige p85. Terwijl het korte peptide Fyn op de gebruikelijke manier aansprak, bond het volledige p85‑fragment sterker en met een ander energetisch signatuur, wat suggereerde dat extra oppervlakken een rol speelden. Door p85 in stukken te knippen en als chimera’s weer op te bouwen, toonde het team aan dat de C‑terminale gebieden — de twee SH2‑domeinen en het coiled iSH2‑segment dat normaal het katalytische p110‑partner vastklemt — ook deelnemen aan dit uitgebreide, ofwel “tertiaire”, contact met SH3.
Twee kleine plekjes die beslissen tussen binden en activeren
Protonenresonantie‑(NMR)experimenten brachten in kaart welke delen van het Fyn SH3‑domein het meest verstoord raken wanneer het aan volledig p85 bindt. Twee posities staken er uit: één nabij de gebruikelijke proline‑bindende groeve (het PR‑proximale gebied) en een andere aan de tegenoverliggende zijde van het domein (een PR‑distale site). Mutaties op deze posities veranderden nauwelijks hoe goed SH3 het eenvoudige proline‑rijke peptide pakte, maar beïnvloedden dramatisch hoe het volledige p85 vastpakte en, cruciaal, hoeveel PI3K‑activiteit daarmee werd opgewekt. In celgebaseerde lipidekinase‑assays activeerden sommige mutanten met matige affiniteit PI3K sterker dan het wildtype, terwijl andere met vergelijkbare affiniteit het grootste deel van hun activerende vermogen verloren. Dit toonde aan dat activatie niet eenvoudigweg afhangt van “hoe strak de greep is”, maar van de vraag of het SH3‑domein de juiste tertiaire contacten kan vormen met beide remmende SH2‑regioenen van p85 en deze zodanig kan herpositioneren dat ze p110 vrijgeven.
Een gewoon contact scheiden van een echte aan‑schakelaar
De onderzoekers testten vervolgens SH3‑domeinen van meerdere andere eiwitten, waaronder Hck, Grb2, p85 zelf en Ubs3A, met speciale aandacht voor de structurele omgeving van de PR‑distale site. Al deze SH3‑domeinen konden p85 binden met globaal vergelijkbare sterkte, maar alleen die met een compatibele hydrofobe patch op de sleutelpositie distaal — zoals Hck en het C‑terminale SH3 van Grb2 — konden PI3K in biochemische assays inschakelen. Niet‑activerende SH3‑domeinen, waaronder het eigen SH3 van p85, kleefden nog aan de proline‑rijke regio van p85 maar slaagden er niet in het extra tertiaire contactpatroon te vormen dat nodig is om de remmende SH2‑domeinen weg te trekken. Crosslinking‑massaspectrometrie ondersteunde dit beeld: activerende SH3‑domeinen vormden gerichte contacten met de SH2‑gebieden, terwijl niet‑activerende domeinen een breder scala aan posities afzochten, wat past bij een lossere, niet‑productieve bevestiging.
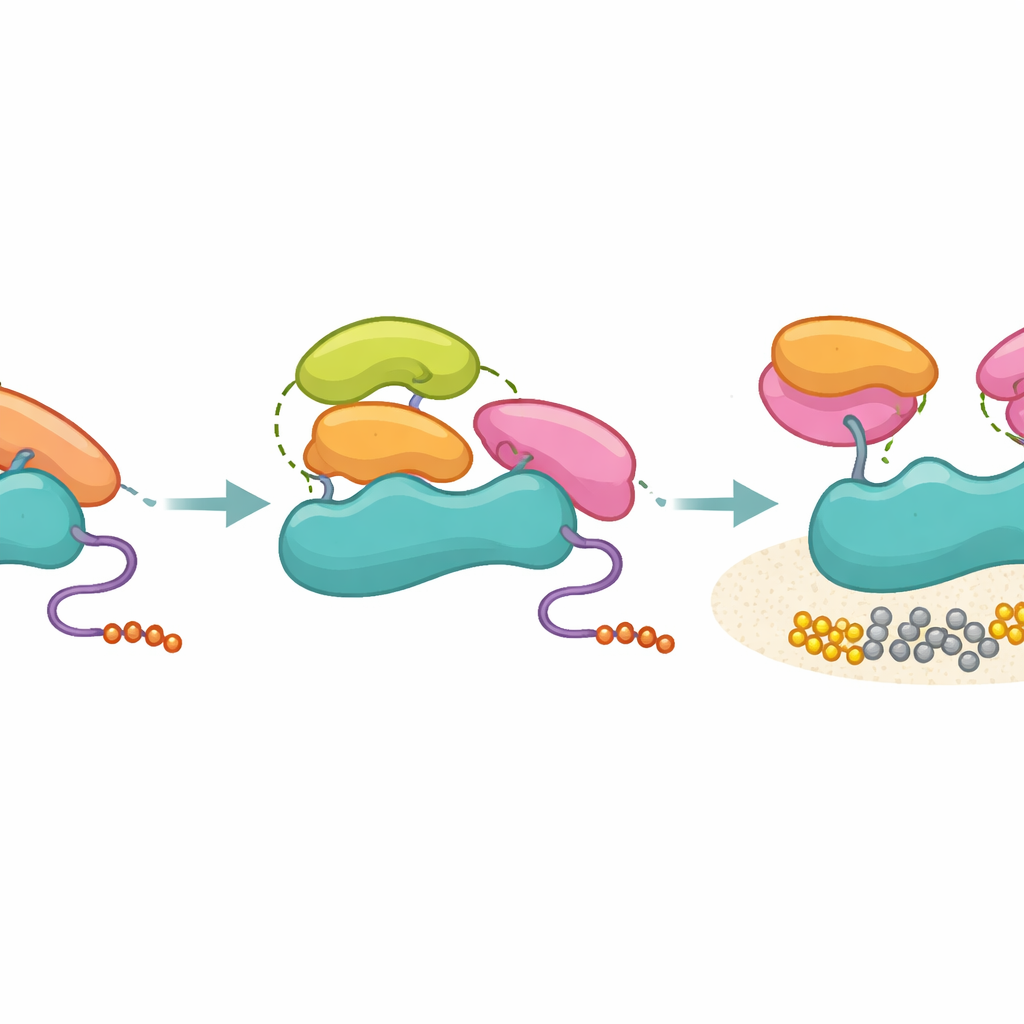
Wat dit betekent voor ziekte en geneesmiddelenontwerp
Gezamenlijk stelt het werk een model voor waarin p85 als een moleculair filter fungeert: het voorkomt niet dat veel SH3‑domeinen binden, maar het laat alleen degenen toe die de juiste driedimensionale contacten kunnen maken om PI3K echt te ontgrendelen. In gewone bewoordingen passen veel sleutels in het sleutelgat, maar slechts enkelen lijnen de interne pinnetjes goed genoeg uit om het slot om te draaien. Deze scheiding van binden en activeren helpt de signaalnauwkeurigheid te bewaren in de drukbevolkte omgeving van de cel en verklaart hoe anderszins “promiscue” SH3‑modules specifieke functionele uitkomsten kunnen hebben. Inzicht in deze regels voor tertiaire contacten kan wijzen op geneesmiddelen die activerende SH3‑oppervlakken nabootsen of blokkeren, en zo nieuwe strategieën bieden om PI3K‑signaaltransductie te sturen bij kanker en andere PI3K‑gedreven ziekten.
Bronvermelding: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
Trefwoorden: PI3 kinase, proteïnesignalering, SH3‑domein, kankerbiologie, moleculaire interacties