Clear Sky Science · ja
非従来型の三次接触を介してPI3キナーゼを選択的に活性化するSH3ドメイン
細胞は増殖シグナルをどう制御しているか
私たちの細胞は常に増殖するか、分裂するか、あるいは静止するかを選択しています。この過程の重要な決定因子の一つがPI3キナーゼ(PI3K)という酵素で、細胞の代謝や生存を制御し、がんではしばしば過剰に活性化されます。本研究は微妙だが重要な問いを立てます:多くの類似した「プラグとソケット」的な部品が細胞内にひしめく中で、PI3Kは無害な出会いと実際にそれを「オフ」から「オン」に切り替える数少ない出会いをどう区別しているのか?その答えは、より精密ながん治療の設計に役立ちうる隠れた選択性の層を明らかにします。
似たプラグは多いが、本当のスイッチはごくわずか
細胞は短い配列に結合するコンパクトなモジュールであるタンパク質ドメインという再利用可能な構成要素で満たされています。広く存在するファミリーの一つであるSH3ドメインは、プロリンを豊富に含む単純なモチーフを認識しますが、これらのモチーフはヒトプロテオーム全体で非常に一般的です。これらのモチーフが多数存在し、SH3ドメインの結合は弱くやや無差別であるため、SH3を含むタンパク質が特異的なシグナル伝達経路に関与して混乱を引き起こさないのはなぜかは長らく謎でした。この問題は、活性化の誤制御ががんや他の病態を引き起こすPI3Kにとって特に重要です。以前の研究では、PI3Kの調節サブユニットであるp85が、ある種のSrcファミリーキナーゼ由来のSH3ドメインにより活性化されうる一方で、他のSH3ドメインではそうならないことが示されていましたが、多くのSH3ドメインが類似したプロリン豊富なタグを認識するにもかかわらず、その違いは説明されていませんでした。
PI3Kスイッチにおける隠れた補助接触
著者らは、異なるタンパク質由来のSH3ドメインがどのようにp85と相互作用し、PI3K活性にどう影響するかに注目しました。精密な結合測定と構造解析を用いて、FynのSH3ドメインとp85の短いプロリン豊富ペプチド、およびほぼ全長のp85断片との相互作用を比較しました。短いペプチドはFynと標準的な方法で結合しましたが、より長いp85断片はより強く、かつ異なるエネルギー的特徴で結合し、追加の表面が関与していることを示唆しました。p85をさらに分解して断片を組み替えるキメラ作成によって、C末端領域──二つのSH2ドメインと通常は触媒サブユニットp110を抑制するコイル状のiSH2セグメント──もSH3との拡張された、いわゆる“三次的”接触に参加していることが示されました。
結合と活性化を決める二つの小さな位置
核磁気共鳴実験により、Fyn SH3ドメインのうち全長p85と結合したときに最も影響を受ける部位がマッピングされました。二つの位置が際立っていました:通常のプロリン結合溝の近くにある位置(PR近傍サイト)と、ドメインの反対面にある位置(PR遠位サイト)です。これらの位置を変異させても単純なプロリン豊富ペプチドに対する結合親和性はほとんど変わりませんでしたが、全長p85との関与の仕方や、重要な点としてPI3K活性をどれだけ誘導するかは劇的に変わりました。細胞ベースの脂質キナーゼアッセイでは、結合親和性が控えめな変異体の一部が野生型よりも強くPI3Kを活性化する一方で、同程度の親和性を持つ他の変異体は活性化能の大部分を失っていました。これは活性化が単に「どれだけ強く掴むか」に従うわけではなく、SH3ドメインがp85の両方の抑制的SH2領域と正しい三次接触を形成してp110からそれらを引き離せるかどうかに依存することを示しています。
単なる接触と真のオン・スイッチの分離
研究者らはHck、Grb2、p85自身、Ubs3Aなど複数の他のタンパク質からのSH3ドメインも調べ、特にPR遠位サイトの構造的近傍に注目しました。これらのSH3ドメインはいずれも概ね同様の強さでp85に結合できましたが、重要な遠位位置に適合する疎水性パッチを持つもの(HckやGrb2のC末端SH3のような)だけが生化学的アッセイでPI3Kをオンにできました。活性化しないSH3ドメイン(p85自身のSH3を含む)はp85のプロリン豊富領域には結合したものの、抑制的SH2ドメインを引き離すために必要な追加の三次接触パターンを生成することに失敗しました。架橋質量分析(クロスリンクング質量分析)はこの見解を支持しました:活性化するSH3ドメインはSH2領域と焦点を絞った接触を形成したのに対し、非活性化のものはより広範な位置を試行し、緩く生産性の低い結びつきをしていることと整合しました。
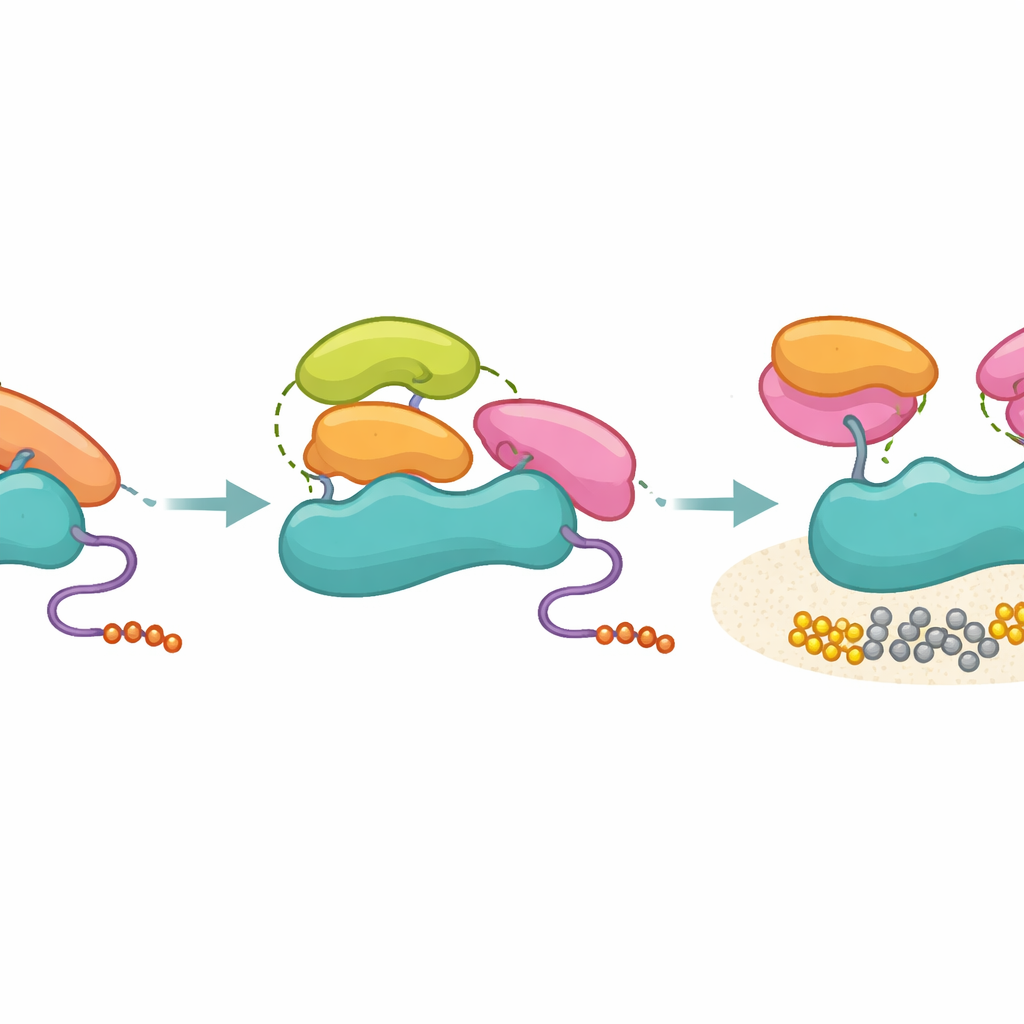
疾患と薬剤設計にとっての意義
総じて、本研究はp85が分子フィルターとして働くというモデルを提案します:多くのSH3ドメインが結合することを阻止はしないが、正しい三次元接触を形成できるものだけが実際にPI3Kのロックを解除できるのです。日常的なたとえで言えば、多くの鍵が鍵穴に入るが、内部のピンを十分に並べて回すことができる鍵はごくわずかということです。結合と活性化の分離は、混雑した細胞内環境におけるシグナルの正確性を維持し、いわゆる“多作”なSH3モジュールが特異的な機能的結果をもたらせる理由を説明します。これらの三次接触ルールを理解することは、活性化するSH3表面を模倣または遮断する薬剤の設計につながり、がんや他のPI3K駆動性疾患におけるPI3Kシグナルを調整する新たな戦略を示唆する可能性があります。
引用: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
キーワード: PI3キナーゼ, タンパク質シグナル伝達, SH3ドメイン, がん生物学, 分子相互作用