Clear Sky Science · tr
SH3 domainları, geleneksel olmayan üçüncül temaslarla PI3 kinazını seçici olarak aktive eder
Hücreler Büyüme Sinyallerini Nasıl Kontrol Altında Tutuyor
Hücrelerimiz sürekli olarak büyümeye, bölünmeye ya da sessiz kalmaya karar veriyor. Bu süreçte kilit bir karar verici, hücre metabolizmasını ve hayatta kalmayı kontrol eden ve kanserlerde sıklıkla aşırı aktifleşen bir enzim olan PI3 kinaz (PI3K) adlı enzimdir. Bu çalışma ince ama önemli bir soruyu yöneltiyor: hücrede benzer birçok moleküler “fiş ve priz” parçası bir arada iken, PI3K zararsız karşılaşmaları nasıl ayırt edip hangilerinin gerçekten onu “kapalı” durumdan “açık” duruma çevirdiğini nasıl anlıyor? Yanıt, daha hassas kanser tedavileri tasarlamaya yardımcı olabilecek gizli bir seçicilik katmanını ortaya koyuyor.
Birçok Benzer Fiş, Sadece Birkaç Gerçek Anahtar
Hücreler, diğer proteinlerin kısa bölgelerine bağlanan sağlam modüller olan protein domainleri adı verilen yeniden kullanılabilir yapı taşlarıyla doludur. Yaygın bir aile olan SH3 domainleri, insan proteomunda çok yaygın olan prolin açısından zengin motifleri tanır. Bu motifler çok bol olduğu ve SH3 domainlerinin onlara yalnızca zayıf ve bir ölçüde ayrım gözetmeden bağlandığı için, SH3 içeren proteinlerin yüksek özgüllüğe sahip sinyal yollarına nasıl zararsızlık yaratmadan katıldığı kafa karıştırıcı olmuştur. Bu bulmaca, yanlış aktive olduğunda kanser ve diğer hastalıkları tetikleyen PI3K için özellikle önemlidir. Önceki çalışmalar, PI3K’nın düzenleyici alt birimi p85’in, bazı Src-aile kinazlarının SH3 domainleri tarafından etkinleştirilebildiğini, ama diğerleri tarafından etkinleştirilemediğini göstermişti; oysa bu birçok SH3 domaini benzer prolin-zengin etiketleri tanır.
PI3K Anahtarında Gizli Yardımcı Temaslar
Yazarlar, farklı proteinlerden gelen SH3 domainlerinin p85 ile nasıl etkileştiğine ve bunun PI3K aktivitesi üzerinde nasıl bir etkisi olduğuna odaklandılar. Hassas bağlanma ölçümleri ve yapısal yöntemler kullanarak, Fyn SH3 domaininin p85’ten kısa bir prolin-zengin peptidiyle olan etkileşimini neredeyse tam uzunluktaki p85 ile karşılaştırdılar. Kısa peptit Fyn ile standart bir şekilde etkileşir görünürken, tam p85 fragmanı daha sıkı bağlandı ve farklı bir enerji imzası gösterdi; bu da ek yüzeylerin devreye girdiğine işaret ediyordu. p85’i parçalara ayırıp melezler olarak yeniden inşa ederek ekip, C-terminal bölgelerinin—katalitik p110 partnerini normalde kavrayan iki SH2 domaini ve iSH2 sarmal segmenti—aynı zamanda bu genişletilmiş ya da “üçüncül” SH3 teması içinde rol oynadığını gösterdi.
Bağlanma ile Aktivasyon Arasındaki Kararı Veren İki Küçük Bölge
Nükleer manyetik rezonans deneyleri, Fyn SH3 domaininin tam p85’e bağlandığında en çok hangi kısımlarının etkilendiğini haritaladı. İki pozisyon öne çıktı: sıradan prolin-bağlayıcı oluğun yakınındaki bir yer (PR-proksimal site olarak adlandırıldı) ve domainin karşı yüzünde bir başka bölge (PR-distal site). Bu pozisyonları mutasyona uğratmak, SH3’ün basit prolin-zengin peptidi ne kadar iyi tuttuğunu neredeyse değiştirmezken, tam uzunlukta p85 ile nasıl etkileştiğini ve önemlisi ne kadar PI3K aktivitesi tetiklediğini dramatik biçimde değiştirdi. Hücre temelli lipid kinaz deneylerinde, mütevazı afiniteye sahip bazı mutantlar aslında vahşi tipe göre PI3K’yı daha güçlü biçimde aktive ederken, benzer afiniteye sahip diğerleri aktivasyon gücünün çoğunu yitirdi. Bu, aktivasyonun basitçe “ne kadar sıkı tutuşa” göre gerçekleşmediğini; aksine SH3 domaininin p85’in inhibitör SH2 bölgeleriyle doğru üçüncül temasları kurup onları p110’dan uzaklaştırıp uzaklaştıramadığına bağlı olduğunu gösterdi.
Sadece Teması Gerçek Anahtarla Ayırmak
Araştırmacılar daha sonra Hck, Grb2, p85’in kendisi ve Ubs3A dahil olmak üzere birkaç başka proteinden SH3 domainlerini test etti ve özellikle PR-distal bölgesinin yapısal komşuluğuna dikkat ettiler. Bu SH3 domainlerinin tümü p85’e genel olarak benzer güçte bağlanabiliyordu, ancak anahtar distal pozisyonda uyumlu bir hidrofobik yama taşıyanlar—Hck ve Grb2’nin C-terminal SH3’ü gibi—biyokimyasal deneylerde PI3K’yı açabildiler. p85’in kendi SH3’ü dahil aktivasyon yapmayan SH3 domainleri hâlâ p85’in prolin-zengin bölgesine tutunuyordu ancak inhibitör SH2 domainlerini uzaklaştırmak için gereken ek üçüncül temas desenini oluşturamıyordu. Çapraz bağlama kütle spektrometrisi bu görüşü destekledi: aktive edici SH3 domainleri SH2 bölgeleriyle odaklanmış temaslar kurarken, aktive etmeyenler daha geniş bir pozisyon kümesini örnekleyerek daha gevşek, ürünsüz bir bağlanmaya uygun bir görünüm sergiledi.
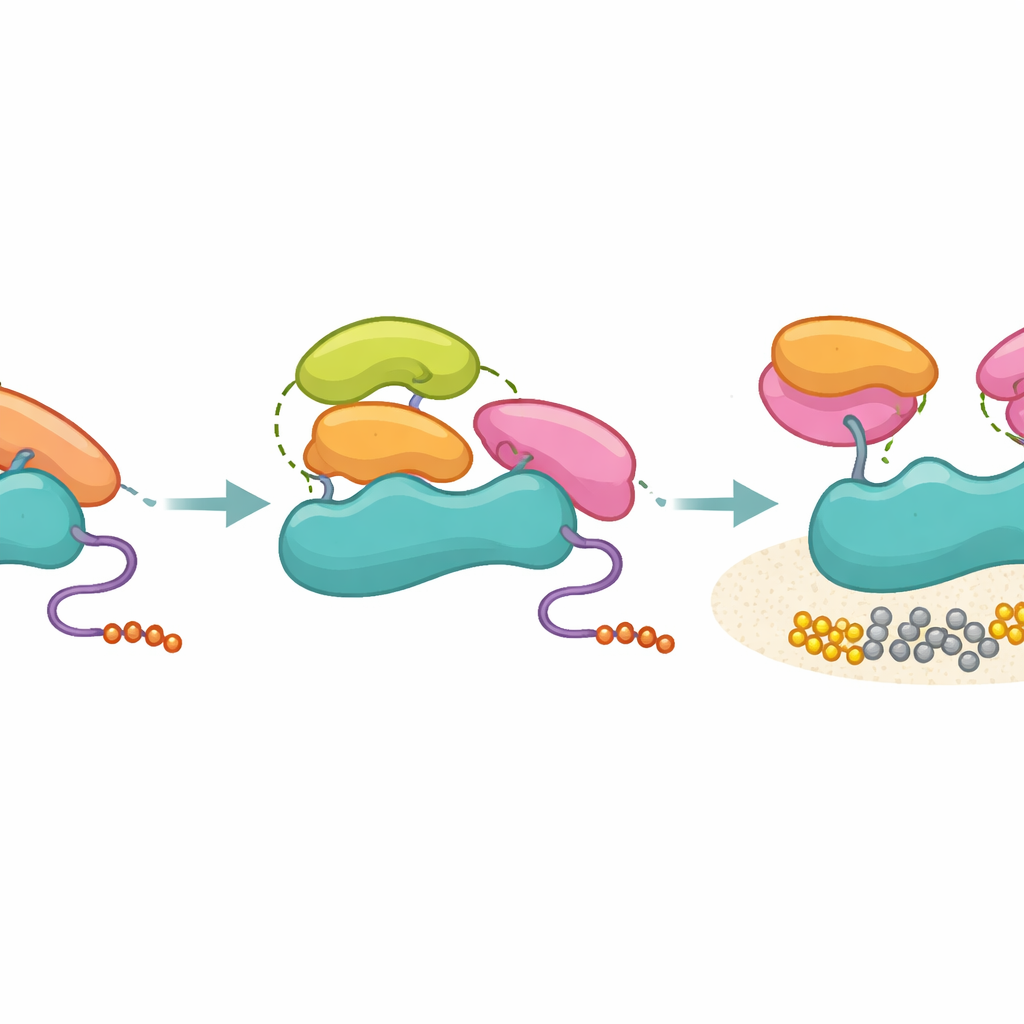
Hastalık ve İlaç Tasarımı Açısından Anlamı
Toplu halde ele alındığında çalışma, p85’in moleküler bir filtre gibi davrandığı bir modeli öne sürüyor: birçok SH3 domaininin bağlanmasını engellemiyor, ancak yalnızca doğru üç boyutlu temasları kurabilenlerin gerçekten PI3K’yı açmasına izin veriyor. Günlük bir benzetmeyle, birçok anahtar kilide uyuyor ama sadece birkaç tanesi iç pimleri yeterince hizalayarak kilidi çevirebiliyor. Bağlanma ile aktivasyonun ayrılması, hücrenin kalabalık ortamında sinyal doğruluğunu korumaya yardımcı olur ve aksi halde “promiskuitif” görünen SH3 modüllerinin nasıl özgül fonksiyonel sonuçlar verebildiğini açıklar. Bu üçüncül temas kurallarının anlaşılması, aktive edici SH3 yüzeylerini taklit eden veya engelleyen ilaçlara işaret edebilir ve PI3K sinyalini kanserler ve diğer PI3K kaynaklı hastalıklarda ayarlamak için yeni stratejiler sunabilir.
Atıf: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
Anahtar kelimeler: PI3 kinaz, protein sinyalleşmesi, SH3 domaini, kanser biyolojisi, moleküler etkileşimler