Clear Sky Science · es
Los dominios SH3 activan selectivamente la PI3 quinasa mediante contactos terciarios no convencionales
Cómo las células mantienen bajo control las señales de crecimiento
Nuestras células deciden constantemente si crecer, dividirse o permanecer en reposo. Un actor clave en este proceso es una enzima llamada PI3 quinasa (PI3K), que contribuye a regular el metabolismo y la supervivencia celular y que suele estar sobreactivada en varios tipos de cáncer. Este estudio aborda una pregunta sutil pero importante: cuando tantas piezas moleculares similares de “enchufe y toma” llenan la célula, ¿cómo distingue PI3K los encuentros inocuos de los pocos que realmente la cambian de “apagada” a “encendida”? La respuesta revela una capa oculta de selectividad que podría ayudar a diseñar terapias contra el cáncer más precisas.
Muchos enchufes parecidos, solo unos pocos interruptores reales
Las células están llenas de bloques de construcción reutilizables llamados dominios proteicos: módulos compactos que se unen a cortos fragmentos de otras proteínas. Una familia muy extendida, los dominios SH3, reconoce motivos ricos en prolina que son muy comunes en el proteoma humano. Dado que estos motivos son tan abundantes y los SH3 los reconocen de forma relativamente débil y algo indiscriminada, resulta desconcertante cómo las proteínas que contienen SH3 participan en vías de señalización altamente específicas sin provocar caos. Este enigma es especialmente relevante para PI3K, cuya desregulación impulsa el cáncer y otras enfermedades. Trabajos previos mostraron que la subunidad reguladora de PI3K, llamada p85, puede activarse por dominios SH3 de ciertas quinasas de la familia Src, pero no por otros, a pesar de que muchos de estos SH3 reconocen etiquetas ricas en prolina similares.
Los contactos auxiliares ocultos en el interruptor PI3K
Los autores se centraron en cómo los dominios SH3 de distintas proteínas interactúan con p85 y cómo esto afecta la actividad de PI3K. Mediante medidas precisas de unión y métodos estructurales, compararon la interacción del dominio SH3 de Fyn con un péptido corto rico en prolina procedente de p85 frente a casi la longitud completa de p85. Mientras que el péptido corto engagó a Fyn de la forma habitual, el fragmento largo de p85 se unió con mayor afinidad y con una firma energética distinta, lo que sugería que entraban en juego superficies adicionales. Desmontando p85 en piezas y reconstruyéndolo como quimeras, el equipo mostró que sus regiones C-terminales —los dos dominios SH2 y el segmento iSH2 en hélice que normalmente abraza a la subunidad catalítica p110— también participan en este contacto extendido, o “terciario”, con SH3.
Dos puntos diminutos que deciden entre unión y activación
Experimentos de resonancia magnética nuclear trazaron qué partes del dominio SH3 de Fyn se alteran más al unirse a p85 completo. Sobresalieron dos posiciones: una cerca de la ranura habitual de unión a prolina (denominada sitio PR-proximal) y otra en la cara opuesta del dominio (un sitio PR-distal). Mutar estas posiciones apenas cambió cuánto captaba SH3 el péptido simple rico en prolina, pero alteró de manera drástica cómo se relacionaba con p85 de longitud completa y, crucialmente, cuánto activaba a PI3K. En ensayos celulares de quinasa lipídica, algunos mutantes con afinidad modest a activaron PI3K más fuertemente que el tipo salvaje, mientras que otros con afinidad similar perdieron la mayor parte de su capacidad activadora. Esto demostró que la activación no sigue simplemente “qué tan fuerte es el agarre”, sino que depende de si el dominio SH3 puede formar los contactos terciarios correctos con ambas regiones SH2 inhibitorias de p85 y reposicionarlas respecto a p110.
Separar el mero contacto de un verdadero interruptor
Los investigadores probaron luego dominios SH3 de varias otras proteínas, incluidas Hck, Grb2, el propio p85 y Ubs3A, prestando atención especial al vecindario estructural del sitio PR-distal. Todos estos dominios SH3 podían unirse a p85 con una fuerza globalmente similar, pero solo aquellos con un parche hidrofóbico compatible en la posición distal clave —como Hck y el SH3 C-terminal de Grb2— pudieron activar PI3K en ensayos bioquímicos. Los dominios SH3 no activadores, incluido el propio SH3 de p85, aún se anclaban en la región rica en prolina de p85 pero no lograban generar el patrón adicional de contactos terciarios necesario para apartar las regiones SH2 inhibitorias. La espectrometría de masas tras entrecruzamiento apoyó esta visión: los SH3 activadores formaron contactos focalizados con las regiones SH2, mientras que los no activadores muestrearon un conjunto más amplio de posiciones, coherente con una unión más laxa y no productiva.
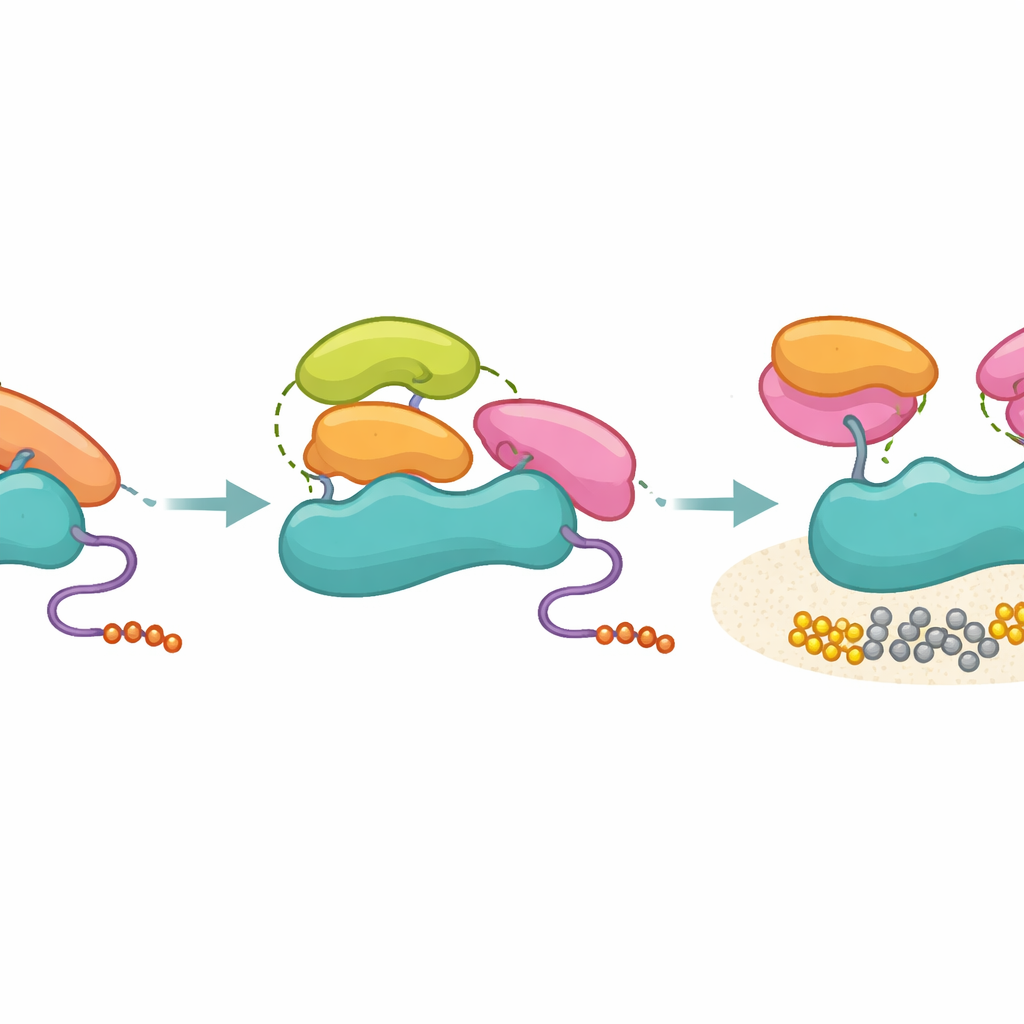
Qué implica esto para la enfermedad y el diseño de fármacos
En conjunto, el trabajo propone un modelo en el que p85 actúa como un filtro molecular: no impide que muchos dominios SH3 se unan, pero solo permite que aquellos que puedan establecer los contactos tridimensionales correctos desbloqueen realmente a PI3K. En términos cotidianos, muchas llaves encajan en la cerradura, pero solo unas pocas alinean los pasadores internos lo suficiente como para girar la llave. Esta separación entre unión y activación ayuda a mantener la precisión de la señalización en el ambiente abarrotado de la célula y explica cómo módulos SH3 aparentemente “promiscuos” pueden producir resultados funcionales específicos. Comprender estas reglas de contactos terciarios puede señalar estrategias para diseñar fármacos que imiten o bloqueen las superficies SH3 activadoras, ofreciendo nuevas vías para ajustar la señalización de PI3K en cánceres y otras enfermedades impulsadas por PI3K.
Cita: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
Palabras clave: PI3 quinasa, señalización proteica, dominio SH3, biología del cáncer, interacciones moleculares