Clear Sky Science · fr
Les domaines SH3 activent sélectivement la PI3 kinase via des contacts tertiaires non conventionnels
Comment les cellules contrôlent les signaux de croissance
Nos cellules décident en permanence de croître, de se diviser ou de rester au repos. Un acteur clé de ce processus est une enzyme appelée PI3 kinase (PI3K), qui régule le métabolisme et la survie cellulaire et qui est fréquemment hyperactive dans les cancers. Cette étude pose une question subtile mais importante : lorsque tant de pièces moléculaires semblables ― sortes de « fiches et prises » ― encombrent la cellule, comment PI3K distingue-t-elle les rencontres inoffensives de celles qui la font basculer de « éteinte » à « activée » ? La réponse révèle un niveau caché de sélectivité qui pourrait aider à concevoir des thérapies anticancéreuses plus précises.
Beaucoup de fiches similaires, seulement quelques véritables interrupteurs
Les cellules regorgent d’unités réutilisables appelées domaines protéiques — des modules compacts qui se lient à de courtes séquences d’autres protéines. Une famille répandue, les domaines SH3, reconnaît des motifs riches en proline qui sont très communs dans le protéome humain. Parce que ces motifs sont si abondants et que les SH3 s’y lient de façon faible et relativement indifférente, il est surprenant que les protéines contenant un SH3 participent à des voies de signalisation hautement spécifiques sans créer de chaos. Ce problème est particulièrement pressant pour PI3K, dont la désactivation mal contrôlée favorise le cancer et d’autres maladies. Des travaux antérieurs avaient montré que la sous-unité régulatrice de PI3K, appelée p85, peut être activée par les domaines SH3 de certaines kinases de la famille Src, mais pas d’autres, alors même que nombre de ces SH3 reconnaissent des étiquettes riches en proline similaires.
Les contacts auxiliaires cachés sur l’interrupteur PI3K
Les auteurs se sont concentrés sur la manière dont les domaines SH3 de différentes protéines interagissent avec p85 et comment cela affecte l’activité de PI3K. À l’aide de mesures de liaison précises et de méthodes structurales, ils ont comparé l’interaction du domaine SH3 de Fyn avec un court peptide riche en proline issu de p85 versus avec p85 presque en pleine longueur. Tandis que le peptide court engageait Fyn de façon standard, le fragment complet de p85 se liait plus fortement et avec un profil énergétique différent, suggérant l’intervention de surfaces supplémentaires. En découpant p85 en morceaux et en le reconstruisant sous forme chimérique, l’équipe a montré que ses régions C‑terminales — les deux domaines SH2 et le segment en hélice iSH2 qui maintiennent normalement le partenaire catalytique p110 — participent aussi à ce contact étendu, ou « tertiaire », avec le SH3.
Deux petits sites qui décident entre liaison et activation
Des expériences de résonance magnétique nucléaire ont cartographié quelles parties du domaine SH3 de Fyn sont le plus perturbées lors de la liaison au p85 complet. Deux positions ressortent : l’une près du sillon de liaison aux prolines habituel (appelée site PR‑proximal) et l’autre sur la face opposée du domaine (un site PR‑distal). Muter ces positions changeait à peine l’affinité du SH3 pour le simple peptide riche en proline, mais modifiait fortement sa manière d’engager le p85 en pleine longueur et, de manière cruciale, le niveau d’activation de PI3K qu’il déclenchait. Dans des essais de kinase lipidique réalisés en cellules, certains mutants d’affinité modeste activaient en fait PI3K plus fortement que le type sauvage, tandis que d’autres, avec une affinité comparable, perdaient la majeure partie de leur pouvoir activateur. Cela montre que l’activation ne suit pas simplement « la force d’adhérence », mais dépend de la capacité du domaine SH3 à établir les bons contacts tertiaires avec les deux régions SH2 inhibitrices de p85 et à les repositionner par rapport à p110.
Séparer le simple contact du véritable passage en marche
Les chercheurs ont ensuite testé des domaines SH3 provenant de plusieurs autres protéines, y compris Hck, Grb2, p85 lui‑même et Ubs3A, en portant une attention particulière au voisinage structural du site PR‑distal. Tous ces domaines SH3 pouvaient se lier à p85 avec une force globalement similaire, pourtant seuls ceux présentant un patch hydrophobe compatible à la position distale clé — comme Hck et le SH3 C‑terminal de Grb2 — parvenaient à activer PI3K dans des essais biochimiques. Les SH3 non activateurs, y compris le propre SH3 de p85, se fixaient toujours sur la région riche en proline de p85 mais échouaient à générer le profil supplémentaire de contacts tertiaires nécessaire pour éloigner les domaines SH2 inhibiteurs. La spectrométrie de masse après réticulation soutient cette vision : les SH3 activateurs formaient des contacts focalisés avec les régions SH2, tandis que les non‑activateurs exploraient un ensemble plus large de positions, cohérent avec une attache plus lâche et non productive.
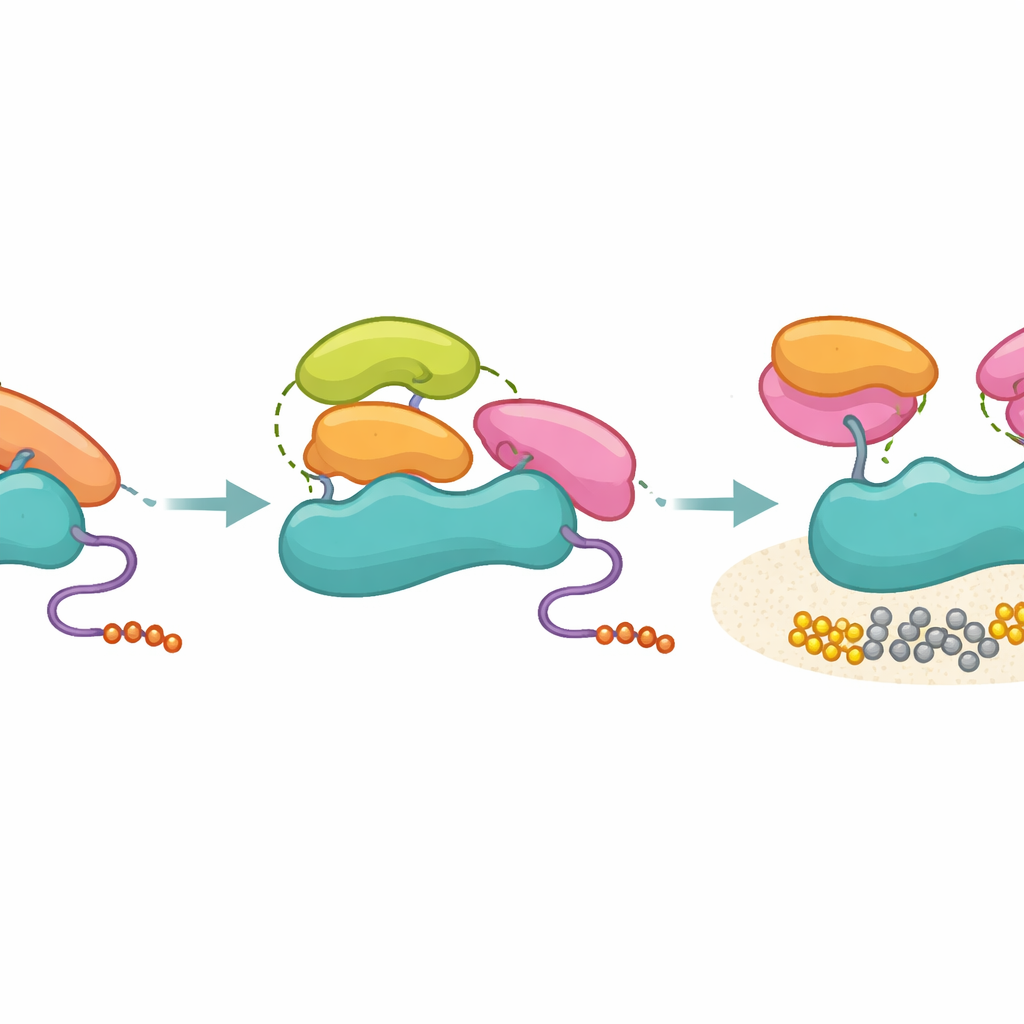
Implications pour la maladie et la conception de médicaments
Dans l’ensemble, ce travail propose un modèle dans lequel p85 agit comme un filtre moléculaire : il n’empêche pas de nombreux SH3 de se lier, mais n’autorise que ceux capables d’établir les bons contacts tridimensionnels à véritablement déverrouiller PI3K. En termes quotidiens, beaucoup de clés entrent dans la serrure, mais seules quelques‑unes alignent suffisamment bien les goupilles internes pour tourner la serrure. Cette séparation entre liaison et activation contribue à maintenir la précision de la signalisation dans l’environnement encombré de la cellule et explique comment des modules SH3 par ailleurs « promiscuous » peuvent aboutir à des résultats fonctionnels spécifiques. Comprendre ces règles de contacts tertiaires pourrait orienter la conception de médicaments qui imitent ou bloquent les surfaces SH3 activatrices, offrant de nouvelles stratégies pour moduler la signalisation PI3K dans les cancers et d’autres maladies dépendantes de la PI3K.
Citation: Aljedani, S.S., Sandholu, A., Aldehaiman, A. et al. SH3 domains selectively activate the PI3 kinase through non-conventional tertiary contacts. Commun Biol 9, 515 (2026). https://doi.org/10.1038/s42003-026-09540-y
Mots-clés: PI3 kinase, signalisation protéique, domaine SH3, biologie du cancer, interactions moléculaires