Clear Sky Science · zh
NDUFA4L2 通过抑制 PANoptosis 调控 HNSCC 的进展和化疗敏感性
这项研究的重要性
化疗对许多头颈部癌症患者来说是生命线,但肿瘤常常学会躲避这些药物。本研究揭示了单一线粒体蛋白 NDUFA4L2 如何帮助头颈鳞状细胞癌(HNSCC)逃避广泛使用的顺铂,并表明关闭该蛋白既能更有效地杀死癌细胞,又能唤醒免疫系统。该工作指向通过针对癌细胞的糖代谢和死亡方式来恢复药物敏感性的潜在新途径。
一种顽固的癌症与失效的药物
头颈鳞状细胞癌(HNSCC)是全球常见癌症之一,常用顺铂治疗。然而许多肿瘤会产生耐药性,使患者选择受限。作者聚焦于 NDUFA4L2——一种位于细胞能量工厂(线粒体)的蛋白,在低氧条件下被激活并改变细胞的能量利用方式。通过分析公开的单细胞数据集并检测患者肿瘤样本,他们发现 NDUFA4L2 在与较差生存相关的一类肿瘤细胞中高度活跃。来自对化疗不再敏感患者的肿瘤样本中该蛋白含量尤其高,提示其在耐药中起核心作用。
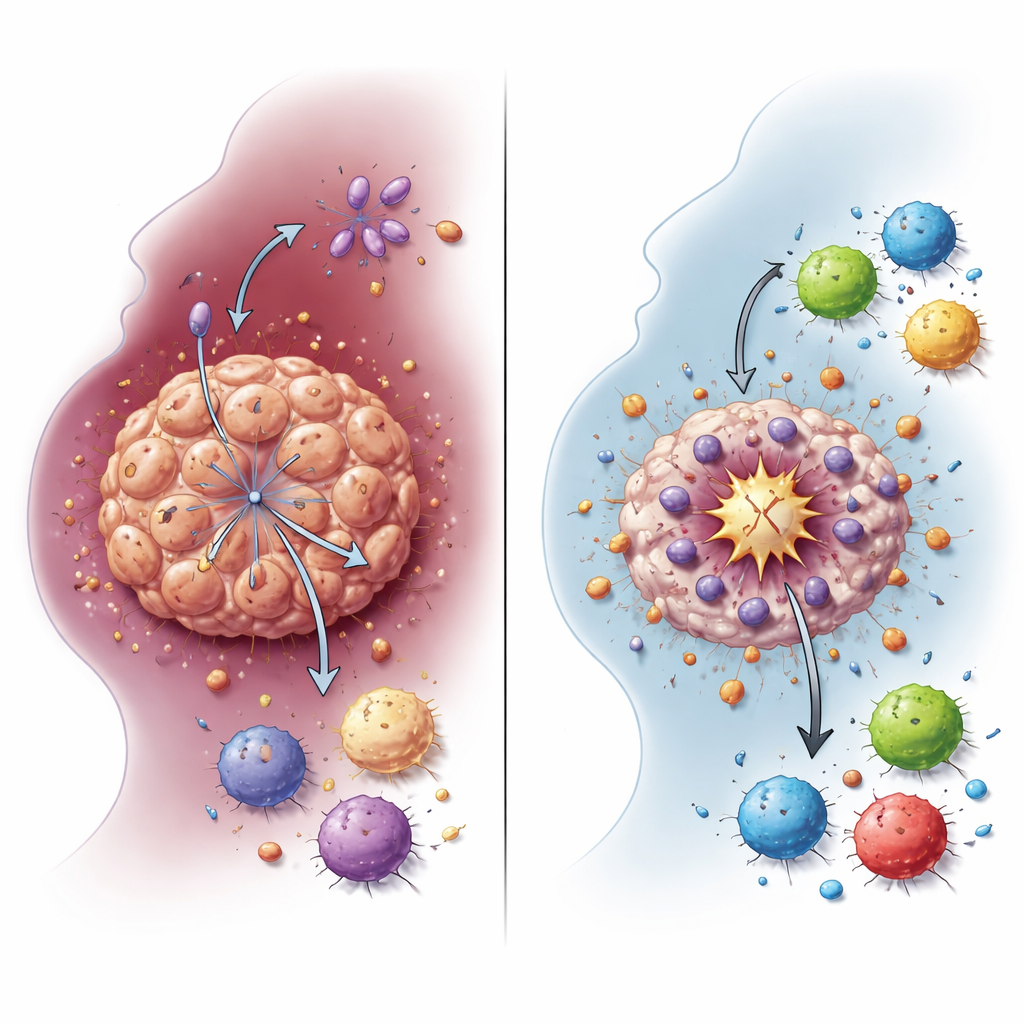
燃料转换如何保护肿瘤细胞
癌细胞常依赖一种快速的糖代谢途径——糖酵解,即使在有氧情况下也产生大量乳酸。研究团队表明 NDUFA4L2 支持 HNSCC 细胞的这种糖酵解状态。将 NDUFA4L2 从细胞系和来源于患者样本的三维类肿瘤中去除后,乳酸水平显著下降。基因表达谱从糖酵解与乳酸代谢方向发生转变,将 NDUFA4L2 与癌细胞改变的能量利用直接关联起来。这种燃料转换并非肿瘤生长的副产物:事实证明它是帮助肿瘤细胞抵御顺铂并逃避一种特别强效细胞死亡形式的屏障。
将癌细胞逼入三重死亡程序
细胞可以通过多种可调控途径死亡,包括凋亡、坏死性凋亡和焦亡。最近研究者描述了 PANoptosis,一种整合的“多合一”死亡程序,结合了三者的关键组成部分。本研究中,敲除 NDUFA4L2 使 HNSCC 细胞对顺铂敏感性大大增强。显微镜下,处理后的细胞出现典型的膨胀与破裂,生化检测也证实了凋亡、坏死性凋亡和焦亡标志物的同步激活。重要的是,阻断任一路径仅能部分挽救细胞,表明是完整的 PANoptosis 程序被触发。在舌部肿瘤小鼠模型中,去除 NDUFA4L2 并联合顺铂可缩小肿瘤、延长生存并增强这一复合死亡反应的标志物。
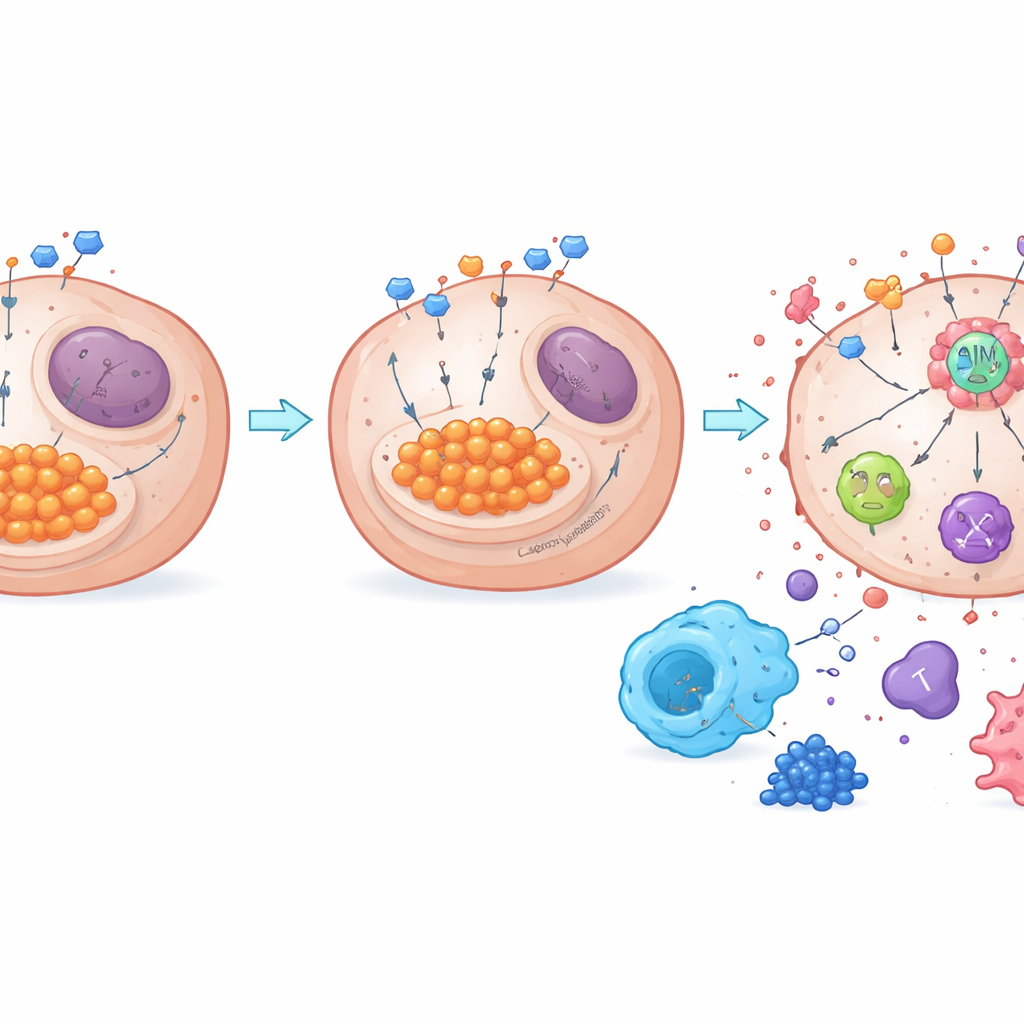
从糖代谢废物到免疫觉醒
该研究还揭示了代谢如何与一个关键死亡调控传感器 AIM2 相连。当糖酵解活跃时,过量乳酸可通过乳酸化对蛋白质进行化学修饰。作者发现 NDUFA4L2 维持较高的乳酸水平并促进 AIM2 的乳酸化,似乎使该传感器处于抑制状态。去除 NDUFA4L2 降低了乳酸、减少了 AIM2 的乳酸化,并增强了由 AIM2 组装的诱导 PANoptosis 的死亡复合体。当实验上降低 AIM2 时,NDUFA4L2 缺失加顺铂引发的强烈杀伤效应大多消失,证实了 AIM2 的核心作用。在小鼠肿瘤和人类样本中,高表达的 NDUFA4L2 与更强的免疫抑制性巨噬细胞浸润及更少的抗癌 T 细胞相关,而阻断糖酵解或 NDUFA4L2 则将微环境向更活跃的免疫状态转变。
对未来治疗的意义
对非专业读者而言,这项研究表明某些头颈癌通过重编程糖代谢并抑制内在的自毁开关来躲避化疗。通过下调 NDUFA4L2 或阻断糖酵解,研究者能够降低乳酸、重新激活 AIM2 死亡传感器、触发侵袭性的三模式细胞死亡程序,并在细胞、类器官和小鼠中增强顺铂的疗效。与此同时,肿瘤微环境也变得更有利于免疫攻击。这些发现提示,未来针对 NDUFA4L2 或其控制的代谢与乳酸化途径的药物,可能与标准化疗联合使用,以克服耐药并改善头颈癌患者的预后。
引用: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
关键词: 头颈癌, 化疗耐药, 癌细胞代谢, 程序化细胞死亡, 肿瘤微环境