Clear Sky Science · de
NDUFA4L2 reguliert das Fortschreiten und die Chemotherapieempfindlichkeit von HNSCC durch Hemmung der PANoptose
Warum diese Forschung wichtig ist
Die Chemotherapie ist für viele Menschen mit Kopf‑ und‑Hals‑Tumoren eine Lebenslinie, doch Tumoren lernen oft, die Medikamente auszutricksen. Diese Studie zeigt, wie ein einzelnes mitochondriales Protein, NDUFA4L2, dem Plattenepithelkarzinom des Kopfes und Halses hilft, dem häufig eingesetzten Wirkstoff Cisplatin zu entgehen, und demonstriert, wie das Abschalten dieses Proteins sowohl Krebszellen effektiver abtöten als auch das Immunsystem aktivieren kann. Die Arbeit weist auf neue Ansätze hin, die Arzneimittelempfindlichkeit wiederherzustellen, indem man die Art und Weise angreift, wie Krebszellen Zucker verbrennen und wie sie absterben.
Ein hartnäckiger Krebs und ein versagendes Medikament
Das Plattenepithelkarzinom des Kopfes und Halses (HNSCC) zählt weltweit zu den häufigsten Krebsarten und wird oft mit Cisplatin behandelt. Viele Tumoren entwickeln jedoch Resistenzen, sodass den Patientinnen und Patienten nur begrenzte Optionen bleiben. Die Autorinnen und Autoren richteten den Fokus auf NDUFA4L2, ein Protein in den Energiezentralen der Zelle (Mitochondrien), das unter niedrigen Sauerstoffbedingungen hochreguliert wird und die Art verändert, wie Zellen Brennstoff nutzen. Anhand öffentlicher Einzelzell‑Datensätze und der Untersuchung von Patientenproben fanden sie heraus, dass NDUFA4L2 in einer klar abgegrenzten Untergruppe von Tumorzellen stark aktiv ist, die mit schlechterem Überleben verbunden ist. Tumoren von Patientinnen und Patienten, deren Krebs nicht mehr auf die Chemotherapie ansprach, hatten besonders hohe Mengen dieses Proteins, was darauf hindeutet, dass es eine zentrale Rolle bei der Resistenz spielt.
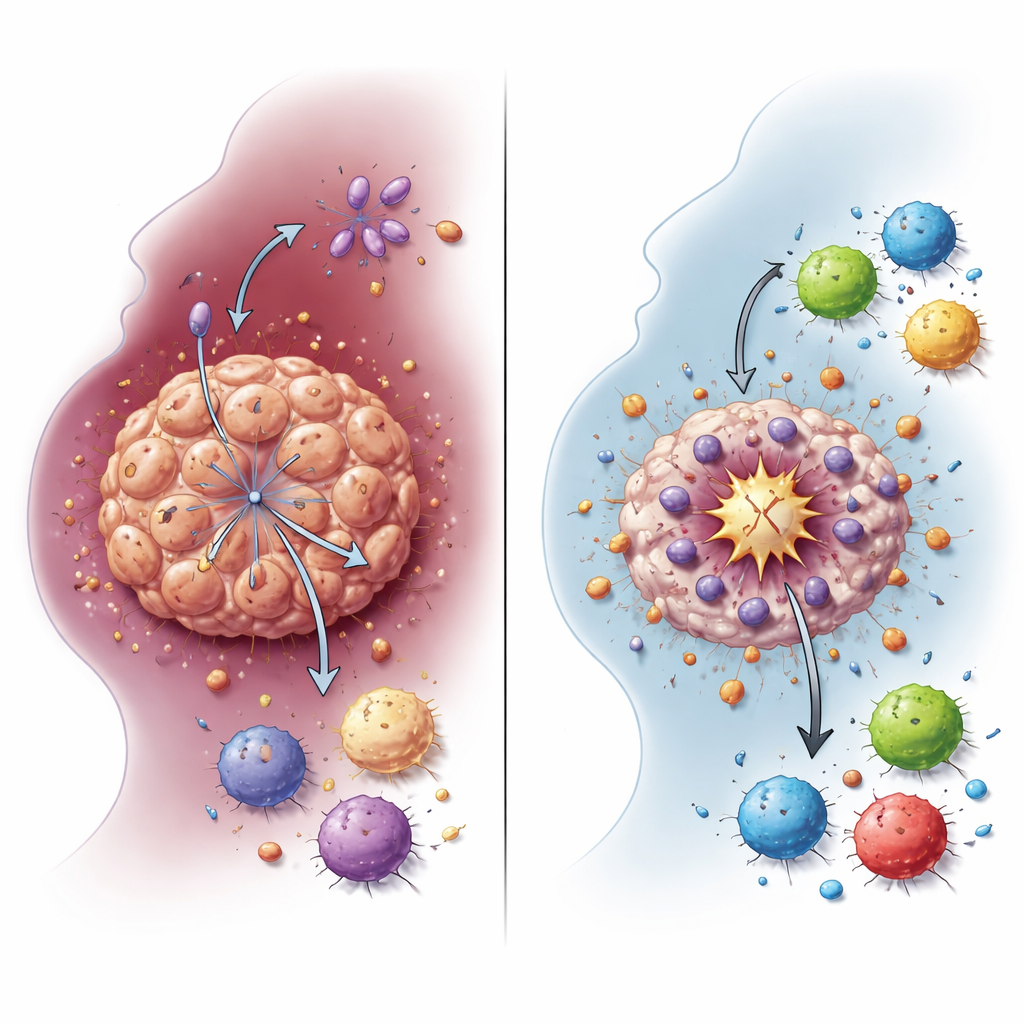
Wie ein Brennstoffwechsel‑Switch Tumorzellen schützt
Krebszellen verlassen sich häufig auf eine verkürzte Form des Zuckerabbaus, die Glykolyse, die große Mengen Laktat produziert, selbst wenn Sauerstoff vorhanden ist. Das Team zeigte, dass NDUFA4L2 diesen glykolytischen Zustand in HNSCC‑Zellen unterstützt. Wurde NDUFA4L2 aus Zelllinien und aus dreidimensionalen Mini‑Tumoren, die aus Patientenproben gezüchtet wurden, entfernt, fielen die Laktatspiegel stark ab. Genexpressionsmuster verschoben sich weg von Glykolyse und Laktatstoffwechsel, wodurch NDUFA4L2 direkt mit der veränderten Energieverwendung des Krebses verknüpft wurde. Dieser Brennstoffwechsel‑Switch ist nicht nur ein Nebenprodukt von Tumorwachstum: Er erweist sich als Schutzschild, der Tumorzellen hilft, Cisplatin zu überleben und eine besonders wirksame Form des Zelltods zu vermeiden.
Die Krebszellen in ein dreifaches Todesprogramm zwingen
Zellen können auf verschiedenen regulierten Wegen sterben, darunter Apoptose, Nekroptose und Pyroptose. Jüngst wurde PANoptose beschrieben, ein integriertes „All‑in‑One“‑Todesprogramm, das zentrale Elemente aller drei Wege kombiniert. In dieser Studie machte das Ausschalten von NDUFA4L2 HNSCC‑Zellen sehr viel anfälliger für Cisplatin. Unter dem Mikroskop zeigten behandelte Zellen charakteristische Aufblähungen und Aufreißen, und biochemische Tests bestätigten die gleichzeitige Aktivierung von Markern für Apoptose, Nekroptose und Pyroptose. Wichtig ist, dass das Blockieren eines einzelnen Weges die Zellen nur teilweise rettete, was darauf hinweist, dass das vollständige PANoptose‑Programm aktiviert war. In Mausmodellen mit Zungen‑Tumoren führten NDUFA4L2‑Entfernung und Cisplatin zu Tumorschrumpfung, verlängerter Überlebenszeit und verstärkten Markern dieses kombinierten Todesantworts.
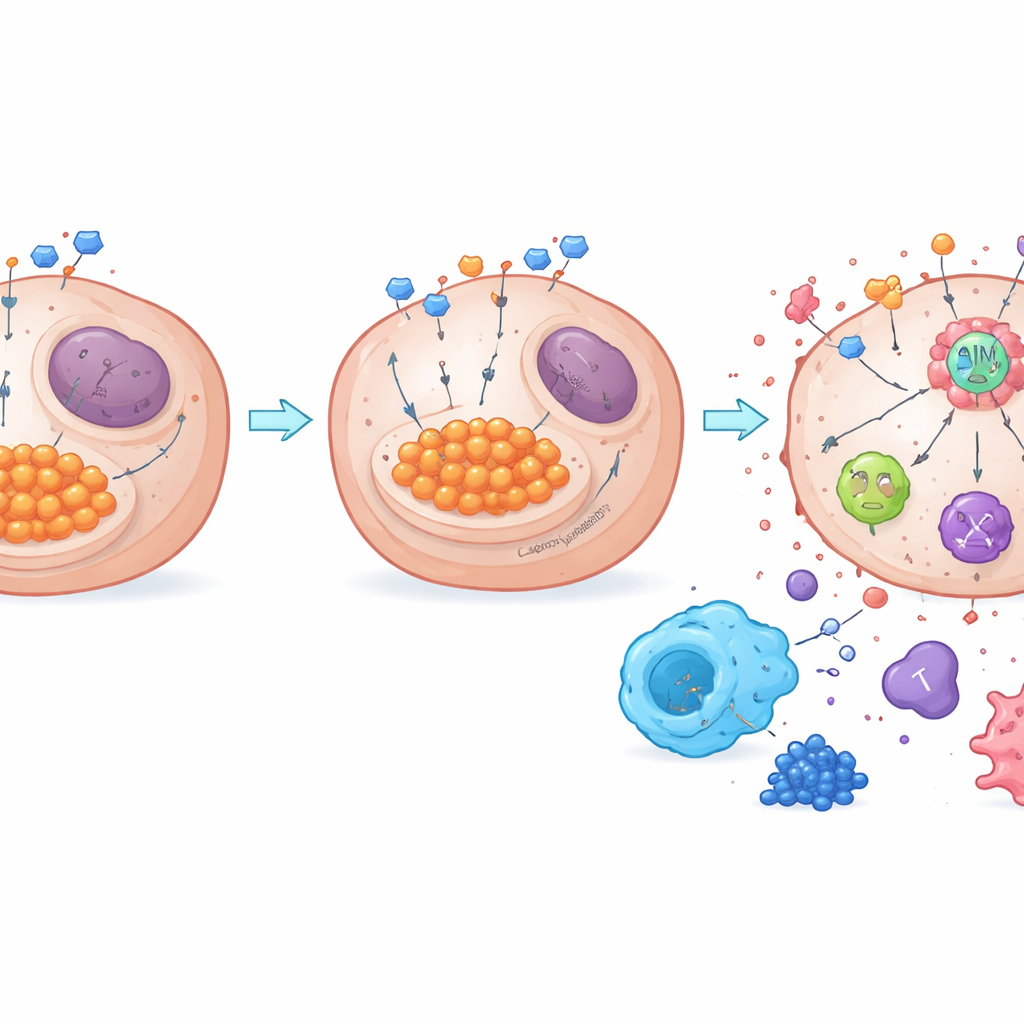
Vom Zuckerabfall zur Immun‑Erweckung
Die Arbeit zeigt außerdem, wie der Stoffwechsel mit einem wichtigen toderegulierenden Sensor namens AIM2 verknüpft ist. Wenn die Glykolyse hoch ist, kann überschüssiges Laktat Proteine chemisch verändern, ein Prozess, der als Laktylierung bezeichnet wird. Die Autorinnen und Autoren entdeckten, dass NDUFA4L2 die Laktatspiegel hoch hält und die Laktylierung von AIM2 fördert, was diesen Sensor offenbar in einem gedämpften Zustand hält. Die Entfernung von NDUFA4L2 senkte Laktat, verringerte die Laktylierung von AIM2 und stärkte die Assemblierung eines AIM2‑basierenden Todeskomplexes, der PANoptose auslöst. Wurde AIM2 experimentell reduziert, ließ die starke Tötungswirkung des NDUFA4L2‑Verlusts plus Cisplatin weitgehend nach, was die zentrale Rolle von AIM2 bestätigte. Sowohl in Maus‑Tumoren als auch in menschlichen Proben waren hohe NDUFA4L2‑Werte und Laktylierung mit mehr immunsuppressiven Makrophagen und weniger krebsbekämpfenden T‑Zellen verbunden, während das Blockieren der Glykolyse oder von NDUFA4L2 das Gleichgewicht in Richtung einer aktiveren Immunumgebung verschob.
Was das für zukünftige Behandlungen bedeutet
Für eine/n Laien zeigt diese Studie, dass bestimmte Kopf‑ und‑Hals‑Krebsarten der Chemotherapie entgehen, indem sie die Nutzung von Zucker umprogrammieren und einen eingebauten Selbstzerstörungs‑Schalter beruhigen. Durch das Herunterregulieren von NDUFA4L2 oder das Blockieren der Glykolyse konnten die Forschenden Laktat senken, den AIM2‑Todsensor reaktivieren, ein aggressives Dreifach‑Zelltodsprogramm auslösen und Cisplatin in Zellen, Organoiden und Mäusen wirksamer machen. Gleichzeitig wurde die Tumorumgebung für einen Immunangriff empfänglicher. Diese Befunde deuten darauf hin, dass Wirkstoffe, die auf NDUFA4L2 oder auf die von ihm kontrollierten Stoffwechsel‑ und Laktylierungswege abzielen, eines Tages mit Standardchemotherapien kombiniert werden könnten, um Resistenzen zu überwinden und die Ergebnisse für Patientinnen und Patienten mit Kopf‑und‑Hals‑Krebs zu verbessern.
Zitation: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
Schlüsselwörter: Kopf‑und‑Hals‑Krebs, Chemotherapie‑Resistenz, Krebsstoffwechsel, programmierter Zelltod, Tumormikroumgebung