Clear Sky Science · it
NDUFA4L2 regola la progressione e la sensibilità alla chemioterapia dell’HNSCC inibendo la PANoptosi
Perché questa ricerca è importante
La chemioterapia è una ancora di salvezza per molte persone con tumori della testa e del collo, ma spesso le neoplasie imparano a eludere i farmaci. Questo studio svela come una singola proteina mitocondriale, NDUFA4L2, aiuti il carcinoma squamocellulare della testa e del collo a sfuggire al comunemente usato cisplatino, e mostra come disattivare questa proteina possa sia uccidere più efficacemente le cellule tumorali sia risvegliare il sistema immunitario. Il lavoro indica nuove vie per ripristinare la sensibilità ai farmaci agendo sul modo in cui le cellule cancerose metabolizzano gli zuccheri e muoiono.
Un cancro ostinato e un farmaco che fallisce
Il carcinoma squamocellulare della testa e del collo (HNSCC) è tra i tumori più comuni al mondo ed è spesso trattato con cisplatino. Molti tumori però diventano resistenti, lasciando ai pazienti poche opzioni. Gli autori si sono concentrati su NDUFA4L2, una proteina nelle “fabbriche energetiche” della cellula (mitocondri) che viene attivata in condizioni di basso ossigeno e modifica l’uso del carburante cellulare. Analizzando set di dati a singola cellula pubblici e campioni tumorali di pazienti, hanno scoperto che NDUFA4L2 è molto attiva in un sottogruppo distintivo di cellule tumorali associato a scarsa sopravvivenza. I tumori di pazienti che avevano smesso di rispondere alla chemioterapia presentavano quantità particolarmente alte di questa proteina, suggerendo un ruolo centrale nella resistenza.
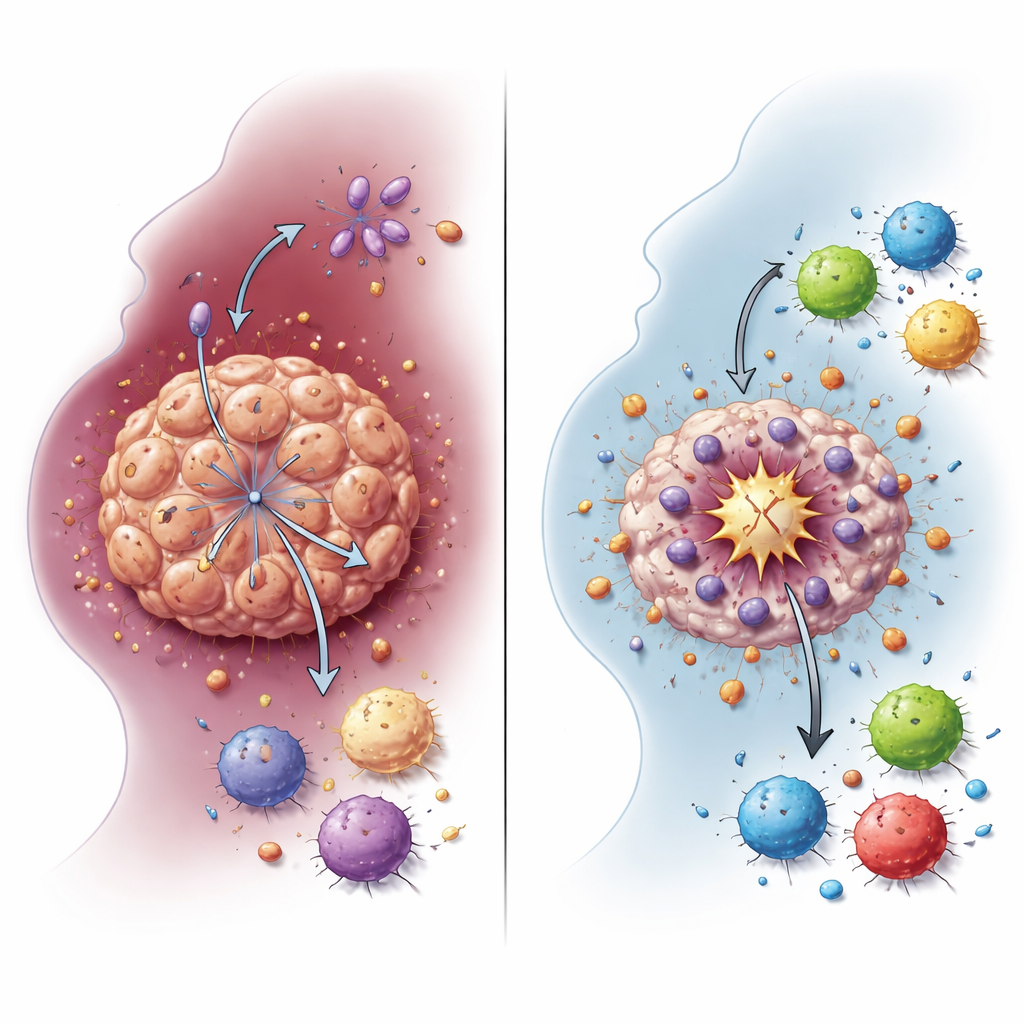
Come un cambio di carburante protegge le cellule tumorali
Le cellule tumorali spesso fanno affidamento su una forma semplificata di utilizzo degli zuccheri chiamata glicolisi, che produce grandi quantità di lattato anche in presenza di ossigeno. Il gruppo ha dimostrato che NDUFA4L2 sostiene questo stato glicolitico nelle cellule HNSCC. Quando NDUFA4L2 è stato rimosso da linee cellulari e da mini-tumori tridimensionali cresciuti da campioni dei pazienti, i livelli di lattato sono crollati. I modelli di espressione genica si sono spostati lontano dalla glicolisi e dal metabolismo del lattato, collegando direttamente NDUFA4L2 all’alterato uso energetico del cancro. Questo switch metabolico non è solo un effetto collaterale della crescita tumorale: si rivela una protezione che aiuta le cellule tumorali a sopravvivere al cisplatino ed evitare una forma particolarmente potente di morte cellulare.
Forzare le cellule cancerose in un programma di triplice morte
Le cellule possono morire attraverso diverse vie regolate, tra cui apoptosi, necroptosi e piroptosi. Recentemente è stata descritta la PANoptosi, un programma integrato “tutto-in-uno” che combina elementi chiave di tutte e tre. In questo studio, l’eliminazione di NDUFA4L2 ha reso le cellule HNSCC molto più vulnerabili al cisplatino. Al microscopio, le cellule trattate mostravano il tipico rigonfiamento e la rottura, e test biochimici hanno confermato l’attivazione simultanea di marcatori per apoptosi, necroptosi e piroptosi. Importante, il blocco di una singola via proteggeva parzialmente le cellule, indicando che era stato attivato il programma completo di PANoptosi. In modelli murini di tumori della lingua, la rimozione di NDUFA4L2 insieme alla somministrazione di cisplatino ha ridotto i tumori, allungato la sopravvivenza e aumentato i marker di questa risposta di morte combinata.
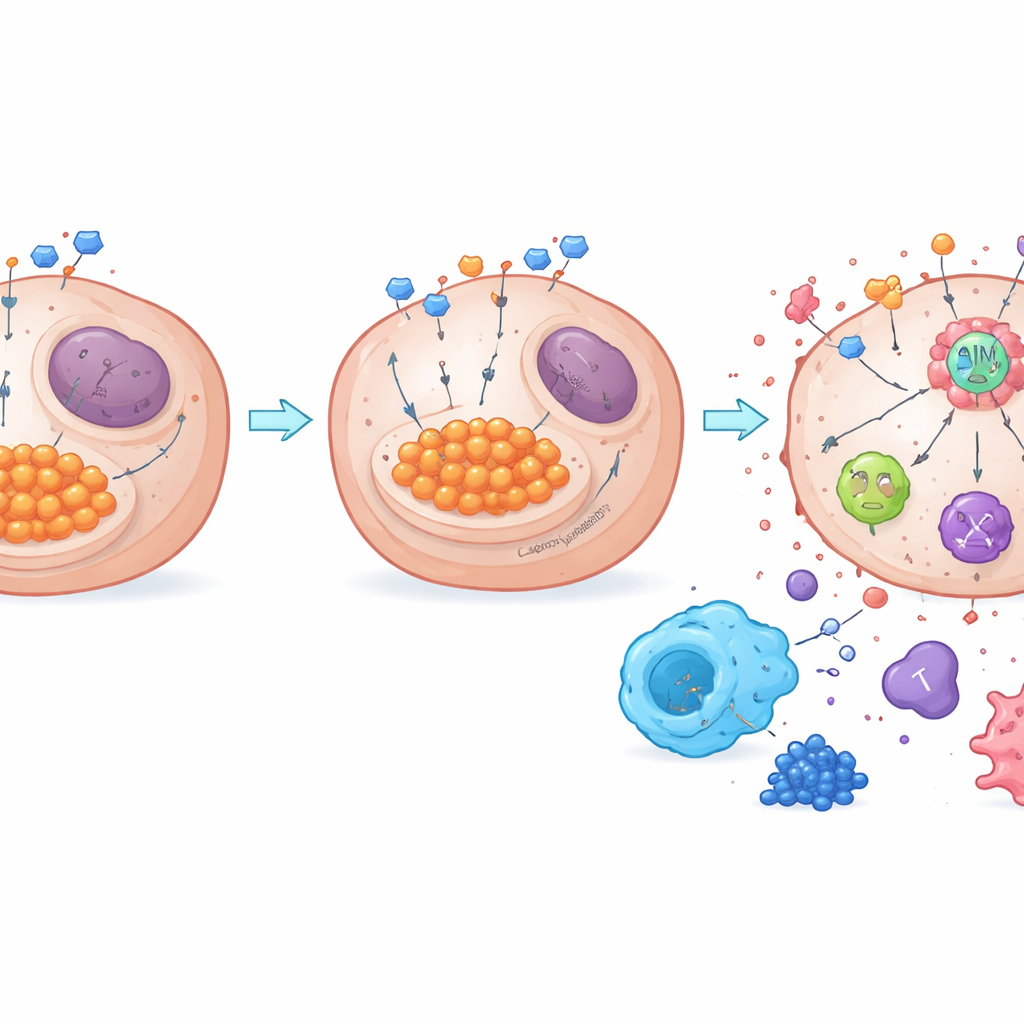
Dal rifiuto degli zuccheri al risveglio immunitario
Il lavoro rivela anche come il metabolismo si colleghi a un sensore chiave della morte cellulare chiamato AIM2. Quando la glicolisi è elevata, l’eccesso di lattato può modificare chimicamente le proteine in un processo noto come lattilazione. Gli autori hanno scoperto che NDUFA4L2 mantiene alti i livelli di lattato e promuove la lattilazione di AIM2, che appare in uno stato più soppresso. La rimozione di NDUFA4L2 ha abbassato il lattato, ridotto la lattilazione di AIM2 e rafforzato l’assemblaggio di un complesso di morte basato su AIM2 che innesca la PANoptosi. Quando AIM2 è stato sperimentalmente ridotto, il potente effetto letale dovuto alla perdita di NDUFA4L2 più cisplatino è in gran parte scomparso, confermando il ruolo centrale di AIM2. Nei tumori murini e nei campioni umani, alti livelli di NDUFA4L2 e lattilazione correvano insieme a un maggior numero di macrofagi immunosoppressivi e a meno cellule T antitumorali, mentre il blocco della glicolisi o di NDUFA4L2 spostava l’equilibrio verso un microambiente più attivo dal punto di vista immunitario.
Cosa significa per i trattamenti futuri
Per un lettore non specialista, questo studio mostra che alcuni tumori della testa e del collo sopravvivono alla chemioterapia riorganizzando il loro uso degli zuccheri e attenuando un interruttore di autodistruzione incorporato. Riducendo NDUFA4L2 o bloccando la glicolisi, i ricercatori sono riusciti ad abbassare il lattato, riattivare il sensore di morte AIM2, innescare un aggressivo programma di morte cellulare a tripla modalità e migliorare l’efficacia del cisplatino in cellule, organoidi e topi. Allo stesso tempo, l’ambiente tumorale è diventato più favorevole all’attacco immunitario. Questi risultati suggeriscono che farmaci mirati a NDUFA4L2, o alle vie metaboliche e di lattilazione che controlla, potrebbero un giorno essere combinati con la chemioterapia standard per superare la resistenza e migliorare gli esiti nei pazienti con tumori della testa e del collo.
Citazione: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
Parole chiave: cancro testa e collo, resistenza alla chemioterapia, metabolismo del cancro, morte cellulare programmata, microambiente tumorale