Clear Sky Science · ar
تنظّم NDUFA4L2 تقدم وحساسية العلاج الكيميائي في سرطان الخلايا الحرشفية بالرأس والعنق عن طريق تثبيط PANoptosis
لماذا يهم هذا البحث
العلاج الكيميائي يشكل شريان حياة للعديد من المصابين بسرطانات الرأس والعنق، لكن الأورام كثيراً ما تتعلّم التحايل على الأدوية. يكشف هذا البحث كيف يساعد بروتين واحد في الميتوكوندريا، NDUFA4L2، سرطان الخلايا الحرشفية بالرأس والعنق على التحايل على الدواء الشائع سيسبلاتين، ويبيّن كيف أن إيقاف هذا البروتين يمكن أن يقتل خلايا السرطان بفعالية أكبر ويوقظ الجهاز المناعي. تشير النتائج إلى طرق جديدة لاستعادة حساسية الأدوية عبر استهداف كيفية استهلاك الخلايا للسكر ومسارات موتها.
سرطان عنيد ودواء يفشل
يعد سرطان الخلايا الحرشفية بالرأس والعنق من أكثر السرطانات انتشاراً عالمياً وغالباً ما يُعالج بالسيسبلاتين. ومع ذلك، تصبح العديد من الأورام مقاومة، ما يترك للمرضى خيارات محدودة. ركّز الباحثون على NDUFA4L2، بروتين في مصانع طاقة الخلايا (الميتوكوندريا) يُنشَّط في ظروف نقص الأكسجين ويغيّر طريقة استخدام الخلايا للوقود. من خلال تحليل مجموعات بيانات خلوية أحادية عامة وفحص عينات أورام المرضى، وجدوا أن NDUFA4L2 نشط بشكل كبير في مجموعة فرعية مميزة من خلايا الورم المرتبطة بتراجع البقاء. كانت الأورام من المرضى التي توقفت عن الاستجابة للعلاج الكيميائي تحتوي على كميات عالية بشكل خاص من هذا البروتين، ما يوحي بأنه يلعب دوراً محورياً في المقاومة.
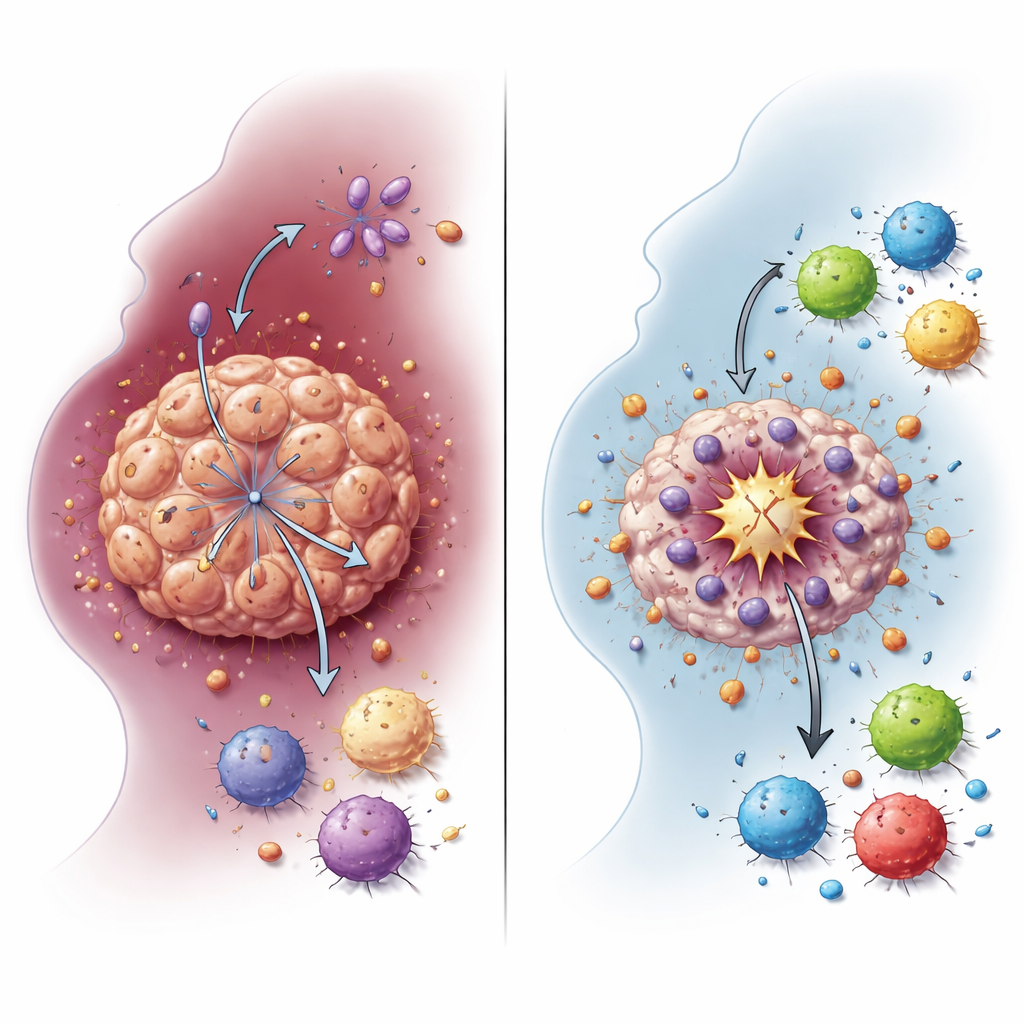
كيف يحمي تبديل الوقود خلايا الورم
تعتمد خلايا السرطان غالباً على شكل مختصر من أكسدة السكر يُدعى تحلل الجلوكوز اللاهوائي (glycolysis)، الذي ينتج كميات كبيرة من اللاكتات حتى في وجود الأكسجين. أظهر الفريق أن NDUFA4L2 يدعم هذه الحالة الجليكولية في خلايا HNSCC. عند إزالة NDUFA4L2 من خطوط الخلايا ومن الأورام المصغرة ثلاثية الأبعاد المستزرعة من عينات المرضى، انخفضت مستويات اللاكتات بشكل حاد. تحوّلت أنماط نشاط الجينات بعيداً عن الجليكوليز وأيض اللاكتات، ما يربط NDUFA4L2 مباشرة بتغيير استهلاك الطاقة في السرطان. هذا التبديل في الوقود ليس مجرد ناتج عرضي لنمو السرطان؛ بل يتضح أنه درع يساعد خلايا الورم على النجاة من السيسبلاتين وتجنب شكل قوي من الموت الخلوي.
إجبار خلايا السرطان على برنامج موت ثلاثي
يمكن للخلايا أن تموت عبر عدة طرق منظمة، منها الاستماتة (apoptosis) والنيكروبتوسيس (necroptosis) والبيروبتوسيس (pyroptosis). وصف الباحثون مؤخراً PANoptosis، برنامج موت متكامل يجمع عناصر رئيسية من الثلاثة معاً. في هذه الدراسة، جعلت عملية حذف NDUFA4L2 خلايا HNSCC أكثر عرضة بكثير للسيسبلاتين. تحت المجهر، أظهرت الخلايا المعالجة انتفاخاً وتمزقاً مميزين، وأكدت الاختبارات الكيميائية الحيوية تنشيط مؤشرات الاستماتة والنيكروبتوسيس والبيروبتوسيس في وقت واحد. والأهم أن حجب أي مسار واحد أنقذ الخلايا جزئياً فقط، ما يدل على انخراط برنامج PANoptosis الكامل. في نماذج الفئران لأورام اللسان، أدى حذف NDUFA4L2 ومعالجة السيسبلاتين إلى تقلص الأورام، وإطالة البقاء، وزيادة مؤشرات هذا الاستجابة المجمعة للموت.
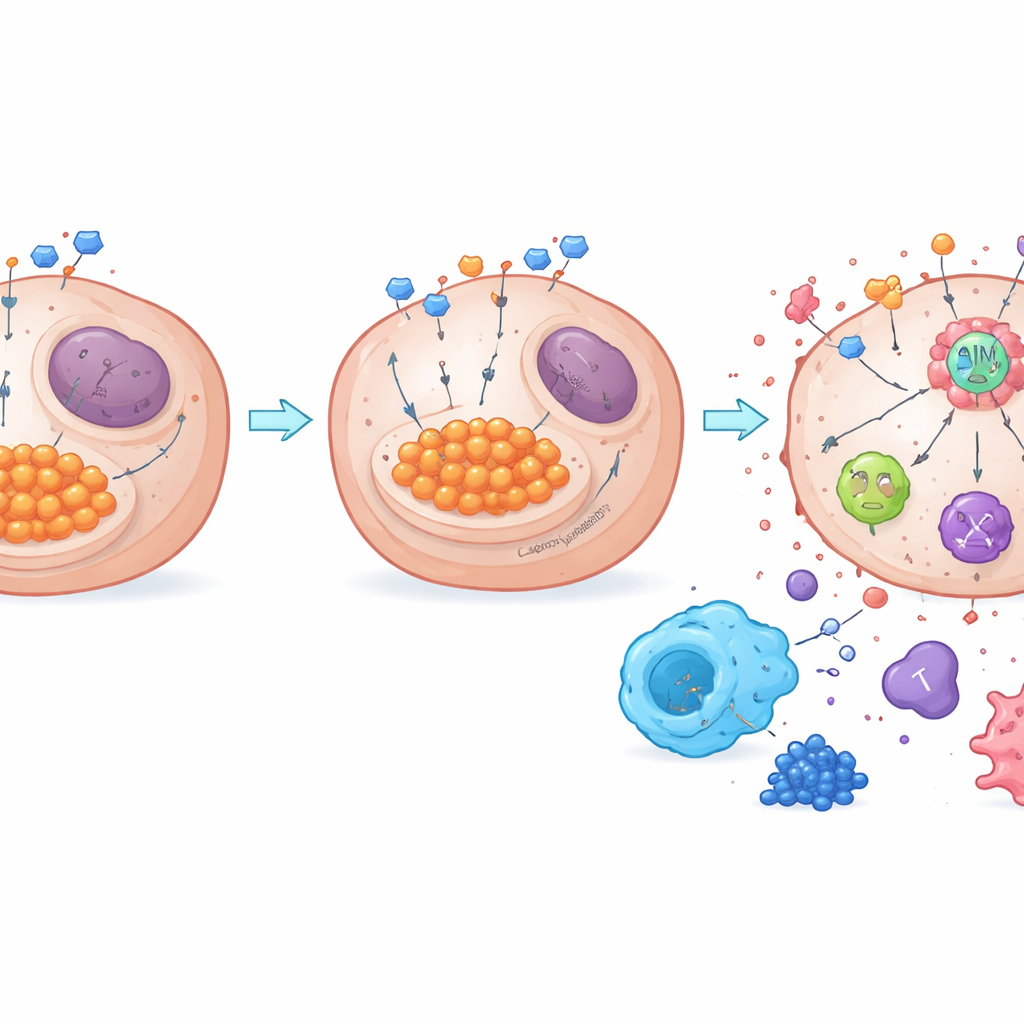
من نفايات السكر إلى إيقاظ المناعة
يكشف العمل أيضاً كيف يرتبط الأيض بمستشعر رئيسي لتنظيم الموت يُدعَى AIM2. عندما يكون التحلل الجليكولي مرتفعاً، يمكن للاكتات الزائدة أن تعدّل البروتينات كيميائياً في عملية تُعرف باللاكتلة (lactylation). اكتشف المؤلفون أن NDUFA4L2 يحافظ على مستويات لاكتات عالية ويعزز لاكتلة AIM2، مما يبدو أنه يبقي هذا المستشعر في حالة كبت. أدى حذف NDUFA4L2 إلى خفض اللاكتات، وتقليل لاكتلة AIM2، وتقوية تجمّع مركب موت قائم على AIM2 الذي يطلق PANoptosis. عندما خُفِّض AIM2 تجريبياً، تلاشت بشكل كبير فعالية القتل القوية الناتجة عن خسارة NDUFA4L2 مع السيسبلاتين، مؤكدة الدور المركزي لـ AIM2. في أورام الفئران والعيّنات البشرية، ارتبطت مستويات عالية من NDUFA4L2 واللاكتلة بوجود المزيد من الخلايا البلعمية المثبطة للمناعة وعدد أقل من خلايا T قاتلة للسرطان، بينما أدى حجب الجليكوليز أو NDUFA4L2 إلى تحويل التوازن نحو بيئة مناعية أكثر نشاطاً.
ماذا يعني هذا للعلاجات المستقبلية
للمشاهد العادي، يُظهر هذا البحث أن بعض سرطانات الرأس والعنق تنجو من العلاج الكيميائي عن طريق إعادة توصيل استهلاك السكر وكبت مفتاح ذاتي للتدمير. بخفض نشاط NDUFA4L2 أو حجب الجليكوليز، تمكن الباحثون من خفض اللاكتات، وإعادة تفعيل مستشعر الموت AIM2، وإطلاق برنامج موت خلوي عدواني متعدد الأوضاع، وجعل السيسبلاتين أكثر فعالية في الخلايا والعضيات الورمية والفئران. في الوقت نفسه، أصبحت محيطات الورم أكثر ملاءمة للهجوم المناعي. تشير هذه النتائج إلى أن أدوية تستهدف NDUFA4L2، أو المسارات الأيضية ولاكتلة التي يتحكم بها، قد تُدمج يوماً ما مع العلاج الكيميائي القياسي لتجاوز المقاومة وتحسين النتائج لمرضى سرطان الرأس والعنق.
الاستشهاد: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
الكلمات المفتاحية: سرطان الرأس والعنق, مقاومة العلاج الكيميائي, أيض السرطان, الموت الخلوي المبرمج, البيئة الميكروية للورم