Clear Sky Science · pl
NDUFA4L2 reguluje progresję i wrażliwość na chemioterapię HNSCC przez hamowanie PANoptozy
Dlaczego to badanie ma znaczenie
Chemioterapia jest ratunkiem dla wielu pacjentów z nowotworami głowy i szyi, jednak guzy często potrafią przechytrzyć leki. To badanie ujawnia, jak jeden białkowy składnik mitochondriów, NDUFA4L2, pomaga płaskonabłonkowemu rakowi głowy i szyi unikać powszechnie stosowanego cisplatyny, oraz pokazuje, że wyłączenie tego białka może skuteczniej zabić komórki nowotworowe i pobudzić układ odpornościowy. Praca wskazuje nowe strategie przywracania wrażliwości na leki poprzez ukierunkowanie na to, jak komórki nowotworowe spalają cukry i umierają.
Uparty nowotwór i zawodzący lek
Płaskonabłonkowy rak głowy i szyi (HNSCC) należy do najczęstszych nowotworów na świecie i często jest leczony cisplatyną. Wiele guzów jednak nabywa oporność, pozostawiając pacjentów z ograniczonymi opcjami. Autorzy skupili się na NDUFA4L2, białku w „elektrowniach” komórkowych (mitochondriach), które jest aktywowane w warunkach niskiego tlenu i zmienia sposób wykorzystania paliwa przez komórki. Analizując publiczne dane z pojedynczych komórek oraz próbki guzów pacjentów, odkryli, że NDUFA4L2 jest silnie aktywne w wyraźnej podgrupie komórek nowotworowych powiązanej z gorszym przeżyciem. Guzy od pacjentów, których nowotwory przestały reagować na chemioterapię, zawierały szczególnie dużo tego białka, co sugeruje jego kluczową rolę w oporności.
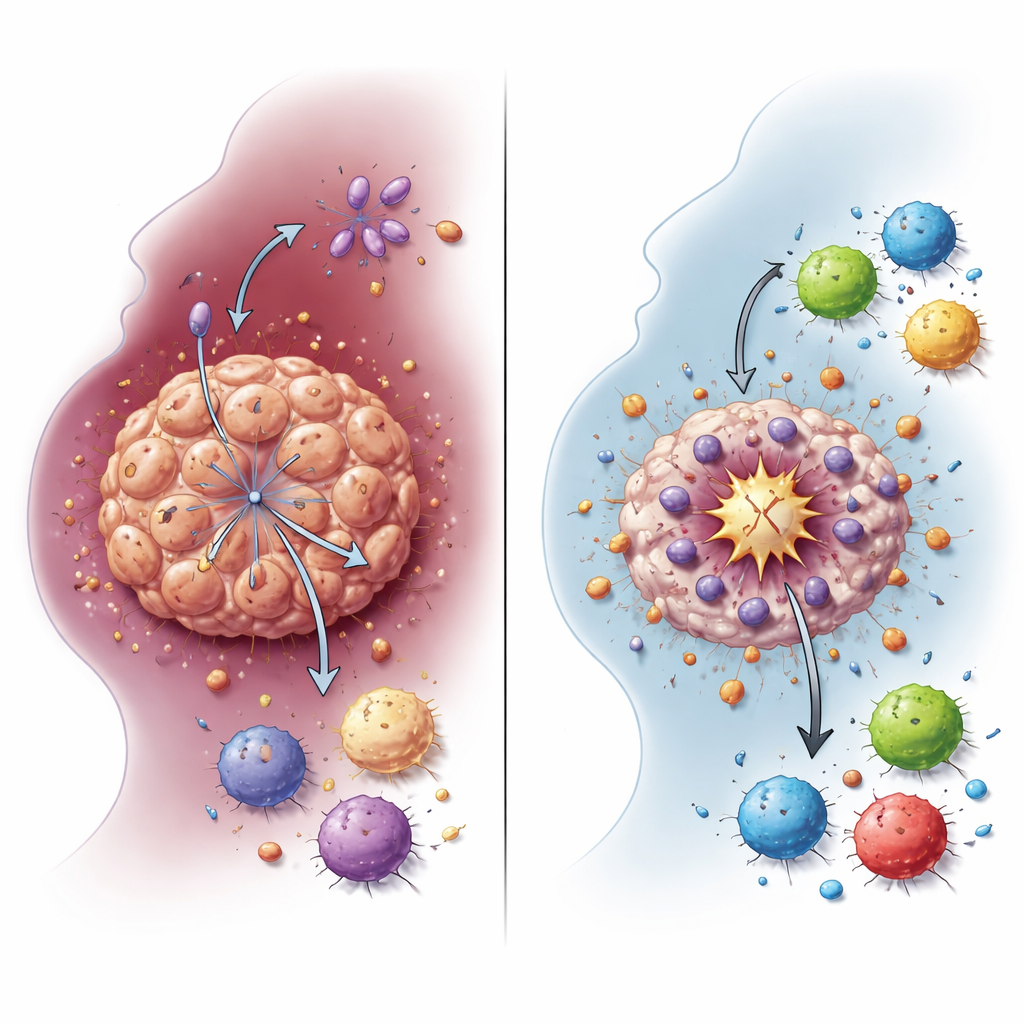
Jak przełączenie paliwa osłania komórki guza
Komórki nowotworowe często polegają na uproszczonej formie utleniania cukru zwanej glikolizą, która wytwarza duże ilości mleczanu nawet przy dostępności tlenu. Zespół wykazał, że NDUFA4L2 wspiera ten glikolityczny stan w komórkach HNSCC. Po usunięciu NDUFA4L2 z linii komórkowych i z trójwymiarowych mini‑guzów hodowanych z próbek pacjentów, poziomy mleczanu spadły gwałtownie. Wzory aktywności genów odchylały się od glikolizy i metabolizmu mleczanu, łącząc NDUFA4L2 bezpośrednio ze zmienionym wykorzystaniem energii przez nowotwór. To przełączenie paliwowe nie jest jedynie skutkiem wzrostu nowotworu: okazuje się być tarczą, która pomaga komórkom guza przetrwać cisplatynę i unikać wyjątkowo silnej formy śmierci komórkowej.
Wymuszenie potrójnego programu śmierci komórek
Komórki mogą umierać przez kilka regulowanych dróg, w tym apoptozę, nekroptozę i pyroptozę. Ostatnio opisano PANoptozę, zintegrowany „wszystko w jednym” program śmierci łączący kluczowe elementy wszystkich trzech. W tym badaniu wyłączenie NDUFA4L2 uczyniło komórki HNSCC znacznie bardziej wrażliwymi na cisplatynę. Pod mikroskopem leczone komórki wykazywały charakterystyczne pęcznienie i pękanie, a testy biochemiczne potwierdziły jednoczesną aktywację markerów apoptotycznych, nekroptotycznych i pyroptotycznych. Co ważne, zablokowanie dowolnej pojedynczej drogi ratowało komórki tylko częściowo, co wskazuje, że uruchomiony został pełny program PANoptozy. W modelach mysich guzów języka usunięcie NDUFA4L2 i zastosowanie cisplatyny zmniejszyło rozmiary guzów, wydłużyło przeżycie i zwiększyło markery tej skumulowanej odpowiedzi śmierci.
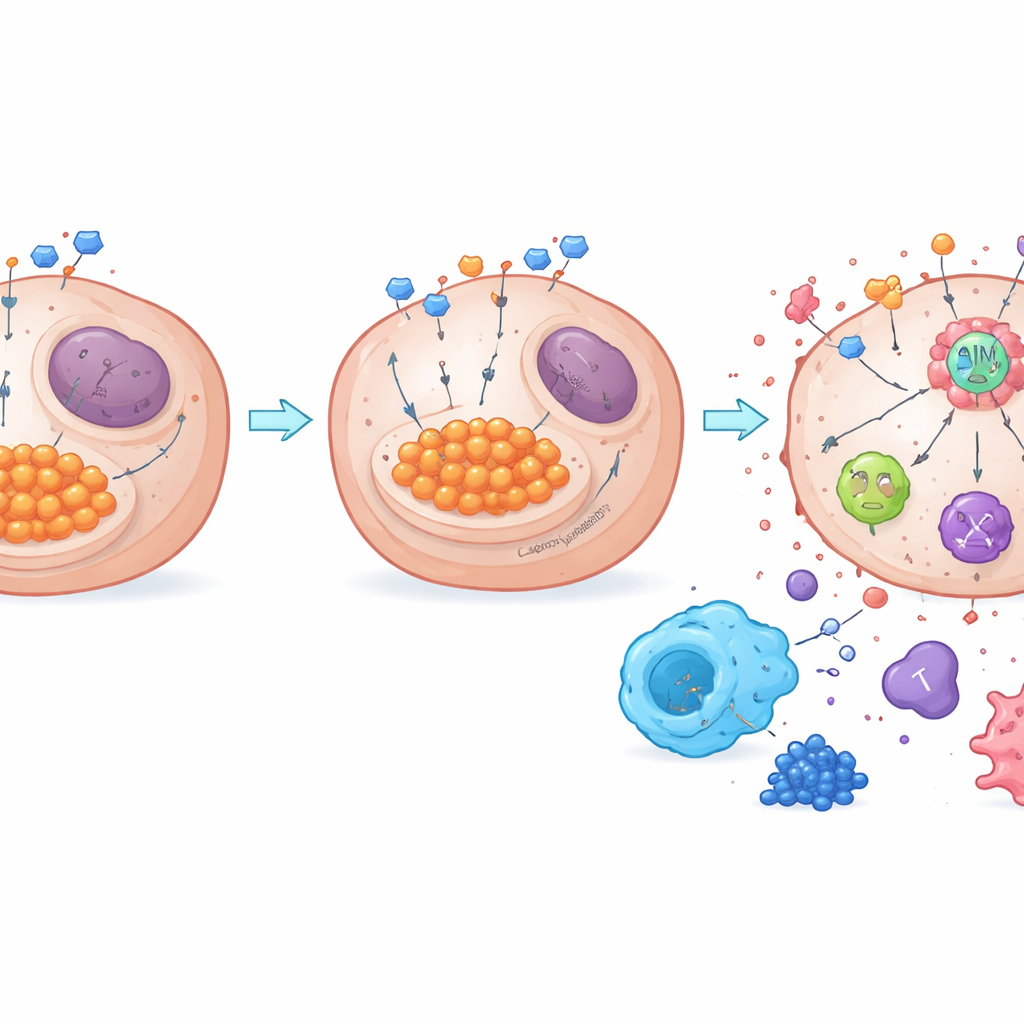
Od odpadu cukrowego do przebudzenia układu odpornościowego
Praca ujawnia także, jak metabolizm łączy się z kluczowym sensorem regulującym śmierć zwanym AIM2. Gdy glikoliza jest intensywna, nadmiar mleczanu może chemicznie modyfikować białka w procesie zwanym laktylacją. Autorzy odkryli, że NDUFA4L2 utrzymuje wysokie poziomy mleczanu i promuje laktylację AIM2, co wydaje się tłumić aktywność tego sensora. Usunięcie NDUFA4L2 obniżało poziom mleczanu, zmniejszało laktylację AIM2 i wzmacniało składanie kompleksu śmierci opartego na AIM2, który uruchamia PANoptozę. Gdy AIM2 było eksperymentalnie zredukowane, silny efekt zabijający wywołany utratą NDUFA4L2 wraz z cisplatyną w dużej mierze zanikał, potwierdzając centralną rolę AIM2. Zarówno w guzach mysich, jak i w próbkach ludzkich, wysoki poziom NDUFA4L2 i laktylacji korelował z większą liczbą immunosupresyjnych makrofagów i mniejszą liczbą komórek T walczących z rakiem, podczas gdy blokada glikolizy lub NDUFA4L2 przesuwała równowagę w kierunku bardziej aktywnego środowiska immunologicznego.
Co to oznacza dla przyszłych terapii
Dla laika to badanie pokazuje, że niektóre raki głowy i szyi przetrwają chemioterapię, przeprogramowując wykorzystanie cukru i wyciszając wbudowany wyłącznik samodestrukcji. Poprzez stłumienie NDUFA4L2 lub blokadę glikolizy badacze byli w stanie obniżyć poziom mleczanu, reaktywować sensor śmierci AIM2, uruchomić agresywny, potrójny program śmierci komórek i zwiększyć skuteczność cisplatyny w komórkach, organoidach i modelach mysich. Równocześnie otoczenie guza stało się bardziej sprzyjające atakowi immunologicznemu. Wyniki te sugerują, że leki celujące w NDUFA4L2, lub w kontrolowane przez nie ścieżki metaboliczne i laktylacji, mogłyby w przyszłości być łączone ze standardową chemioterapią, aby przezwyciężyć oporność i poprawić wyniki u pacjentów z rakiem głowy i szyi.
Cytowanie: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
Słowa kluczowe: rak głowy i szyi, oporność na chemioterapię, metabolizm nowotworu, programowana śmierć komórki, mikrośrodowisko guza