Clear Sky Science · es
NDUFA4L2 regula la progresión y la sensibilidad a la quimioterapia del SCC de cabeza y cuello al inhibir la PANoptosis
Por qué importa esta investigación
La quimioterapia es una tabla de salvación para muchas personas con cánceres de cabeza y cuello, pero los tumores a menudo aprenden a eludir los fármacos. Este estudio revela cómo una única proteína mitocondrial, NDUFA4L2, ayuda al carcinoma escamoso de cabeza y cuello a escapar del ampliamente utilizado cisplatino, y muestra cómo apagar esta proteína puede tanto matar con más eficacia a las células cancerosas como activar el sistema inmune. El trabajo señala nuevas maneras de restaurar la sensibilidad a los fármacos al dirigirse a cómo las células cancerosas queman azúcar y mueren.
Un cáncer persistente y un fármaco que falla
El carcinoma escamoso de cabeza y cuello (HNSCC) está entre los cánceres más comunes en el mundo y a menudo se trata con cisplatino. Sin embargo, muchos tumores desarrollan resistencia, dejando a los pacientes con opciones limitadas. Los autores se centraron en NDUFA4L2, una proteína en las fábricas de energía de la célula (mitocondrias) que se activa en condiciones de baja oxigenación y altera cómo las células usan el combustible. Al analizar conjuntos de datos públicos de células individuales y examinar muestras tumorales de pacientes, encontraron que NDUFA4L2 está muy activa en un subgrupo distinto de células tumorales vinculado a una peor supervivencia. Los tumores de pacientes cuyos cánceres dejaron de responder a la quimioterapia presentaban cantidades especialmente altas de esta proteína, lo que sugiere que desempeña un papel central en la resistencia.
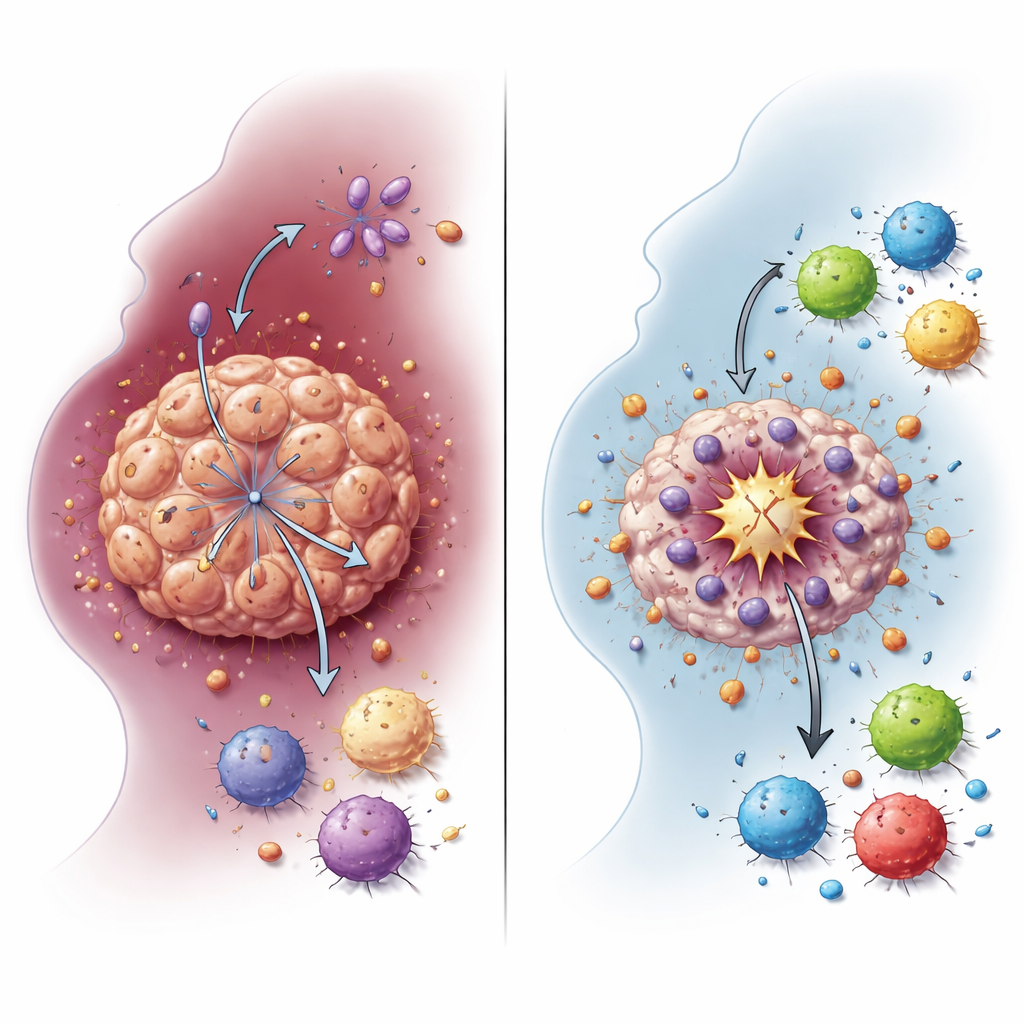
Cómo un cambio en el combustible protege a las células tumorales
Las células cancerosas a menudo dependen de una vía rápida de combustión de la glucosa llamada glucólisis, que produce grandes cantidades de lactato incluso cuando hay oxígeno disponible. El equipo mostró que NDUFA4L2 sostiene este estado glucolítico en las células de HNSCC. Cuando NDUFA4L2 se eliminó de líneas celulares y de mini-tumores tridimensionales derivados de muestras de pacientes, los niveles de lactato cayeron drásticamente. Los patrones de actividad génica se desplazaron alejándose de la glucólisis y del metabolismo del lactato, vinculando directamente a NDUFA4L2 con el uso de energía alterado del cáncer. Este cambio en el combustible no es solo un subproducto del crecimiento tumoral: resulta ser un escudo que ayuda a las células tumorales a sobrevivir al cisplatino y a evitar una forma de muerte celular especialmente potente.
Forzar a las células cancerosas a un programa de muerte triple
Las células pueden morir por varias vías reguladas, incluida la apoptosis, la necroptosis y la piroptosis. Recientemente, los investigadores han descrito la PANoptosis, un programa de muerte integrado “todo en uno” que combina elementos clave de las tres. En este estudio, la eliminación de NDUFA4L2 hizo que las células de HNSCC fueran mucho más vulnerables al cisplatino. Bajo el microscopio, las células tratadas mostraron la típica hinchazón y ruptura, y pruebas bioquímicas confirmaron la activación simultánea de marcadores de apoptosis, necroptosis y piroptosis. Importante: bloquear cualquiera de las vías solo rescató parcialmente a las células, lo que indica que se activó el programa completo de PANoptosis. En modelos murinos de tumores de la lengua, eliminar NDUFA4L2 y administrar cisplatino redujo los tumores, prolongó la supervivencia y aumentó los marcadores de esta respuesta combinada de muerte.
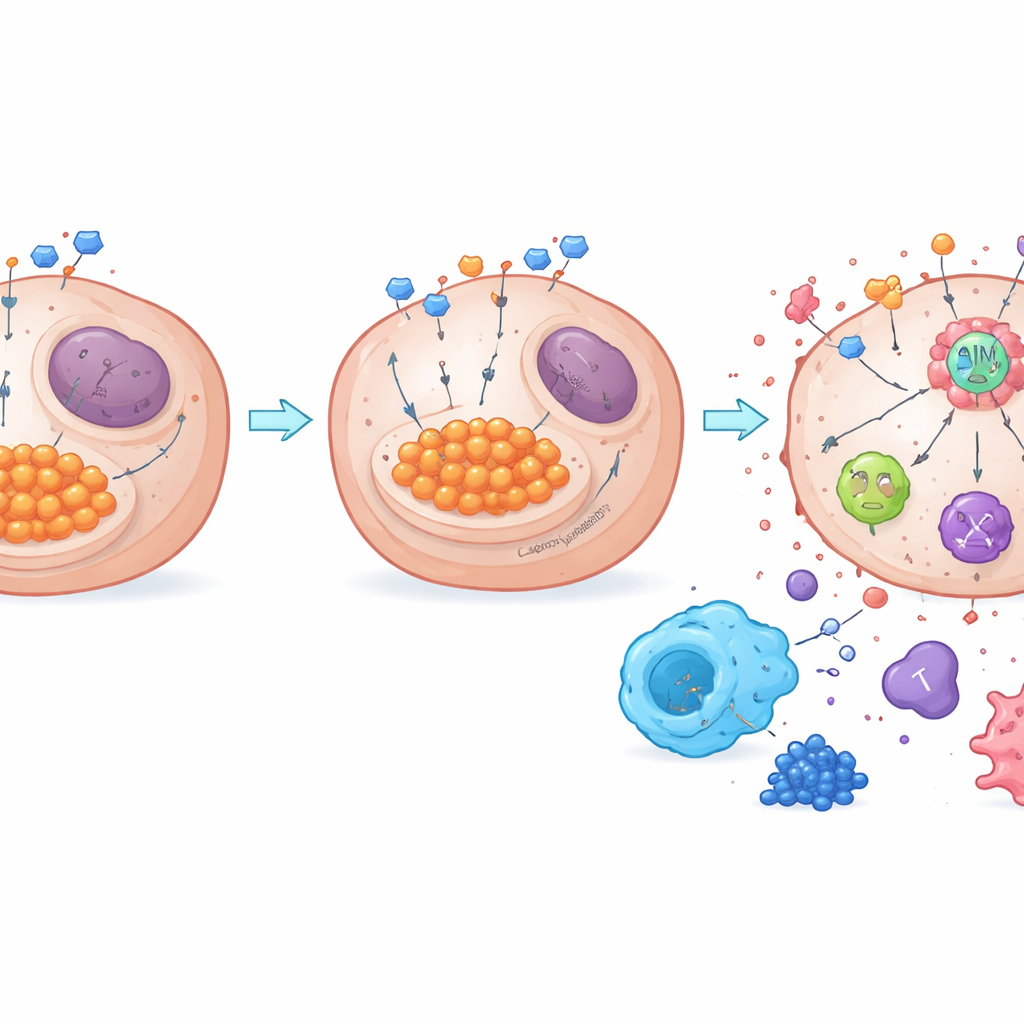
Del desecho de azúcar al despertar inmune
El trabajo también revela cómo el metabolismo se conecta con un sensor clave que regula la muerte llamado AIM2. Cuando la glucólisis es alta, el exceso de lactato puede modificar químicamente proteínas en un proceso conocido como lactilación. Los autores descubrieron que NDUFA4L2 mantiene altos los niveles de lactato y promueve la lactilación de AIM2, lo que parece mantener a este sensor en un estado atenuado. Eliminar NDUFA4L2 redujo el lactato, disminuyó la lactilación de AIM2 y fortaleció el ensamblaje de un complejo de muerte basado en AIM2 que desencadena la PANoptosis. Cuando AIM2 se redujo experimentalmente, el potente efecto letal de la pérdida de NDUFA4L2 más cisplatino se atenuó en gran medida, confirmando el papel central de AIM2. Tanto en tumores de ratón como en muestras humanas, altos niveles de NDUFA4L2 y de lactilación se asociaron con más macrófagos inmunosupresores y menos células T antitumorales, mientras que bloquear la glucólisis o NDUFA4L2 cambió el equilibrio hacia un microambiente inmunitario más activo.
Qué significa esto para tratamientos futuros
Para un observador no experto, este estudio muestra que ciertos cánceres de cabeza y cuello sobreviven a la quimioterapia reconfigurando su uso de azúcar y silenciando un interruptor interno de autodestrucción. Al reducir NDUFA4L2 o bloquear la glucólisis, los investigadores pudieron disminuir el lactato, reactivar el sensor de muerte AIM2, desencadenar un agresivo programa de muerte en triple modo y hacer que el cisplatino funcionara mejor en células, organoides y ratones. Al mismo tiempo, el entorno tumoral se volvió más propicio para el ataque inmune. Estos hallazgos sugieren que los fármacos dirigidos a NDUFA4L2, o a las vías metabólicas y de lactilación que controla, podrían algún día combinarse con la quimioterapia estándar para superar la resistencia y mejorar los resultados en pacientes con cáncer de cabeza y cuello.
Cita: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
Palabras clave: cáncer de cabeza y cuello, resistencia a la quimioterapia, metabolismo tumoral, muerte celular programada, microambiente tumoral