Clear Sky Science · sv
NDUFA4L2 reglerar progression och kemoterapikänslighet hos HNSCC genom att hämma PANoptos
Varför denna forskning är viktig
Kemoterapi är en livlina för många med cancer i huvud och hals, men tumörer lär sig ofta att överlista läkemedlen. Denna studie avslöjar hur ett enda mitokondriellt protein, NDUFA4L2, hjälper skivepitelcancer i huvud och hals att undvika det vanligt använda läkemedlet cisplatin, och visar hur avstängning av detta protein både kan döda cancerceller mer effektivt och väcka immunsystemet. Arbetet pekar mot nya sätt att återställa läkemedelskänslighet genom att rikta in sig på hur cancerceller förbränner socker och dör.
En seglivad cancer och ett sviktande läkemedel
Skivepitelcancer i huvud och hals (HNSCC) är en av de vanligaste cancerformerna globalt och behandlas ofta med cisplatin. Många tumörer blir dock resistenta, vilket lämnar patienterna med begränsade alternativ. Författarna koncentrerade sig på NDUFA4L2, ett protein i cellens energifabriker (mitokondrierna) som aktiveras vid lågt syre och ändrar hur celler använder bränsle. Genom att analysera publika enkelcellsdataset och undersöka patienttumörer fann de att NDUFA4L2 är mycket aktivt i en viss undergrupp av tumörceller som kopplas till sämre överlevnad. Tumörer från patienter vars cancer inte längre svarade på kemoterapi hade särskilt höga nivåer av detta protein, vilket tyder på att det har en central roll i resistens.
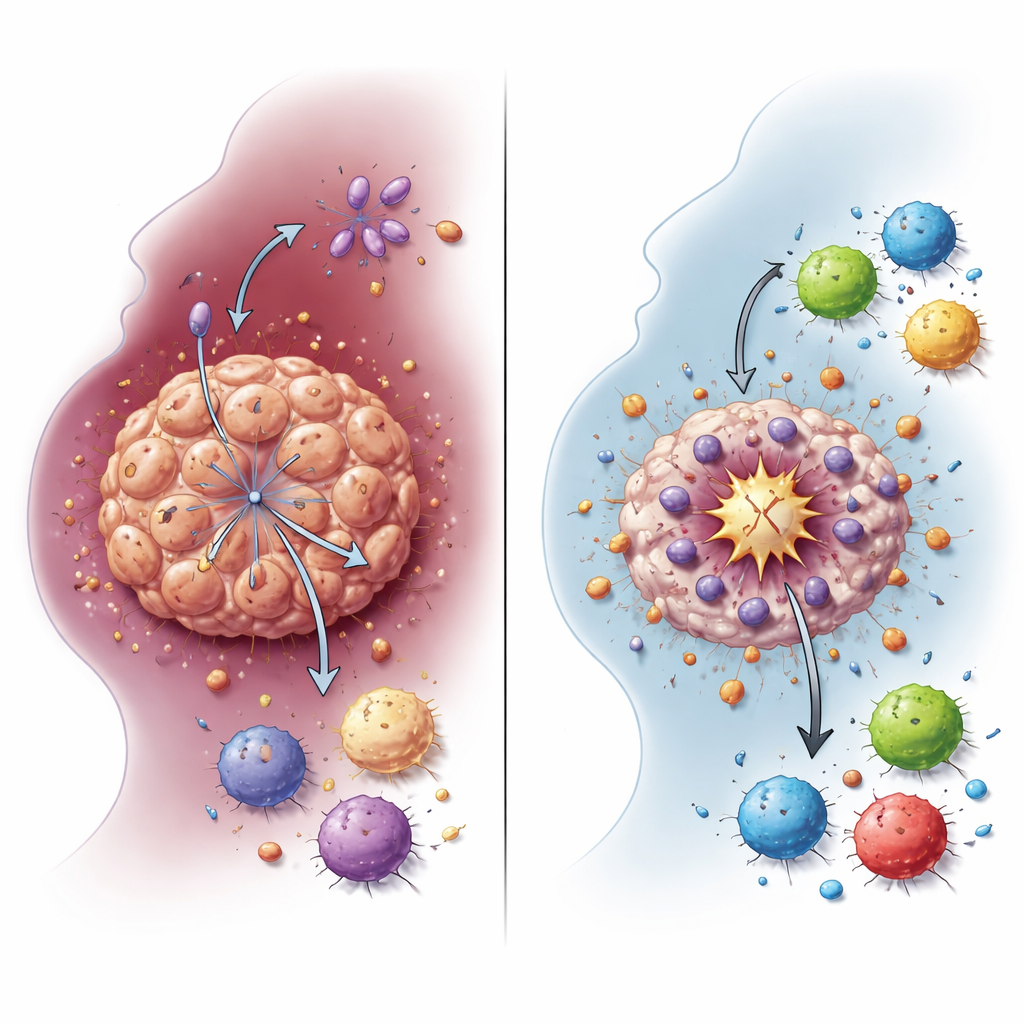
Hur en bränsleomkoppling skyddar tumörceller
Cancerceller förlitar sig ofta på en snabbare form av sockerförbränning kallad glykolys, som producerar stora mängder laktat även när syre finns tillgängligt. Teamet visade att NDUFA4L2 understöder detta glykolytiska tillstånd i HNSCC-celler. När NDUFA4L2 togs bort från cellinjer och från tredimensionella mini-tumörer odlade från patientprover sjönk laktatnivåerna kraftigt. Genuttrycksmönster skiftade bort från glykolys och laktatmetabolism, vilket kopplar NDUFA4L2 direkt till cancercellernas förändrade energianvändning. Denna bränsleomkoppling är inte bara en biprodukt av cancertillväxt: det visar sig vara en sköld som hjälper tumörceller att överleva cisplatin och undvika en särskilt potent form av celldöd.
Att tvinga cancerceller in i ett tredubbelt dödsprogram
Celler kan dö via flera reglerade vägar, inklusive apoptos, nekroptos och pyroptos. På senare tid har forskare beskrivit PANoptos, ett integrerat ”allt-i-ett”-dödsprogram som kombinerar viktiga delar av alla tre. I denna studie gjorde utslag (knockout) av NDUFA4L2 HNSCC-celler mycket mer sårbara för cisplatin. Under mikroskopet visade behandlade celler karakteristisk uppblåsning och ruptur, och biokemiska tester bekräftade samtidig aktivering av markörer för apoptos, nekroptos och pyroptos. Viktigt är att blockering av någon enskild väg bara delvis räddade cellerna, vilket indikerar att hela PANoptos-programmet var igång. I musmodeller med tungtumörer krympte tumörer, överlevnaden förlängdes och markörer för detta kombinerade dödsrespons ökade när NDUFA4L2 togs bort och cisplatin gavs.
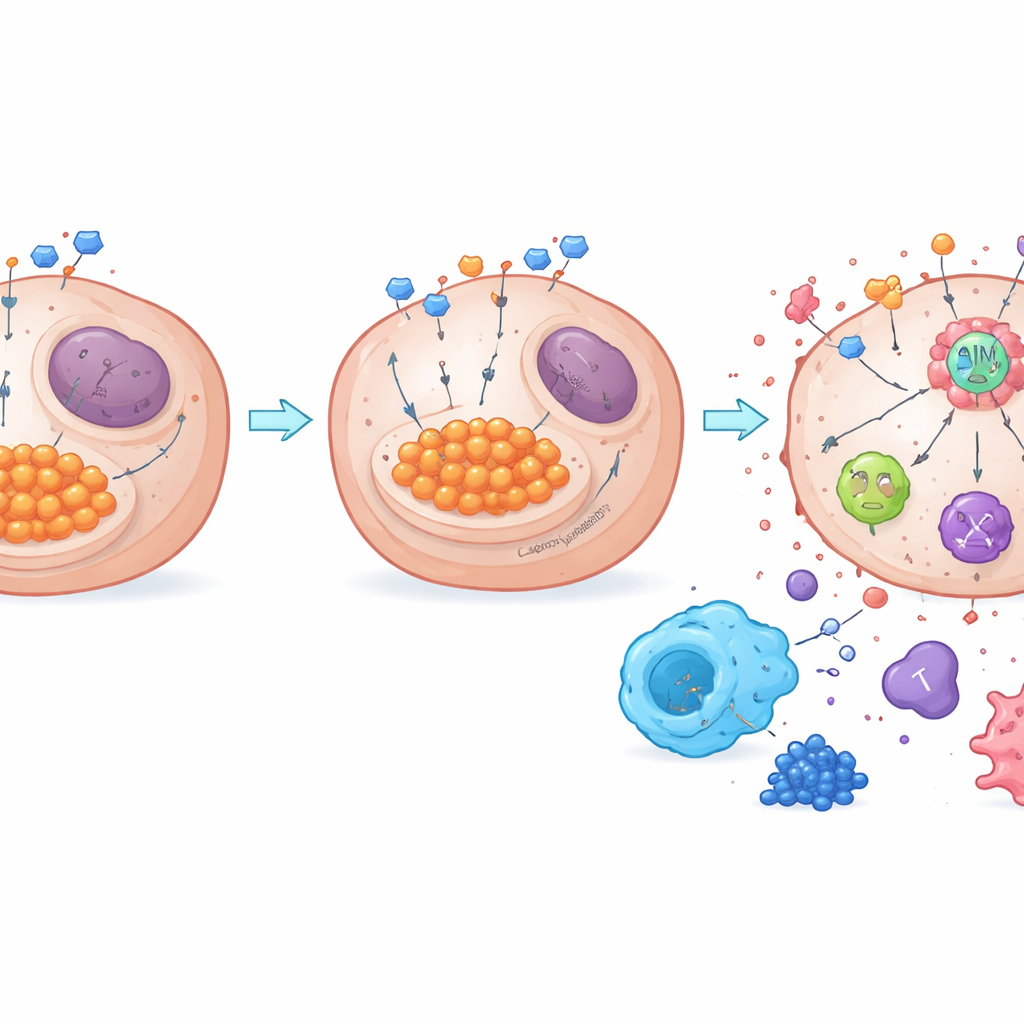
Från sockeravfall till immunväckelse
Arbetet visar också hur metabolism kopplas till en nyckelsensor för celldöd som kallas AIM2. När glykolysen är hög kan överskott av laktat kemiskt modifiera proteiner i en process känd som laktylation. Författarna upptäckte att NDUFA4L2 håller laktatnivåerna höga och främjar laktylation av AIM2, vilket tycks hålla denna sensor i ett dämpat tillstånd. Att ta bort NDUFA4L2 minskade laktat, reducerade AIM2-laktylation och stärkte bildandet av ett AIM2-baserat dödskomplex som utlöser PANoptos. När AIM2 experimentellt minskades försvann den kraftfulla dödseffekten av NDUFA4L2-borttagning plus cisplatin i stor utsträckning, vilket bekräftar AIM2:s centrala roll. Både i mustumörer och mänskliga prov var hög NDUFA4L2 och laktylation kopplat till fler immunosuppressiva makrofager och färre cancerbekämpande T‑celler, medan blockering av glykolys eller NDUFA4L2 försköt balansen mot en mer aktiv immunsituation.
Vad detta innebär för framtida behandlingar
För en lekmannabetydelse visar denna studie att vissa huvud- och halscancer överlever kemoterapi genom att omskola hur de använder socker och genom att tysta en inbyggd självdestruktionsbrytare. Genom att dämpa NDUFA4L2 eller blockera glykolys lyckades forskarna sänka laktat, återaktivera AIM2-dödssensorn, utlösa ett aggressivt tredelat celldödsprogram och göra cisplatin mer effektivt i celler, organoider och möss. Samtidigt blev tumörens omgivning mer mottaglig för immunsvar. Dessa fynd tyder på att läkemedel riktade mot NDUFA4L2, eller mot de metabola och laktylationsvägar den kontrollerar, en dag skulle kunna kombineras med standardkemoterapi för att övervinna resistens och förbättra utfallen för patienter med huvud- och halscancer.
Citering: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
Nyckelord: huvud- och halscancer, kemoterapiresistens, cancermetabolism, programmerad celldöd, tumörmikromiljö