Clear Sky Science · ja
NDUFA4L2 は PANoptosis を抑制することで HNSCC の進行と化学療法感受性を制御する
この研究が重要な理由
化学療法は多くの頭頸部がん患者にとって命綱ですが、腫瘍はしばしば薬剤を回避する術を身につけます。本研究は、ミトコンドリアタンパク質である NDUFA4L2 が、頭頸部扁平上皮癌(HNSCC)において広く使われるシスプラチンを回避させる仕組みを明らかにし、このタンパク質をオフにすることでがん細胞をより効果的に死滅させ、免疫応答を活性化できることを示します。本成果は、がん細胞の糖代謝と細胞死の制御を標的化することで薬剤感受性を回復させる新たな方策を示唆します。
手強いがんと効かなくなる薬
頭頸部扁平上皮癌(HNSCC)は世界的に多いがんの一つで、しばしばシスプラチンで治療されます。しかし多くの腫瘍が耐性を獲得し、患者の治療選択肢が限られてしまいます。著者らは低酸素下で発現が上がり細胞の燃料利用を変えるミトコンドリアタンパク質 NDUFA4L2 に着目しました。公的な単一細胞データセットの解析と患者腫瘍サンプルの検討により、NDUFA4L2 は予後不良と関連する腫瘍細胞の明確なサブグループで高く発現していることが分かりました。化学療法に反応しなくなった患者由来の腫瘍ではこのタンパク質量が特に高く、耐性に中心的な役割を果たしていることが示唆されます。
燃料スイッチが腫瘍細胞を守る仕組み
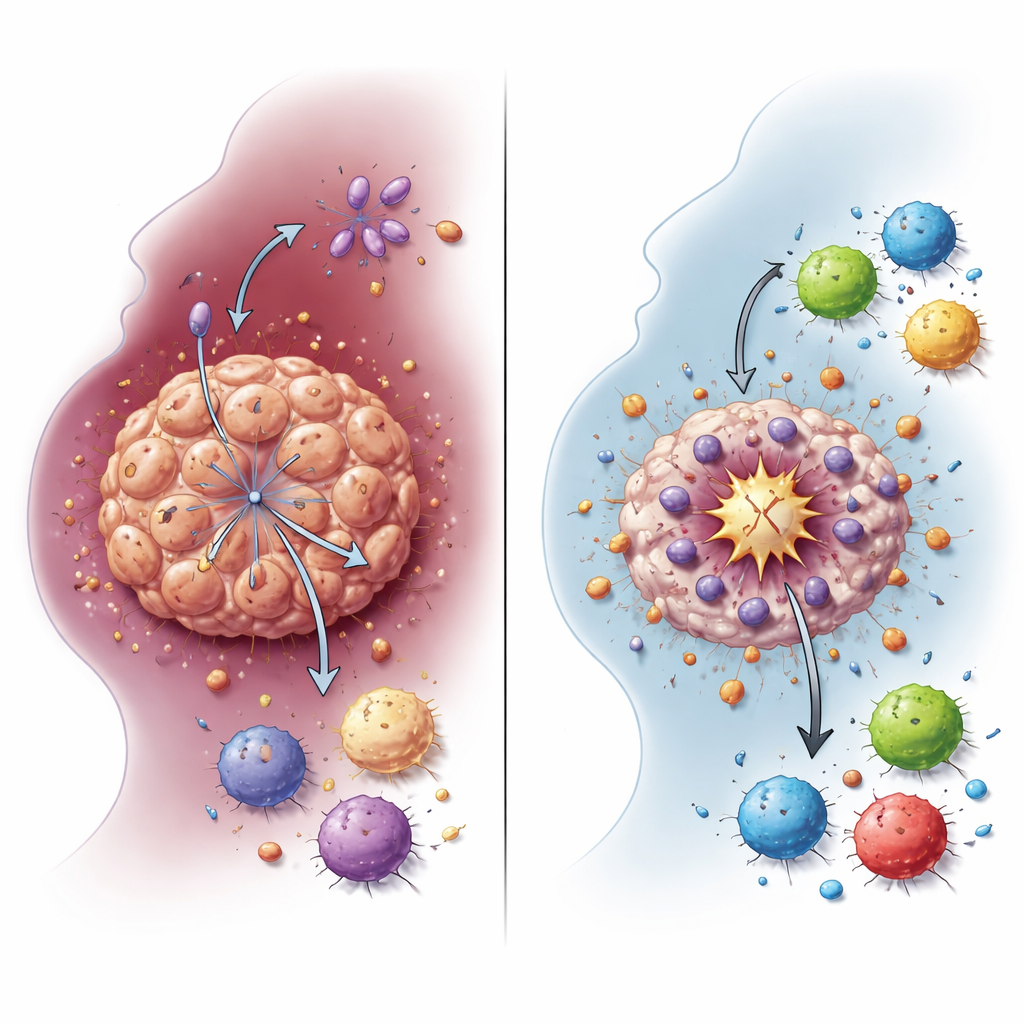
がん細胞は酸素があっても乳酸を多く作る近道的な糖の燃焼、いわゆる解糖に頼ることが多いことが知られています。研究チームは NDUFA4L2 が HNSCC 細胞におけるこの解糖状態を支持していることを示しました。細胞株や患者由来の三次元ミニ腫瘍から NDUFA4L2 を除去すると、乳酸レベルが急激に低下しました。遺伝子発現パターンも解糖と乳酸代謝から離れる方向に変化し、NDUFA4L2 ががんのエネルギー利用の変化に直接結びついていることが明らかになりました。この燃料スイッチは単なるがん増殖の副産物ではなく、シスプラチンに耐えるための盾として作用し、特に強力な細胞死の形態を回避するのに寄与していることが示されました。
がん細胞を三重の死へ追い込む
細胞はアポトーシス、ネクロプトーシス、ピロトーシスなどいくつかの制御された経路で死にます。最近、これらを統合した PANoptosis という「オールインワン」型の死プログラムが記述されました。本研究では NDUFA4L2 をノックアウトすると HNSCC 細胞がシスプラチンに対して著しく脆弱になることが示されました。顕微鏡下では処理された細胞に膨張や破裂の特徴が見られ、生化学的検査でもアポトーシス、ネクロプトーシス、ピロトーシスのマーカーが同時に活性化していることが確認されました。重要なのは、どれか一つの経路を遮断しても細胞は部分的にしか救われず、完全な PANoptosis プログラムが作動していることを示唆している点です。舌腫瘍のマウスモデルでも、NDUFA4L2 を除去してシスプラチンを投与すると腫瘍が縮小し、生存が延び、この統合された死応答のマーカーが増加しました。
糖の廃棄物から免疫の覚醒へ
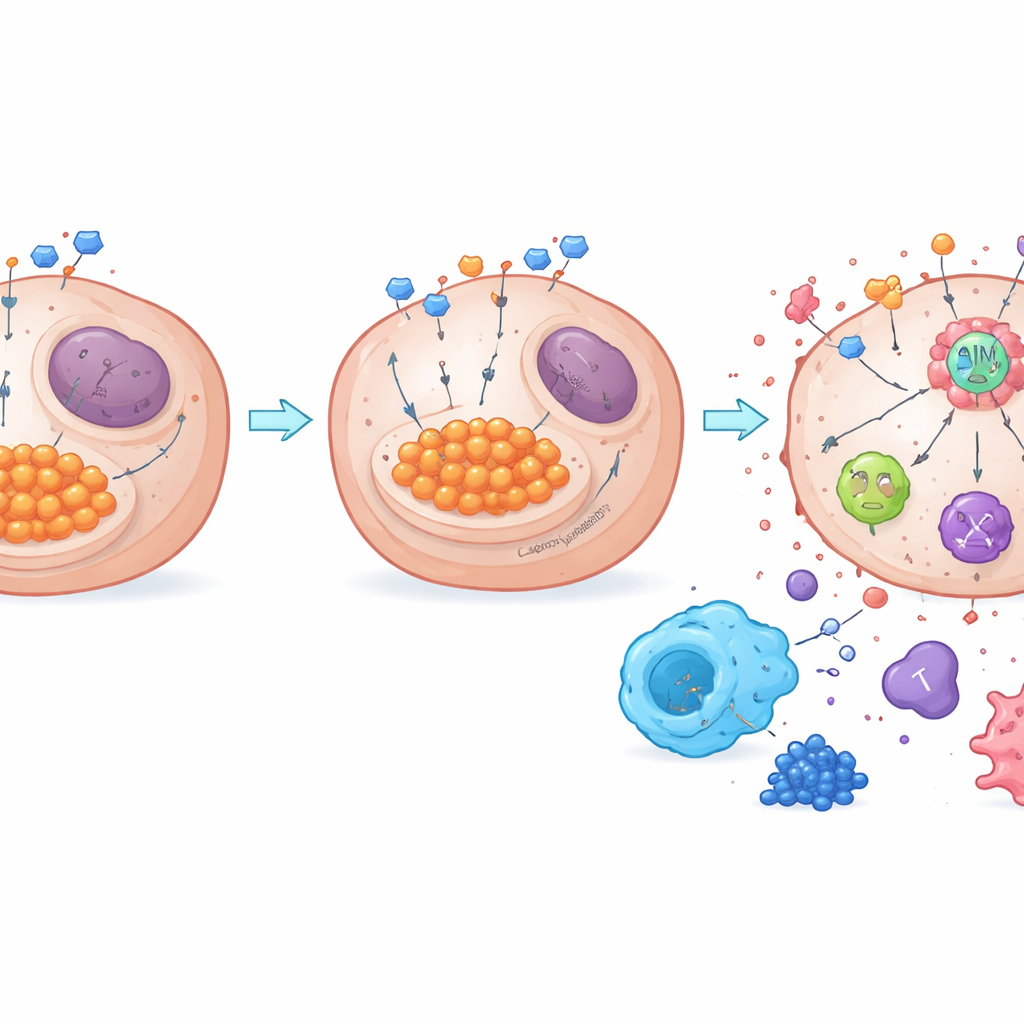
本研究は代謝と、AIM2 と呼ばれる重要な死制御センサーとの結びつきも明らかにしました。解糖が亢進すると過剰な乳酸が生じ、乳酸化(lactylation)としてタンパク質を化学的に修飾できます。著者らは NDUFA4L2 が乳酸レベルを高く保ち、AIM2 の乳酸化を促進してこのセンサーを抑圧状態にしていることを見出しました。NDUFA4L2 を除去すると乳酸と AIM2 の乳酸化が低下し、PANoptosis を引き起こす AIM2 基盤の死複合体の組み立てが強化されました。実験的に AIM2 を減らすと、NDUFA4L2 欠失とシスプラチンの組み合わせによる強力な殺傷効果は大部分が失われ、AIM2 の中心的役割が確認されました。マウス腫瘍とヒトサンプルの双方で、NDUFA4L2 と乳酸化の高値は免疫抑制的なマクロファージの増加とがんと戦う T 細胞の減少と結びついており、解糖や NDUFA4L2 を阻害すると免疫環境がより活性化する方向へシフトしました。
今後の治療への示唆
一般向けに言えば、本研究は一部の頭頸部がんが糖の使い方を書き換え、内在する自己破壊スイッチを鈍らせることで化学療法を生き延びていることを示しています。NDUFA4L2 を減らすか解糖を阻害することで乳酸が低下し、AIM2 センサーが再活性化され、攻撃的な三重モードの細胞死プログラムが誘導され、細胞、オルガノイド、マウスにおいてシスプラチンの効果が向上しました。同時に腫瘍周囲の環境は免疫攻撃に対してより受容的になりました。これらの結果は、将来的に NDUFA4L2 あるいはそれが制御する代謝・乳酸化経路を標的とする薬剤を標準的な化学療法と組み合わせることで、耐性を克服し頭頸部がん患者の成績を改善できる可能性を示唆します。
引用: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
キーワード: 頭頸部がん, 化学療法耐性, がんの代謝, プログラム細胞死, 腫瘍微小環境