Clear Sky Science · pt
NDUFA4L2 regula a progressão e a sensibilidade à quimioterapia do HNSCC ao inibir a PANoptose
Por que esta pesquisa é importante
A quimioterapia é um recurso vital para muitas pessoas com cânceres de cabeça e pescoço, mas os tumores frequentemente aprendem a escapar dos medicamentos. Este estudo revela como uma única proteína mitocondrial, NDUFA4L2, ajuda o carcinoma de células escamosas de cabeça e pescoço a driblar o medicamento amplamente usado cisplatina, e mostra como desligar essa proteína pode tanto matar as células cancerosas de forma mais eficaz quanto reativar o sistema imunológico. O trabalho aponta para novas maneiras de restaurar a sensibilidade aos medicamentos ao visar como as células tumorais queimam açúcar e morrem.
Um câncer persistente e um medicamento que falha
O carcinoma de células escamosas de cabeça e pescoço (HNSCC) está entre os cânceres mais comuns no mundo e é frequentemente tratado com cisplatina. Muitos tumores, entretanto, tornam-se resistentes, deixando os pacientes com opções limitadas. Os autores concentraram-se em NDUFA4L2, uma proteína nas usinas de energia da célula (mitocôndrias) que é ativada em condições de baixo oxigênio e altera como as células usam combustível. Ao analisar conjuntos de dados públicos de célula única e examinar amostras de tumores de pacientes, eles descobriram que NDUFA4L2 está altamente ativa em um subgrupo distinto de células tumorais associado a pior sobrevida. Tumores de pacientes cujos cânceres não respondiam mais à quimioterapia apresentaram quantidades especialmente altas dessa proteína, sugerindo que ela desempenha um papel central na resistência.
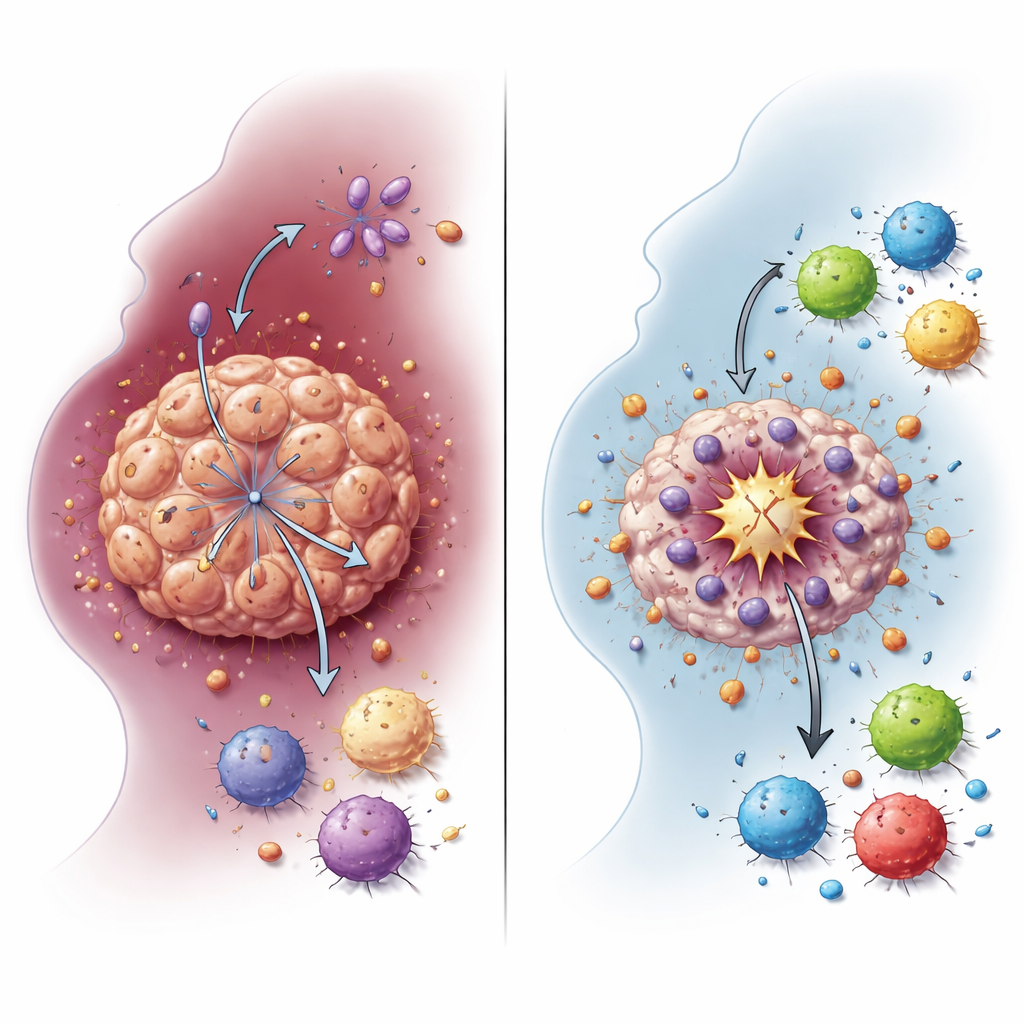
Como uma mudança de combustível protege as células tumorais
As células cancerosas muitas vezes dependem de uma forma atalho de queima de açúcar chamada glicólise, que produz grandes quantidades de lactato mesmo quando há oxigênio disponível. A equipe mostrou que NDUFA4L2 sustenta esse estado glicolítico em células de HNSCC. Quando NDUFA4L2 foi removida de linhagens celulares e de mini-tumores tridimensionais cultivados a partir de amostras de pacientes, os níveis de lactato caíram abruptamente. Padrões de atividade gênica deslocaram-se para longe da glicólise e do metabolismo do lactato, vinculando NDUFA4L2 diretamente ao uso de energia alterado do câncer. Essa mudança de combustível não é apenas um subproduto do crescimento tumoral: revela-se como um escudo que ajuda as células tumorais a sobreviver à cisplatina e a evitar uma forma especialmente potente de morte celular.
Forçando as células cancerosas a um programa triplo de morte
As células podem morrer por várias vias reguladas, incluindo apoptose, necroptose e piroptose. Recentemente, pesquisadores descreveram a PANoptose, um programa integrado de “tudo-em-um” que combina partes-chave das três vias. Neste estudo, a eliminação de NDUFA4L2 tornou as células de HNSCC muito mais vulneráveis à cisplatina. Ao microscópio, as células tratadas mostraram o característico inchaço e ruptura, e testes bioquímicos confirmaram a ativação simultânea de marcadores de apoptose, necroptose e piroptose. Importante, bloquear qualquer uma das vias apenas resgatou parcialmente as células, indicando que o programa completo de PANoptose estava em ação. Em modelos de camundongos com tumores de língua, remover NDUFA4L2 e administrar cisplatina reduziu os tumores, prolongou a sobrevida e aumentou marcadores dessa resposta combinada de morte.
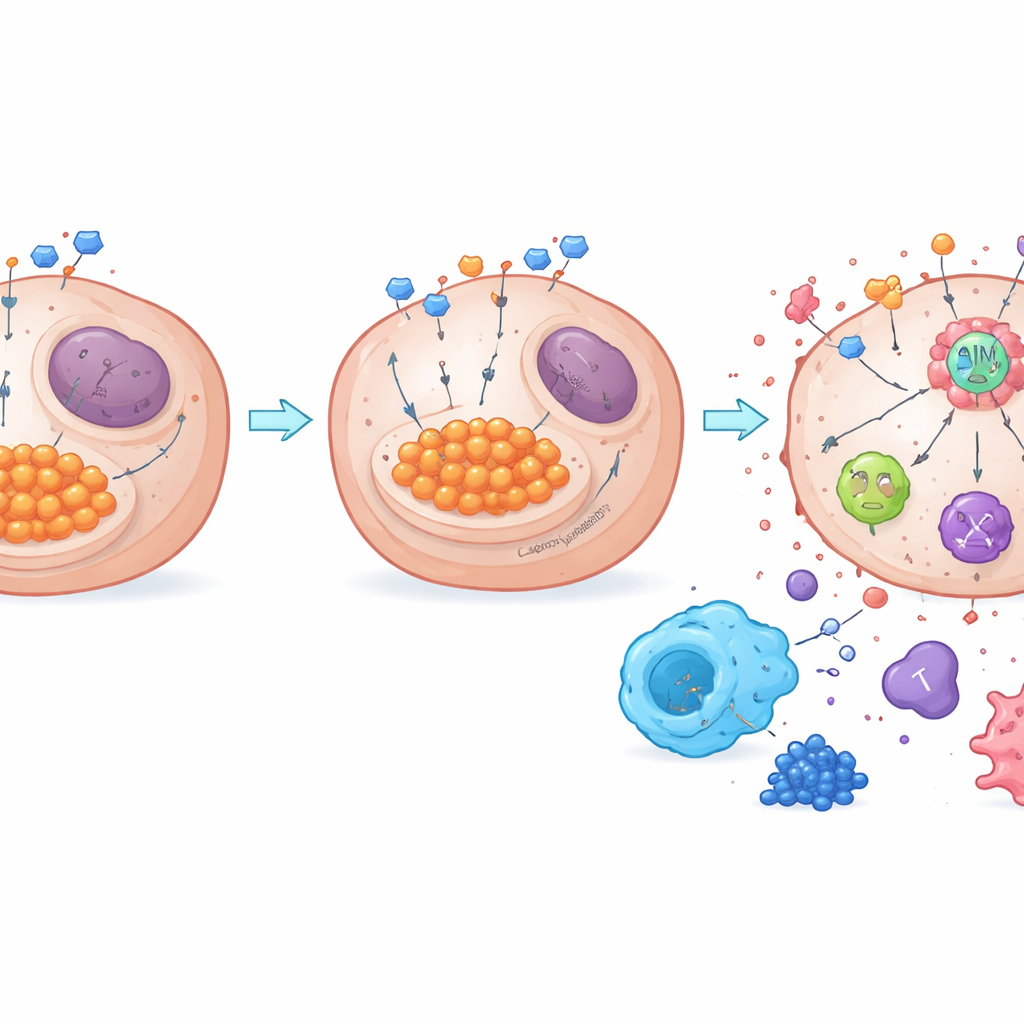
Do desperdício de açúcar ao despertar imunológico
O trabalho também revela como o metabolismo se conecta a um sensor chave que regula a morte chamado AIM2. Quando a glicólise é alta, o excesso de lactato pode modificar quimicamente proteínas em um processo conhecido como lactilação. Os autores descobriram que NDUFA4L2 mantém os níveis de lactato elevados e promove a lactilação de AIM2, o que parece manter esse sensor em um estado subjugado. Remover NDUFA4L2 reduziu o lactato, diminuiu a lactilação de AIM2 e fortaleceu a montagem de um complexo de morte baseado em AIM2 que desencadeia a PANoptose. Quando AIM2 foi reduzido experimentalmente, o potente efeito de morte da perda de NDUFA4L2 mais cisplatina praticamente desapareceu, confirmando o papel central de AIM2. Tanto em tumores de camundongo quanto em amostras humanas, altos níveis de NDUFA4L2 e de lactilação estiveram associados a mais macrófagos imunossupressores e menos células T anti-tumorais, enquanto bloquear a glicólise ou NDUFA4L2 deslocou o equilíbrio para um ambiente imune mais ativo.
O que isso significa para tratamentos futuros
Para um observador leigo, este estudo mostra que certos cânceres de cabeça e pescoço sobrevivem à quimioterapia ao reconfigurar como usam açúcar e ao silenciar um gatilho interno de autodestruição. Ao reduzir NDUFA4L2 ou bloquear a glicólise, os pesquisadores conseguiram diminuir o lactato, reativar o sensor de morte AIM2, desencadear um agressivo programa triplo de morte celular e tornar a cisplatina mais eficaz em células, organoides e camundongos. Ao mesmo tempo, o microambiente tumoral tornou-se mais receptivo ao ataque imunológico. Esses achados sugerem que drogas direcionadas a NDUFA4L2, ou às vias metabólicas e de lactilação que ela controla, poderiam algum dia ser combinadas com a quimioterapia padrão para superar a resistência e melhorar os resultados para pacientes com câncer de cabeça e pescoço.
Citação: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
Palavras-chave: câncer de cabeça e pescoço, resistência à quimioterapia, metabolismo do câncer, morte celular programada, microambiente tumoral