Clear Sky Science · ru
NDUFA4L2 регулирует прогрессирование и чувствительность к химиотерапии при HNSCC, подавляя PANoptosis
Почему это исследование важно
Химиотерапия — жизненная поддержка для многих пациентов с опухолями головы и шеи, но нередко опухоли со временем «обходят» действие препаратов. В этом исследовании показано, как один митохондриальный белок, NDUFA4L2, помогает плоскоклеточному раку головы и шеи уклоняться от широко применяемого цисплатина, и как подавление этого белка одновременно усиливает гибель раковых клеток и пробуждает иммунную систему. Работа указывает на новые подходы к восстановлению чувствительности к препаратам через вмешательство в метаболизм глюкозы и механизмы клеточной гибели.
Упорная опухоль и утраченный эффект препарата
Плоскоклеточный рак головы и шеи (HNSCC) относится к числу наиболее распространённых онкопатологий в мире и часто лечится цисплатином. Однако многие опухоли приобретают устойчивость, оставляя пациентам мало вариантов лечения. Авторы сосредоточились на NDUFA4L2 — белке митохондрий, включающемся при низком уровне кислорода и меняющем пути использования топлива в клетке. Анализируя публичные данные одиночных клеток и образцы опухолей пациентов, они обнаружили высокую активность NDUFA4L2 в отдельной подгруппе опухолевых клеток, связанной с плохим прогнозом. В опухолях пациентов, у которых рак перестал реагировать на химиотерапию, этот белок встречался в особенно больших количествах, что указывает на его центральную роль в резистентности.
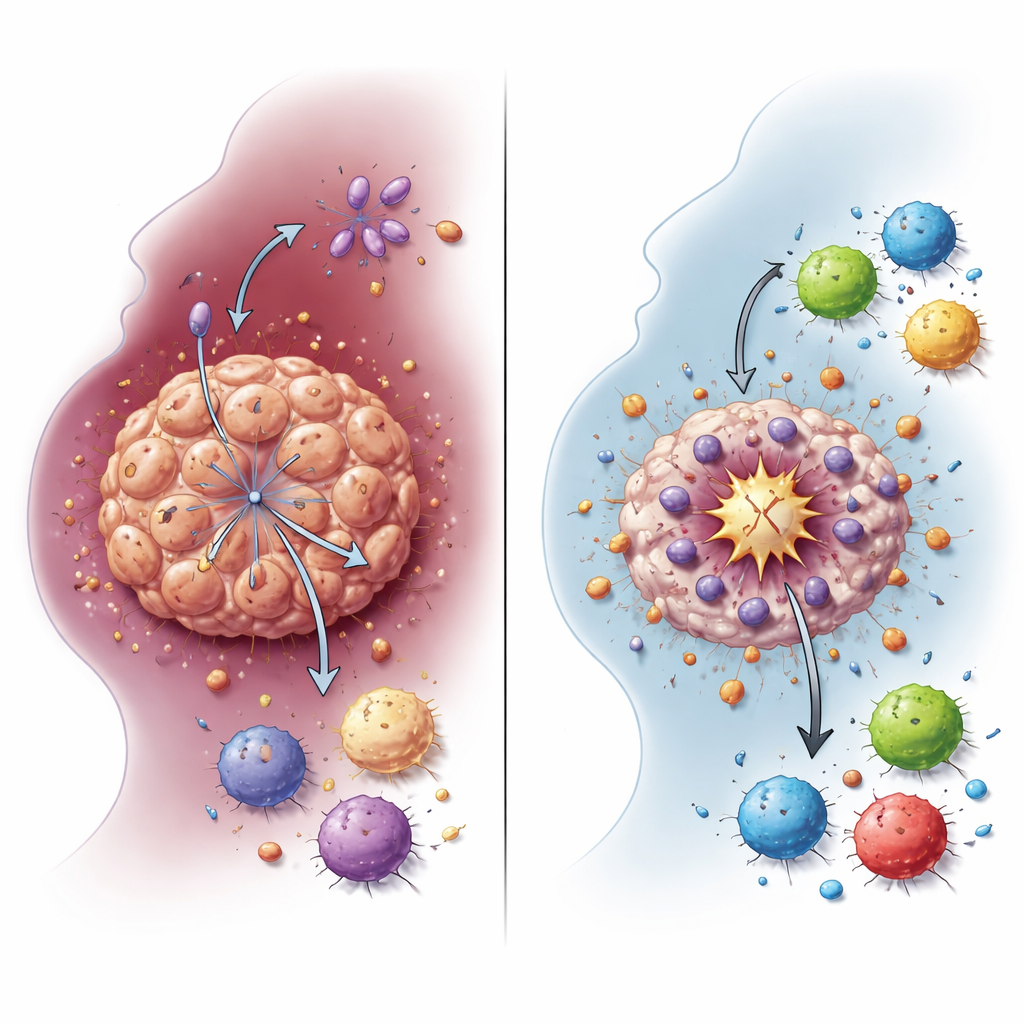
Как переключение топлива защищает опухолевые клетки
Раковые клетки часто полагаются на упрощённый путь расщепления сахара — гликолиз, который даёт большое количество лактата даже при наличии кислорода. Исследователи показали, что NDUFA4L2 поддерживает это гликолитическое состояние в клетках HNSCC. При удалении NDUFA4L2 из линий клеток и из трёхмерных мини-опухолей, выращенных из образцов пациента, уровни лактата резко снижались. Паттерны экспрессии генов смещались от гликолиза и метаболизма лактата, напрямую связывая NDUFA4L2 с изменённым энергетическим поведением рака. Это переключение топлива — не просто побочный продукт роста опухоли: оно служит щитом, помогающим клеткам выживать при обработке цисплатином и избегать особенно мощной формы гибели.
Принуждение клеток к тройной программе гибели
Клетки могут гибнуть по нескольким регулируемым путям, включая апоптоз, некроптоз и пироптоз. В последнее время описали PANoptosis — интегрированную «всё-в-одном» программу гибели, комбинирующую ключевые элементы всех трёх путей. В этом исследовании удаление NDUFA4L2 делало клетки HNSCC значительно более уязвимыми к цисплатину. При микроскопии обработанные клетки демонстрировали характерное раздувание и разрыв, а биохимические тесты подтвердили одновременную активацию маркеров апоптоза, некроптоза и пироптоза. Важно, что блокирование любого одного пути лишь частично спасало клетки, что указывает на вовлечение полной программы PANoptosis. В мышиных моделях опухолей языка удаление NDUFA4L2 в сочетании с цисплатином приводило к уменьшению объёма опухолей, увеличению выживаемости и росту маркеров этой объединённой реакции гибели.
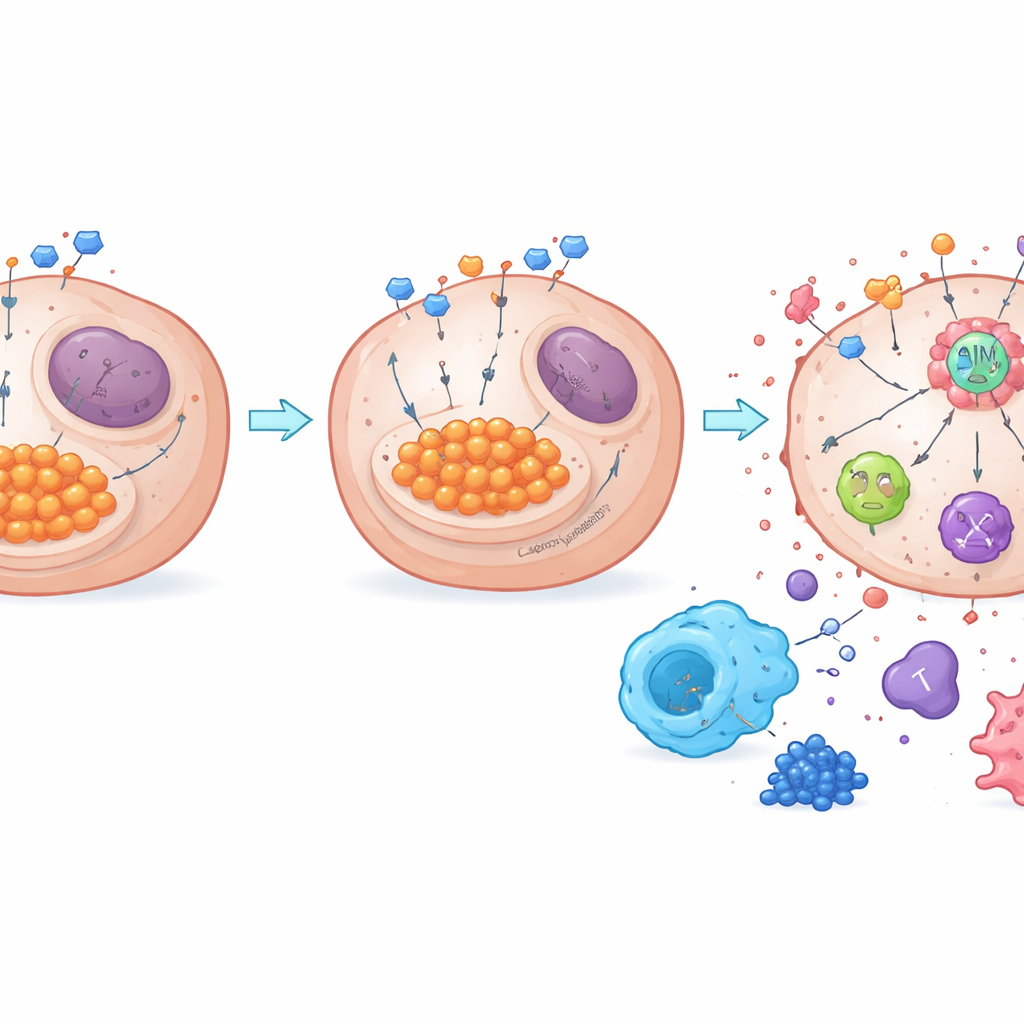
От отходов сахара к пробуждению иммунитета
Работа также раскрывает связь между метаболизмом и ключевым датчиком, регулирующим гибель, — AIM2. При высоком гликолизе избыток лактата может химически модифицировать белки в процессе, известном как лактиляция. Авторы показали, что NDUFA4L2 поддерживает высокий уровень лактата и способствует лактиляции AIM2, что, по-видимому, удерживает этот датчик в подавленном состоянии. Удаление NDUFA4L2 снижало лактат, уменьшало лактиляцию AIM2 и усиливало сборку AIM2-основанного комплекса гибели, запускающего PANoptosis. При экспериментальном уменьшении AIM2 мощный летальный эффект от потери NDUFA4L2 в сочетании с цисплатином в значительной мере ослабевал, что подтверждает центральную роль AIM2. В мышиных опухолях и в образцах пациентов высокий уровень NDUFA4L2 и лактиляции ассоциировался с большим числом иммуноподавляющих макрофагов и меньшим количеством противоопухолевых Т-клеток, тогда как блокирование гликолиза или NDUFA4L2 смещало баланс в сторону более активного иммунного окружения.
Что это значит для будущих лечений
Для непрофессионала это исследование показывает, что некоторые раки головы и шеи выживают после химиотерапии, перенастраивая использование сахара и «отключая» встроенный выключатель самоуничтожения. При снижении активности NDUFA4L2 или блокировании гликолиза исследователи уменшали уровень лактата, восстанавливали активность сенсора AIM2, запускали агрессивную тройную программу гибели клеток и повышали эффективность цисплатина в клетках, органоидах и мышах. Одновременно микроокружение опухоли становилось более благоприятным для иммунной атаки. Эти результаты дают основание полагать, что препараты, нацеленные на NDUFA4L2 или на метаболические и лактиляционные пути, которые он контролирует, в будущем могут быть использованы вместе со стандартной химиотерапией для преодоления резистентности и улучшения исходов у пациентов с раком головы и шеи.
Цитирование: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
Ключевые слова: рак головы и шеи, резистентность к химиотерапии, метаболизм рака, запрограммированная гибель клеток, микроокружение опухоли