Clear Sky Science · fr
NDUFA4L2 régule la progression et la sensibilité à la chimiothérapie du HNSCC en inhibant la PANoptose
Pourquoi cette recherche est importante
La chimiothérapie est une bouée de sauvetage pour de nombreuses personnes atteintes de cancers de la tête et du cou, pourtant les tumeurs apprennent souvent à déjouer les médicaments. Cette étude révèle comment une seule protéine mitochondriale, NDUFA4L2, aide le carcinome épidermoïde de la tête et du cou à échapper au cisplatine, médicament largement utilisé, et montre que l’inhibition de cette protéine peut à la fois tuer les cellules tumorales plus efficacement et réveiller le système immunitaire. Ce travail ouvre la voie à de nouvelles stratégies pour restaurer la sensibilité aux médicaments en ciblant la façon dont les cellules cancéreuses métabolisent le glucose et meurent.
Un cancer tenace et un médicament qui faiblit
Le carcinome épidermoïde de la tête et du cou (HNSCC) est l’un des cancers les plus fréquents au monde et est souvent traité par cisplatine. De nombreuses tumeurs deviennent cependant résistantes, laissant les patients avec peu d’options. Les auteurs se sont concentrés sur NDUFA4L2, une protéine des centrales énergétiques de la cellule (mitochondries) qui s’active en conditions d’hypoxie et modifie l’utilisation des carburants par la cellule. En analysant des jeux de données unicellulaires publics et des échantillons tumoraux de patients, ils ont montré que NDUFA4L2 est fortement exprimée dans un sous-groupe distinct de cellules tumorales associé à une survie défavorable. Les tumeurs de patients dont le cancer ne répondait plus à la chimiothérapie présentaient des niveaux particulièrement élevés de cette protéine, ce qui suggère qu’elle joue un rôle central dans la résistance.
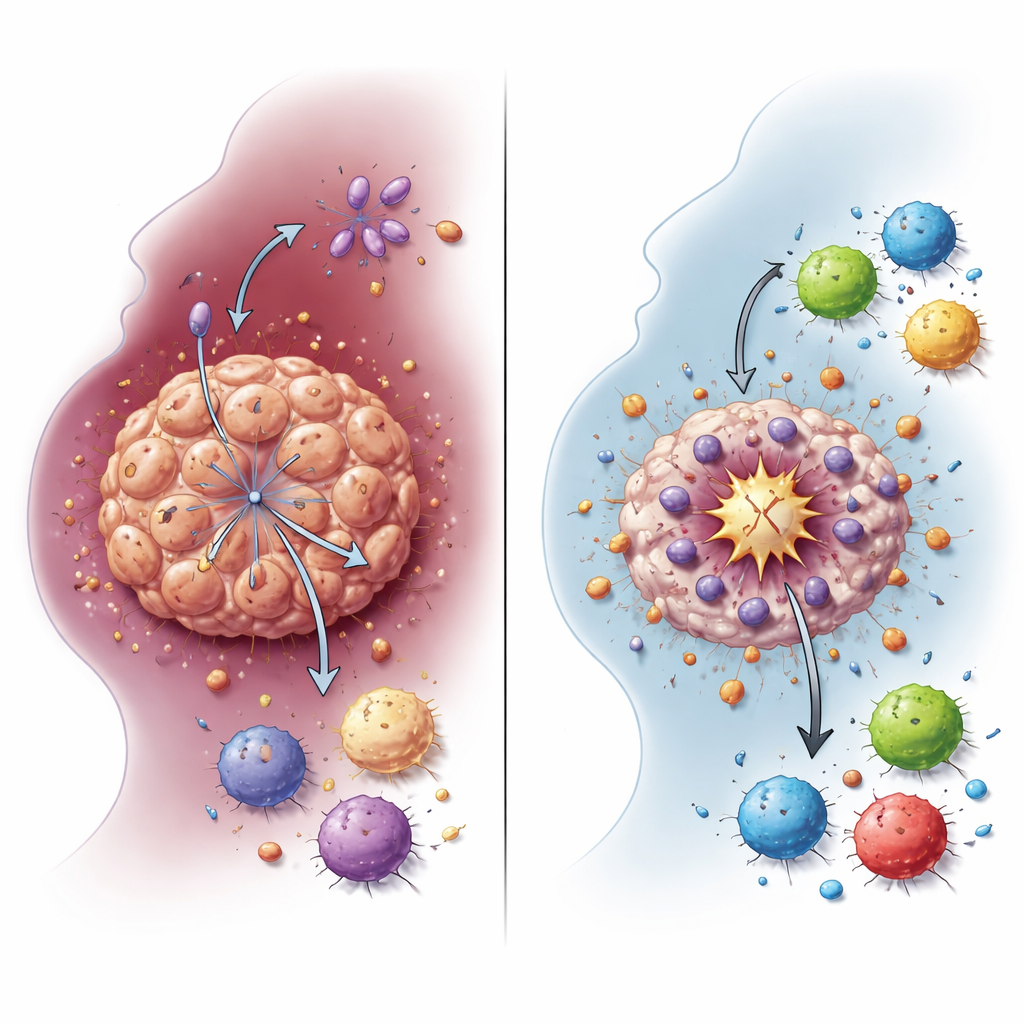
Comment un changement de carburant protège les cellules tumorales
Les cellules cancéreuses s’appuient souvent sur une forme raccourcie de combustion du glucose appelée glycolyse, qui produit de grandes quantités de lactate même en présence d’oxygène. L’équipe a montré que NDUFA4L2 soutient cet état glycolytique dans les cellules de HNSCC. Lorsqu’on a supprimé NDUFA4L2 dans des lignées cellulaires et dans des mini-tumeurs tridimensionnelles issues d’échantillons de patients, les niveaux de lactate ont chuté fortement. Les profils d’expression génique se sont décalés loin de la glycolyse et du métabolisme du lactate, reliant directement NDUFA4L2 à l’utilisation énergétique altérée du cancer. Ce basculement métabolique n’est pas seulement un sous-produit de la croissance tumorale : il constitue un bouclier qui aide les cellules tumorales à survivre au cisplatine et à échapper à une forme particulièrement puissante de mort cellulaire.
Forcer les cellules cancéreuses dans un programme de mort triple
Les cellules peuvent mourir par plusieurs voies régulées, notamment l’apoptose, la nécroptose et la pyroptose. Récemment, des chercheurs ont décrit la PANoptose, un programme de mort intégré « tout-en-un » combinant des éléments clés des trois voies. Dans cette étude, l’extinction de NDUFA4L2 rendait les cellules de HNSCC beaucoup plus vulnérables au cisplatine. Au microscope, les cellules traitées montraient les signes caractéristiques de gonflement et de rupture, et des tests biochimiques confirmaient l’activation simultanée de marqueurs d’apoptose, de nécroptose et de pyroptose. De manière importante, le blocage d’une voie seule ne sauvait que partiellement les cellules, ce qui indique que le programme complet de PANoptose était engagé. Dans des modèles murins de tumeurs de la langue, la suppression de NDUFA4L2 associée au cisplatine réduisait les tumeurs, prolongeait la survie et augmentait les marqueurs de cette réponse de mort combinée.
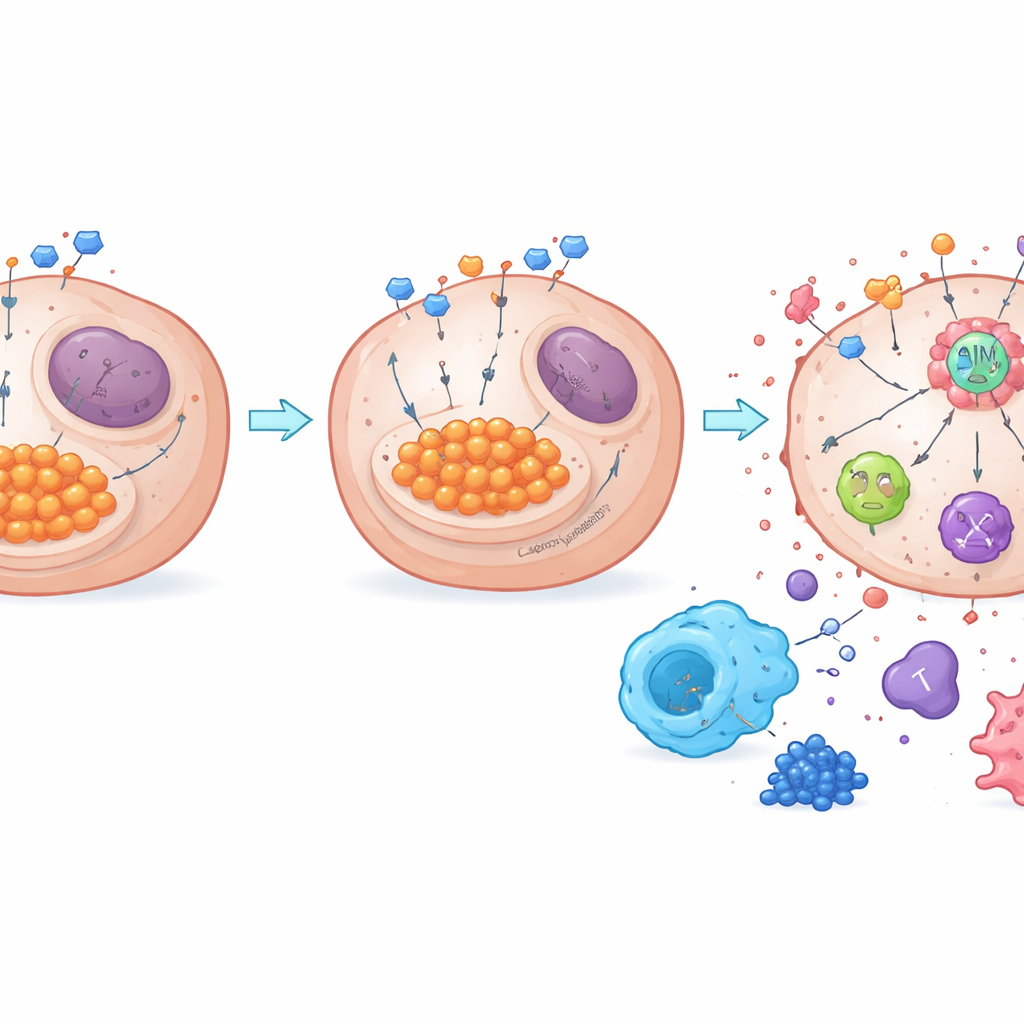
Du déchet de sucre à l’éveil immunitaire
Le travail révèle aussi comment le métabolisme se relie à un capteur clé de la mort cellulaire appelé AIM2. Lorsque la glycolyse est élevée, l’excès de lactate peut modifier chimiquement des protéines dans un processus appelé lactylation. Les auteurs ont découvert que NDUFA4L2 maintient des niveaux élevés de lactate et favorise la lactylation d’AIM2, ce qui semble maintenir ce capteur dans un état atténué. La suppression de NDUFA4L2 abaissait le lactate, réduisait la lactylation d’AIM2 et renforçait l’assemblage d’un complexe de mort basé sur AIM2 déclenchant la PANoptose. Lorsque AIM2 était réduit expérimentalement, l’effet létal puissant de la perte de NDUFA4L2 combinée au cisplatine s’est largement estompé, confirmant le rôle central d’AIM2. Tant dans les tumeurs murines que dans les échantillons humains, des niveaux élevés de NDUFA4L2 et de lactylation étaient associés à davantage de macrophages immunosuppresseurs et à moins de lymphocytes T anti-tumoraux, alors que le blocage de la glycolyse ou de NDUFA4L2 favorisait un microenvironnement immunitaire plus actif.
Ce que cela signifie pour les traitements futurs
Pour le lecteur non spécialiste, cette étude montre que certains cancers de la tête et du cou survivent à la chimiothérapie en reconfigurant leur utilisation du glucose et en neutralisant un interrupteur d’autodestruction intégré. En diminuant NDUFA4L2 ou en bloquant la glycolyse, les chercheurs ont pu abaisser le lactate, réactiver le capteur de mort AIM2, déclencher un programme de mort cellulaire agressif en triple mode et améliorer l’efficacité du cisplatine dans des cellules, des organoïdes et des modèles murins. Parallèlement, l’environnement tumoral devenait plus favorable à l’attaque immunitaire. Ces résultats suggèrent que des médicaments ciblant NDUFA4L2, ou les voies métaboliques et de lactylation qu’elle contrôle, pourraient un jour être associés à la chimiothérapie standard pour surmonter la résistance et améliorer les résultats chez les patients atteints de cancer de la tête et du cou.
Citation: Cui, JJ., Yang, Y., Zhao, JH. et al. NDUFA4L2 regulates the progression and chemotherapy sensitivity of HNSCC by inhibiting PANoptosis. npj Precis. Onc. 10, 154 (2026). https://doi.org/10.1038/s41698-026-01358-5
Mots-clés: cancer de la tête et du cou, résistance à la chimiothérapie, métabolisme du cancer, mort cellulaire programmée